Сульфування - Хімія та технологія основного органічного і нафтохімічного синтезу
Сульфуванням називають взаємодію органічної сполуки з концентрованою сірчаною кислотою і деякими її похідними, у результаті якого атом водню замінюється сульфогрупою та утворюються сульфокислоти.

Сульфування є однією з найважливіших реакцій органічного синтезу в ряду сполук (феноли, нафтол, крезоли, резорцин, барвники, фізіологічно активні сполуки, ПАР). Крім того, введення сульфогрупи використовують для надання хімічним сполукам кислих властивостей, розчинності у воді.
Сульфуючи агенти:
- 1. Сірчана кислота концентрована, 98-100 % моногідрат. 2. Олеум - сірчана кислота, що димить, містить 20-25 % або 60-65 % SO3, який розчинено у моногідраті. 3. Хлорсульфонова кислота - монохлорангідрид сірчаної кислоти, який утворюється із сірчаного ангідриду і НСl.
Для сульфування високореакційних сполук, нестабільних у кислому середовищі, іноді застосовують продукти приєднання сірчаного ангідриду до піридину або діоксану в надлишку цих розчинників.

Найчастіше для сульфування застосовують сірчану кислоту, реакція якої з ароматичними сполуками оборотна. Швидкість сульфування дуже сильно залежить від концентрації сірчаної кислоти. Оскільки при реакції утворюється вода, що розбавляє сірчану кислоту, швидкість сульфування може впасти до повного припинення реакції. У зв'язку з цим, масу агента, що сульфує, необхідного для проведення реакції, розраховують не по стехіометричному співвідношенню, а по концентрації сірчаної кислоти, що повинна утворитися після завершення процесу сульфування. Ця маса неоднакова для різноманітних сполук і залежить від їхньої реакційної спроможності. За інших рівних умов вона може бути тим нижче, чим активніше ароматичне сполучення. Це явище характеризують величиною "-сульфування". Вона чисельно дорівнює масовій долі SO3 у відпрацьованій кислоті, при якій сульфування більше не йде. Наприклад, для бензолу =64; для нафталіну - 56, для нітробензолу - 82. Знаючи - сульфування і масову долю SO3 у вихідній кислоті - , розраховують необхідну для сульфування 1 моля ароматичної сполуки масу кислоти за формулою

Де 80 - молярна маса SO3.
Наведена формула показує, що для зниження витрати Н2SO4 і зменшення кількості відпрацьованої кислоти потрібно використовувати більш концентровану сірчану кислоту. Так, при сульфуванні бензолу купоросним маслом = 75%, = 64. Мінімальна кількість купоросного масла складає 262 г, а для реакції з 100%-ною Н2SO4 (моногідрат) = 81.7 потрібно тільки 162 г. При цьому утворюється відповідно 182 та 82 г відпрацьованої кислоти.
Реакція сульфування протікає порівняно повільно. Тому, хоча вона й екзотермічна (тепловий ефект 126 - 168 кДж/моль), її частіше усього проводять при нагріванні. Реакційна маса може бути гетерогенна, і тому дуже важливо ефективне перемішування.
Сульфування олеумом
Реакції ароматичних сполук з олеумом протікають у дві стадії. На першій стадії відбувається перетворення надлишкового сірчаного ангідриду

Ця реакція необоротна і високо екзотермічна (180 кДж/моль для 20%-ного олеуму). В другій стадії сульфування участь починає приймати сірчана кислота. Закономірності її взаємодії з ароматичними сполуками розглянуто вище. При використанні олеуму та SO3 на відміну від сульфування сірчаною кислотою протікає значно більше число реакцій. Висока активність цих агентів дозволяє вступ у ядро другої сульфогрупи по типовій схемі послідовних перетворень

Це використовують у цільовому синтезі м-бензолдісульфокислоти і з неї - резорцину, коли першу стадію ведуть за допомогою Н2SO4, а другу - під дією олеуму.
При сульфуванні олеумом і SO3 утворюється деяка кількість сульфонів

Ця реакція особливо помітна для бензолу, для алкілбензолів вона спостерігається в незначному ступені.
Інша побічна реакція утворює ангідриди сульфокислот, вихід яких росте при надлишку SO3
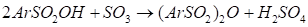
При дії невеличкої кількості води можна перетворити ангідриди в цільові сульфокислоти.
Сульфохлориди (сульфонілхлориди) - звичайно одержують, сульфуючи ароматичні сполуки хлорсульфоновою кислотою. На першому етапі реакції утворюється сульфокислота.
Ця стадія реакції необоротна, тому що вода в реакційній масі відсутня. Далі по рівноважній реакції з хлорсульфоновою кислотою утворюється сульфохлорид.


Щоб усунути цю рівновагу праворуч, необхідний надлишок хлорсульфонової кислоти. Тому звичайно для сульфування беруть не менше 4-5 моль хлорсульфонової кислоти на 1 моль вихідного сполучення. Після проведення реакції, сульфомасу обережно виливають на колотий лід або охолоджену воду, продукт реакції відокремлюють фільтруванням або (якщо він рідкий) розшаровуванням. Сульфохлориди утворюються також при дії PCl5 на сульфокислоти та їхні солі. Їх використовують як ацилюючі агенти для одержання сульфамідів, а відновленням одержують сульфінові кислоти і тіофеноли.
Аміносульфокислоти
Аміногрупа є одним із сильніших електронодонорних заступників і спрямовує сульфогрупу в о - і п-положення. Проте, при дії сірчаної кислоти або олеуму аміногрупа протонується, причому рівновага майже цілком зміщується праворуч


Протонована аміногрупа (амонієва) є вже сильним електроноакцепторним заступником, який мінімально гальмує реакцію в мета-положенні. Тому при прямому сульфуванні амінів практично неминуче утворення ізомерів, що, як правило, важко розділяються. Тому для одержання чистих індивідуальних продуктів користуються обхідними методами або застосовують так звану "реакцію запікання". Наприклад, бісульфат аніліну при цьому через N-фенілсульфамінову кислоту утворює сульфанілову кислоту - п-амінобензолсульфокислоту:

Цю реакцію здійснюють шляхом тривалого нагрівання заздалегідь приготовлених сульфатів (бісульфатів) ароматичних амінів при визначеній температурі, звичайно яка не перевищує 2000С. Раніш це робили на металевих листах у спеціальних печах при заданій температурі. В теперішній час у промисловості бісульфати амінів нагрівають в органічних розчинниках, що мають високу температуру кипіння, (наприклад, поліхлориди бензолу). Це забезпечує значно більш рівномірний обігрів й виключає підгорання твердого продукту.
Похожие статьи
-
Пластичными массами называют материалы, полученные на основе полимеров, содержащие различные добавки и способные под влиянием температуры и давления,...
-
1. Окиснення спиртів. Первинні спирти окиснюються до альдегідів, а вторинні - до кетонів. 3. Гідратація алкінів (реакція Кучерова) . З ацетилену в умовах...
-
Комплекс фізико-механічних, хімічних і діелектричних властивостей поліетилену дозволяє широко застосовувати цей матеріал в багатьох галузях промисловості...
-
Бромистый этил представляет бесцветную прозрачную жидкость, обладающую эфирным запахом и сначала сладким, потом жгучим вкусом. Кипит при 38,4°С. В воде...
-
Антрацен - соединение, молекула которого состоит из трех ароматических колец, лежащих в одной плоскости. Его получают из антраценовой фракции...
-
Основные опасности при перегонке связаны с использованием электрических нагревательных приборов (электроплитки, колбонагреватели). 1. Шнур (нельзя...
-
Данные для расчета: Основная реакция: (1) Побочные реакции: Рабочий объем катализатора - 24 м3. Расход оксида углерода и метанола на побочные продукты с...
-
5.1 Основные опасности при работе с концентрированными кислотами 1. Сильные неорганические кислоты при попадании на кожу вызывают химические ожоги. При...
-
Реакції, в які вступають спирти, супроводжуються розривом зв'язків О-Н або С-О. 1. Кислотні властивості спиртів. Утворення алкоголятів. Спирти не...
-
Оптимальний процес полімеризації в реакторі протікає при дотриманні певних параметрів в межах норми. Основними параметрами регулювання, які забезпечують...
-
Общая методика. В трехгорловую колбу емкостью 50 мл, снабженную мешалкой, обратным холодильником и термометром, помещаем 20.0 мл моногидрата и нагреваем...
-
Общая методика. В круглодонной трехгорлой колбе емкостью 100 мл растворяли 11,9 г бензотриазола (2-аминопиридина) в 20 мл толуола. Колбу соединяли с...
-
Синтез бромэтана проводили в соответствии с методикой, изложенной в источнике [2]. ХОД РАБОТЫ - Приготовление исходных реактивов и собирание прибора Рис....
-
Процесс окислительного декарбоксилирования состоит из двух основных стадий: окисления углеводорода до арилкарбоновой кислоты и собственно окислительного...
-
Получение фенола прямым каталитическим гидроксилированием бензола - Синтез фенола
Предложен способ получения фенола прямым каталитическим гидроксилированием бензола. Реакция прямого введения гидроксильной группы в бензольное ядро...
-
Висновок - Загальна характеристика, номенклатура та ізомерія оксигеновмісних органічних сполук
До оксигеновмісних органічних сполук належать такі класи сполук, як спирти, феноли, альдегіди і кетони. Я ознайомилась із загальною будовою молекул...
-
ОСНОВНЫЕ СВОЙСТВА ФЕРМЕНТОВ - Аминокислоты и ферменты
К ферментам применимы три основных критерия, характерных и для неорганических катализаторов. В частности, они остаются неизмененными после реакции, т. е....
-
Упрочнение химических связей, соединяющих основные звенья углеродной цепи, под действием акрилонитрильных группы - СН2--СН атомов фтора приводит к...
-
Газообразные продукты (NH3, HCI, CI2, SO2, HCN), растворимые в воде, поглощаются носовой полостью. Нерастворимые в воде (СО) продукты проникают в легкие,...
-
Координаційні сполуки дигідразиду 2,6-диметил-3,5-піридиндикарбонової кислоти з солями перехідних металів Серед піридинкарбонових кислот найбільш...
-
Властивості міді - Властивості міді
Мідь - блискучий метал, який має червунувате забарвлення. Мідь, як і її аналоги срібло і золото, відносно малоактивні. Однак, на відміну від срібла і...
-
Обзор литературы - Синтез пара-нитродифенила. Теоретические основы нитрования
Нитрование - введение нитрогруппы - NO2 в молекулы органических соединений. Может проходить по электрофильному, нуклеофильному и радикальному механизмам;...
-
Окисление глицерина, Синтез жирных кислот - Обмен и функции липидов
На первом этапе глицерин активируется в глицерофосфат, затем окисляется до фосфодигидроксиацетона, который через стадию образования пирувата переходит в...
-
Представление о механизме окислительного декарбоксилирования арилкарбоновых кислот - Синтез фенола
Окислительное декарбоксилирование арилкарбоновых кислот проводится при 200--300°С в присутствии солей двухвалентной меди при подаче в реактор воздуха и...
-
Щелочное плавление сульфокислот - Синтез фенола
При щелочном плавлении сульфокислот замещение сульфогруппы на оксигруппу считают результатом сложного процесса, предполагающего промежуточное...
-
Важнейшей характеристикой раствора является его состав. Содержание растворенного вещества в растворе может быть выражено безразмерными единицами (долями...
-
Разбавленные Растворы неэлектролитов (веществ, растворы или расплавы которых не проводят электрический ток) обладают рядом свойств, количественное...
-
Экспериментальная часть - Синтез пара-нитродифенила. Теоретические основы нитрования
A. Реагенты и оборудование Для проведения синтеза использовались следующие реагенты: Дифенил C12H10 Молекулярная масса: 154.2 Температура кипения: 256°C...
-
Процесс нитрования углеводородов смесью азотной и серной кислот протекает в гетерогенной среде, так как образуются две фазы - органическая...
-
Визначення чистоти продуктів і контроль за реакціями здійснювались методом ТШХ на пластинах "Silufol UV-254", елюент бензол-етилацетат-етанол, 1:1:1,...
-
Или N экв.1=n экв.2 для газообразных ве-в наряду с понятием молярного V (22,4 моль/л), исп-ся понятие - молярный объем эквивалента-это V одного моль...
-
В последнее десятилетие в нашей стране очень сильно возросло потребление парфюмерно-косметических товаров. На российском рынке постоянно появляются новые...
-
Контрольные вопросы - Химико-токсикологический анализ органов трупа
ВАРИАНТ№1 1. Характеристика токсикологической группы веществ "летучие яды". Особенности различных видов отравлений. Летучие органически соединения...
-
Выбор метода получения 1 способ Готовят отдельно два раствора: 9 г хлорида кобальта (II) в 25 мл воды (раствор 1) , 10 г хлорида аммония и 14 г нитрата...
-
Жири і олії, які містять радикали ненасичених жирних кислот, окиснюються киснем повітря. Реакція окиснення може відбуватися під дією фермента...
-
Фенолфталеин - один из наиболее широко используемых индикаторов, особенно при объемном определении слабых кислот. Он обладает рядом преимуществ: не...
-
Кислород: история открытия и основные свойства
Кислород - элемент главной подгруппы шестой группы, второго периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 8....
-
В связи с тем, что для синтеза целевых фталоцианинов, аннелированные гетероциклическими хинонами мы выбрали метод темплатного синтеза, то первым шагом...
-
Эфиры карбоновых кислот очень редко получают из хлорангидридов, так как последние являются дорогостоящими веществами. В отличие от этого эфиры угольной...
-
Вихідними продуктами для виробництва полівінілхлориду є рідкий вінілхлорид і вода. Вінілхлорид (CH2 = CHCl) - білі пластинки, легкорозчинні у воді....
Сульфування - Хімія та технологія основного органічного і нафтохімічного синтезу