Способи добування, Фізичні та хімічні властивості - Загальна характеристика, номенклатура та ізомерія оксигеновмісних органічних сполук

1. Окиснення спиртів. Первинні спирти окиснюються до альдегідів, а вторинні - до кетонів.
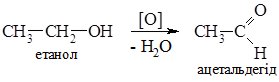
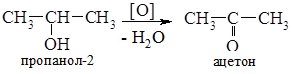
- 3. Гідратація алкінів (реакція Кучерова). З ацетилену в умовах реакції утворюється ацетальдегід, всі інші алкіни дають кетони: 4.
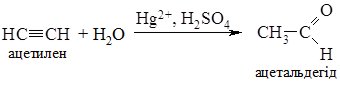
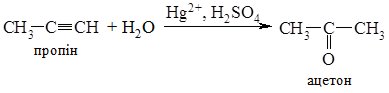
Гідратацією ацетилену в промисловості одержують оцтовий альдегід, а з нього відновленням - етиловий спирт; окисненням - оцтову кислоту.
3. Гідроліз дигалогеналканів. При гідролізі дигалогеналканів з атомами галогену біля первинного атома Карбону утворюються альдегіди, а біля вторинного - кетони. Особливо легко гідроліз відбувається в лужному середовищі:
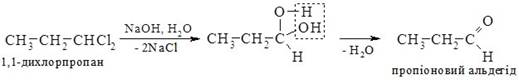
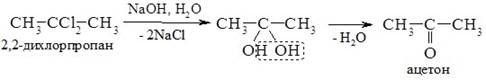
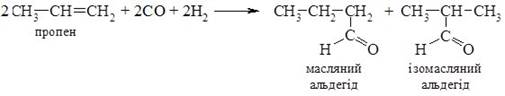
4. Оксосинтез. В промисловості альдегіди одержують взаємодією алкенів з карбон (ІІ) оксидом, воднем при підвищених температурі та тиску в присутності платинового або кобальтового каталізаторів. Зазвичай утворюється суміш ізомерів: спирт фенол альдегід оксиген
Фізичні та хімічні властивості
Мурашиний альдегід - газ, нижчі альдегіди і кетони - леткі рідини. Альдегіди і кетони добре розчиняються в органічних розчинниках, нижчі - розчинні у воді. Більшість альдегідів і кетонів мають характерний запах. Альдегіди, що містять 8 - 12 атомів Карбону - пахучі речовини, їх використовують у парфумерії.
Хімічні властивості альдегідів та кетонів визначаються наявністю в їх складі карбонільної групи.
Атоми Карбону та Оксигену в карбонільній групі перебувають у стані Sp2_гібридизації і зв'язані подвійним зв'язком, який складається з s - та p_зв'язків. Атом Оксигену, як більш електронегативний, зміщує на себе електронну густину подвійного зв'язку. Внаслідок цього на атомі Карбону утворюється частковий позитивний (д+), а на атомі Оксигену частковий негативний заряд (д-):
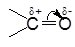
Завдяки такій поляризації карбонільної групи, альдегіди і кетони є високореакційноздатними сполуками і вступають у реакції приєднання з реагентами, що мають неподілену пару електронів, або молекули яких містять атом з підвищеною електронною густиною або атом з негативним зарядом. Реакція починається з атаки атома Карбону карбонільної групи. Тому реакційна здатність карбонільних сполук в реакціях приєднання визначається величиною часткового позитивного заряду (д+) на атомі карбону С=О-групи: чим він більший, тим вища їх реакційна здатність.
Альдегіди, як правило, більш реакційноздатні, ніж кетони. Алкільні радикали за рахунок +І-ефекту зміщують електронну густину у бік С=О-групи, зменшуючи позитивний заряд на атомі Карбону карбонільної групи. Наявність в молекулі кетону двох алкільних груп біля карбонільної групи, веде до більшого зниження величини позитивного заряду, ніж в молекулі альдегіду.
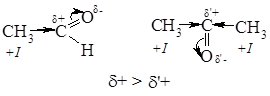
Всі реакції альдегідів та кетонів можна умовно поділити на групи:
- - реакції приєднання; - реакції окиснення і відновлення; - реакції полімеризації.
Реакції приєднання.
- 1. Приєднання синильної кислоти відбувається по карбонільній групі альдегідів або кетонів з утворення ціангідринів (гідроксинітрилів). 2.
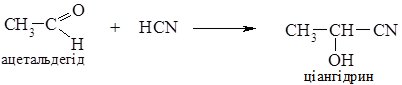
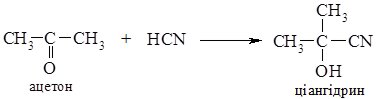
Реакція прискорюється в присутності основи; утворені ціангідрини використовують в синтезі гідрокси - та амінокислот.
2. Приєднання натрій гідроген сульфіту до альдегідів і найпростіших кетонів веде до утворення "бісульфітних сполук". Реакція проходить без каталізатора.
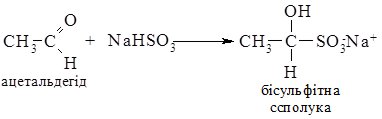
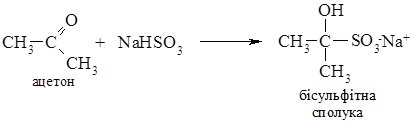
Бісульфітні сполуки погано розчинні у воді, тому ця реакція є якісною на карбонільну групу, також її використовують для виділення і очищення альдегідів і кетонів.
3. При взаємодії з амоніаком альдегіди утворюють альдіміни.
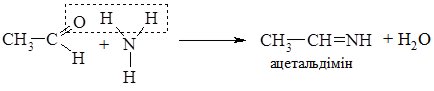
Альдіміни - нестійкі сполуки, вони самовільно полімеризуються (циклізуються). Три молекули ацетальдіміну самовільно циклізуються з утворенням альдегідаміаку:
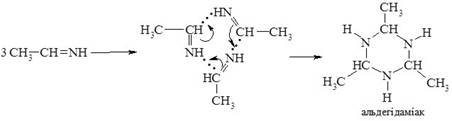
4. При взаємодії карбонільних сполук з гідроксиламіном (NH2OH) утворюються оксими, у випадку альдегідів - альдоксими, кетонів - кетоксими.
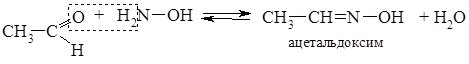
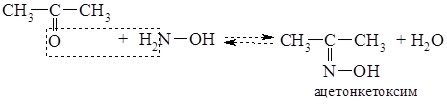
Альдоксими і кетоксими - тверді кристалічні речовини з чіткими температурами плавленнями, реакцію їх утворення використовують для виділення та ідентифікації альдегідів і кетонів.
Реакції відновлення та окиснення.
1. Реакції відновлення Альдегідів та кетонів широко застосовують для одержання спиртів (альдегіди відновлюються до первинних, а кетони - до вторинних спиртів). У промисловості проводять гідрування карбонільних сполук у присутності каталітичних кількостей кобальту, нікелю або платини:
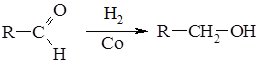
2. Окиснення Альдегідів та кетонів відбувається по-різному. Альдегіди дуже легко окиснються, навіть при дії слабких окисників (Ag+, Cu+), вони перетворюються в карбонові кислоти:
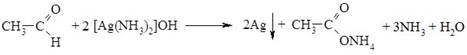
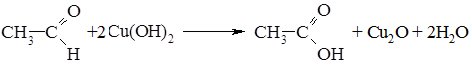
Реакцію окиснення альдегідів амоніачним розчином аргентум (І) оксиду називають реакцією "срібного дзеркала". Іон Аргентуму в цій реакції відновлюється до вільного металу, яке виділяється у вигляді дзеркала на стінках пробірки.
Окиснення кетонів відбувається лише сильними окисниками - калій перманганатом або дихроматом, реакція супроводжується розривом зв'язків С_С у молекулі кетону.
Реакції полімеризації.
Альдегіди, на відміну від кетонів здатні полімеризуватись. Процес проходить за звичайних умов і прискорюється кислотами. Полімеризація формальдегіду проходить з утворенням полімеру лінійної структури:
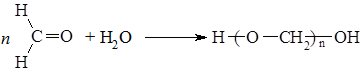
Полімеризація ацетальдегіду за наявності слідів сульфатної кислоти веде до утворення циклічного продукту - тримеру - паральдегіду:
Похожие статьи
-
Альдегіди і кетони - похідні вуглеводнів, що містять в своєму складі карбонільну групу (>С=О). Тому їх ще називають карбонільними сполуками. Назву...
-
Реакції, в які вступають спирти, супроводжуються розривом зв'язків О-Н або С-О. 1. Кислотні властивості спиртів. Утворення алкоголятів. Спирти не...
-
Феноли - безбарвні кристалічні речовини або рідини з характерним запахом. Як правило, вони погано розчинні у воді; при зберіганні на повітрі окиснюються...
-
1. Гідроліз галогенопохідних. При обробці галагенопохідних водним розчином лугу, іде заміщення галогену на гідроксил. СН3СН2Br + NaOH > СН3СН2OH +...
-
Гідроксильні похідні ароматичних вуглеводнів, у яких гідроксильна група безпосередньо зв'язана з бензольним ядром. Сполуки, що містять гідроксил в...
-
Загальна формула одноатомних спиртів R-OH. Залежно від того, з яким атомом Карбону (первинним, вторинним чи третинним) зв'язана гідроксильна група,...
-
Фенол (гідроксибензен, карболова кислота - лат. Carbo, carbonis - вугілля та лат. Oleum - олія) С6Н5ОН. Безбарвна кристалічна речовина зі специфічним...
-
Спирти, молекули яких містять декілька гідроксильних груп відносять до Багатоатомних спиртів . Спирти, які містять дві гідроксильні групи біля одного...
-
Вступ - Загальна характеристика, номенклатура та ізомерія оксигеновмісних органічних сполук
Всі органічні речовини передусім складаються з атомів карбону і гідрогену. Але, поряд з тим, відомо багато речевин містить також атоми оксигену. Із...
-
Горіння простих і складних речовин: А) С + О2 СО2 2Сu + O2 = 2CuO (окислення, крім благородних металів) Б) СН4 + 2О2 СО2 + 2Н2О 2. Розклад під час...
-
Фізичні та хімічні властивості - Натрій: історія, властивості
Фізичні властивості. Оскільки в атомах лужних металів один зовнішній електрон доводиться на 4 і більше вільні орбіталі, а енергія іонізації атомів...
-
СПГ зберігається в спеціальних кріоцістернах, влаштованих за принципом посудини Дюара. Транспортується СПГ на спеціалізованих морських суднах - танкерах,...
-
Альдегіди Ми знаємо, що спирти легко окиснюються. При їх повному окисненні (горінні) утворюються оксид вуглецю (IV) і вода. Під впливом різних окисників...
-
Вступ - Типові неметали - галогени, їх характеристика, властивості і сполуки
До головної підгрупи VII групи періодичної системи елементів Д. І. Менделєєва входять: Фтор F, Хлор Cl, Бром Br, Йод J та Астат At. Загальна назва цієї...
-
Фізичні властивості, ХІМІЧНІ ВЛАСТИВОСТІ - Амінокислоти: одержання, властивості, роль у біології
Амінокислоти-безбарвні кристалічні речовини з високими температурами плавлення, які мало відрізняються для цих кислот і тому не характерні. Плавлення...
-
ЙОД Сировиною для промислового одержання йоду служать нафтові бурові води, морські водорості, а також маткові розчини чилійської (натрієвої) селітри, що...
-
ЙОД ЙОД - І хімічний елемент VII групи періодичної системи Менделєєва, належить до галогенів (у літературі зустрічається також символ J); атомний номер...
-
ХІМІЧНІ ВЛАСТИВОСТІ КИСНЮ І СІРКИ - Неметали та їхні сполуки
Ви вже знаєте, що кисень - дуже реакційноздатна речовина. Він реагує з багатьма металами, неметалами багатьма складними речовинами, виявляючи властивості...
-
ЗАГАЛЬНА ХАРАКТЕРИСТИКА ОКСИГЕНУ І СУЛЬФУРУ - Неметали та їхні сполуки
Історичні відомості. Про історію відкриття кисню, молекули якого складаються з елемента Оксигену, ви довідалися ще у 8 класі. Тепер ознайомтеся з деякими...
-
ХІМІЧНІ ВЛАСТИВОСТІ КИСНЮ І СІРКИ - Загальні відомості про елементи
Ви вже знаєте, що кисень -- дуже реакційноздатна речовина. Він реагує з багатьма металами, неметалами багатьма складними речовинами, виявляючи...
-
ЗАГАЛЬНА ХАРАКТЕРИСТИКА ОКСИГЕНУ І СУЛЬФУРУ - Загальні відомості про елементи
Історичні відомості. Про історію відкриття кисню, молекули якого складаються з елемента Оксигену, ви довідалися ще у 8 класі. Тепер ознайомтеся з деякими...
-
Каталітичний крекінг - Алкани як паливо. Октанове та цетанове число
Значно вищі октанові числа бензинів, які одержують в процесі каталітичного крекінгу (у порівнянні з термічним крекінгом), пояснюється головним чином...
-
Оксиди, їх класифікація. Номенклатура - Оксиди, загальна характеристика
Оксидами називаються складні речовини, до яких входять два елементи, один з яких оксиген. Майже всі хімічні елементи утворюють оксиди. І досі ще не...
-
АМІНОКИСЛОТИ, ІЗОМЕРІЯ. НОМЕНКЛАТУРА - Амінокислоти: одержання, властивості, роль у біології
Органічні сполуки, що містять в молекулі карбоксильну та аміно групи, називають - амінокислотами. Амінокислоти мають надзвичайно велике значення в...
-
Каталітичний крекінг - Алкани як паливо
Значно вищі октанові числа бензинів, які одержують в процесі каталітичного крекінгу (у порівнянні з термічним крекінгом), пояснюється головним чином...
-
Загальні властивості функцій - Функції та способи їх задання
Означення : Множина всіх значень аргумента, для яких можна обчислити значення функції, називається природною областю визначення функції. Область...
-
Номенклатура спиртов - Химические свойства и характеристики спиртов
Для распространенных спиртов, имеющих простое строение, используют упрощенную номенклатуру: название органической группы преобразуют в прилагательное (с...
-
Понятие и классификация спиртов СПИРТЫ (алкоголи) - класс органических соединений, содержащих одну или несколько группировок С-ОН, при этом гидроксильная...
-
Фізичні і механічні властивості титану - Титан та його властивості
Титан дуже тугоплавкий метал. Довгий час вважався, що він плавиться при 1800° С, однак у середині 50-х рр. англійські вчені Діардорф і Хейс установили...
-
Фізичні властивості. - Виробництво і застосування платини
Платина дуже тугоплавкий метал, кристалізується в гранецентровані кубічні (р. ц. до.) грати. При дії на розчини солей відновниками метал може бути...
-
Реакція термічного алкілування пропану етиленом - Алкани як паливо
Представляє скоріше теоретичний, ніж практичний інтерес. З цієї реакції витікає, що атоми водню метиленової групи більш реакційноздатні, ніж атоми водню...
-
ШЛЯХИ ОТРИМАННЯ АМІНОКИСЛОТ - Амінокислоти: одержання, властивості, роль у біології
Розроблено багато шляхів отримання - амінокислот. Найважливіші з них три: 1. Дія аміаку на солі хлорзамісних кислот:...
-
Ряди розподілу вибіркової сукупності. Характеристика центру розподілу При статистичному групуванні даних кожну групу характеризують системою показників...
-
Применение спиртов - Химические свойства и характеристики спиртов
Способность спиртов участвовать в разнообразных химических реакциях позволяет их использовать для получения всевозможных органических соединений:...
-
Визначення : Скалярний добуток двох векторів і дорівнює добутку модулів цих векторів на косинус кута між ними . (6.1) Таким чином, скалярний добуток двох...
-
Властивості титану - Титан та його властивості
У періодичній системі елементів Менделєєва титан має порядковий номер 22. Атомна маса природного титану, обчислена за результатами досліджень його...
-
Скорость перемещения заряда в приповерхностной области полупроводника гетероструктуры, являющейся зоной перемещения сигнальных зарядовых пакетов...
-
Об'єктом дослідження послужив сучасний осад мінералізований відібраний в літній час по глибині мулової колонки в інтервалі 50-100 см (мінералізація води...
-
ТЕОРЕТИЧНА ЧАСТИНА, Характеристика досліджуваного об'єкту - Питні мінеральні води
Титрування кальцій магній мінеральний Характеристика досліджуваного об'єкту Питні мінеральні води - як правило підземні води, що характеризуються...
-
А) Углерод (С), кремний (Si), германий (Ge), олово (Sn), свинец (РЬ) - элементы 4 группы главной подгруппы ПСЭ. На внешнем электронном слое атомы этих...
Способи добування, Фізичні та хімічні властивості - Загальна характеристика, номенклатура та ізомерія оксигеновмісних органічних сполук