Щелочное плавление сульфокислот - Синтез фенола
При щелочном плавлении сульфокислот замещение сульфогруппы на оксигруппу считают результатом сложного процесса, предполагающего промежуточное присоединение щелочи по кратной связи:


Кроме этого основного процесса возможно также прохождение и других, ведущих к образованию побочных продуктов, в частности протекает расщепление сульфонов с образованием фенолятов и частично дифенола:

Возможно взаимодействие сульфокислот и фенолятов с образованием дифениловых эфиров:
Наконец, возможно окисление компонентов сплава под действием кислорода воздуха с образованием диоксидифенилов, оксидифенилов и их гомологов.

При щелочном плавлении сульфокислот гомологов бензола и нафталина происходит также окисление метильных групп с образованием спиртовых и карбоксильных групп и далее, вплоть до отщепления карбоксильных групп:
Так, пpи щелочном плавлении толуолсульфокислоты образуется заметное количество фенола (от 1--1,5% при исключении контактов плава с воздухом до 15-20% -- в случае интенсивного перемешивания плава). При щелочном плавлении сульфокислот ксилолов при температурах выше 350оС количество фенола и крезолов в плаве может достигать 15-25% от общего количества фенолов. По литературным данным, при использовании над плавом подушки из инертного газа и времени контакта 1,5 ч выход крезолов составляет 92%, тогда как в отсутствие инертного газа только 60 70%.

Для уменьшения потерь фенолов при окислении плава применяются различные способы изоляции плава от атмосферы -- чаще всего за счет применения подушки из перегретого водяного пара или инертных газов. Однако даже при изоляции от воздуха в плаве возможно прохождение -- тем более при высоких температурах -- окислительно-восстановительных процессов, например:
Приводящих к образованию оксидифенилов и тиофенолятов. Правда, глубина их не очень велика, однако они приводят не только к увеличению количества примесей вообще, но и к появлению трудноотделимых от фенолов тиофенолов.
На выход фенолов и развитие побочных процессов серьезное влияние оказывают примеси солей. По данным Беркмана, присутствие 2% хлорида натрия в плаве уменьшает выход фенола при плавлении на 3- 4%, присутствие 0,5% солей железа сокращает выход фенола на 3--4%. Последнее объясняется окислительным действием ионов железа при высоких температурах.
Сульфат натрия в количестве до 10% незначительно влияет на процесс щелочного плавления. Это позволяет не выделять из сульфонатов серную кислоту при небольшом (до 5-6%) ее содержании.

Па процесс щелочного плавления определенное влияние оказывает вид применяемой щелочи. Так, в промышленности чаще используют более дешевый и доступный едкий натр. В лабораторных условиях чаще применяют едкое кали, в котором лучше растворяются соли сульфокислот. Это обстоятельство имеет особое значение для щелочного плавления сульфокислот гомологов бензола, соли которых в щелочи растворяются значительно хуже, чем соли бензолсульфокислоты. В связи с этим было предложено брать для проведения плавления смесь щелочей, содержащую не менее 28% едкого кали, или плавить толуол сульфонат в присутствии бензолсульфоната.
Рис 2.2. Принципиальная технологическая схема щелочного плавления арилсульфонатов (непрерывная схема с каскадом плавильников)
Аппараты: 1 - обогреваемые плавильники; 2-- аппарат для разбавления ("гашения") плава; 3 - фильтр для выделения сульфита натрия; 4 -- скруббер для выделения фенолов из фенолятов; 5 - отстойник.
Потоки: I - арилсульфонат натрия, II -- едкий натp; III - водяной паp; IV - продукты щелочного плавления; V - вода; VI - отбросные газы и пары; VII - paствop фенолятов в смеси с кристаллами сульфита натрия; IX - раствор фенолятов натрия; Х -- двуокись серы; XI - фенолы; XII - сульфитный щелок.
Плохая растворимость солей толуолсульфокислот делает особо важным использование избытка щелочи. При небольшом избытке щелочи образуется темный вязкий плав, имеющий консистенцию мокрого песка, что увеличивает опасность пригорания и окисления плава. При большем избытке щелочи образуется светлый, подвижный плав, легко перемешивающийся якорной мешалкой.
Увеличение мольного отношения щелочь сульфокислота с 2,5 до 4 - 5 увеличивает выход крезола с 50--60 до 70 - 80%, считая на исходную соль. Однако при оптимальных температурах и при минимальном избытке щелочи (мольное соотношение щелочь - сульфонат 2,5) также возможно достижение выходов крезола порядка 84--92%.
Данные о влиянии температуры на выход крезолов противоречивы. По данным Энгланда, оптимальная температура составляет 340--360°С. Опыты показывают, что при этой температуре происходит значительное осмоление плава, а выход фенола увеличивается до 5%, считая на крезол. Максимальный выход достигается при температуре 320°С.
Выход фенолов при щелочном плавлении зависит также и от избытка щелочи, что иллюстрирует рис. 429. Увеличение времени пребывания фенолята н сульфоната в зоне высоких температур усиливает образование побочных продуктов. Существование оптимальных соотношений температур и времени пребывания в зоне нагрева подтверждается данными о щелочном плавлении сульфонатов ксилолов:
Таблица 2.1. Щелочное плавление солей сульфокислот м-ксилола (мольное соотношение щелочь; соль равно 3)
|
Условия плавки |
Состав фенолов, % |
Выход 2 ,4- ксиленола, считая на исходную соль, % | |||
|
Температура, оС |
Время, Ч |
Фенол |
Крезолы |
2,4-ксиленол | |
|
320 |
1,0 |
6,13 |
2,55 |
90,40 |
58,53 |
|
" |
1,5 |
2,00 |
4,3 |
92,5 |
78,25 |
|
" |
2,0 |
4,65 |
5,08 |
85,6 |
69,85 |
|
330 |
1,5 |
6,05 |
2,3 |
92,5 |
57,45 |
|
340 |
0,5 |
1,60 |
1,74 |
96,0 |
11,22 |
|
" |
1,0 |
4,88 |
1.95 |
92,5 |
15,66 |
|
" |
1,5 |
5,05 |
4,90 |
90,0 |
40,25 |
|
350 |
1,5 |
2,3 |
12,16 |
85,7 |
23,6 |
|
1,5 I 5 |
|
78,8 16,9 |
20,4 0,75 |
Таким образом, в зависимости от условий щелочного плавления выход фенолов на этой стадии может колебаться в довольно широких пределах. В особенности это относится к щелочному плавлению дисульфокислот. Так, при щелочном плавлении соли бензол-м-дисульфокислоты по разным данным выход колеблется от 20 до 90%. Это объясняется особой легкостью окисления двухатомных фенолов и соответствующих сульфокислот, иx сравнительно малой термической устойчивостью, а также своеобразным изменением консистенции плава. До 200°С плав представляет асфальтоподобную вязкую массу. В интервале 200 - 280°С плав у большинства дисульфокислот приобретает жидкую консистенцию, при 290°С после завершения замещения одной сульфогруппы в плавильнике вновь тестообразная масса, даже иногда рассыпающаяся в порошок, после 290 - 300оС выделяется вода, образующаяся при замещении второй сульфогруппы, и масса вновь приобретает подвижность. И, наконец, при завершении отгона этой воды плав снова обращается в порошок. Все эти превращения резко меняют условия перемешивания содержимого плавильника, увеличивают опасность местных перегревов, пригорания реакционной массы, ее усиленного окисления.
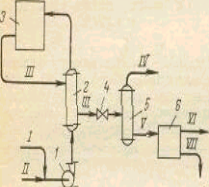
Рис. 2.3. Принципиальная технологическая схема щелочного плавления арилсульфонатов натрия в трубчатом реакторе
Аппараты: 1 - насос; 2 - теплообменник; 3 - трубчатый реактор; 4 - дроссельный вентиль; 5 - испаритель; 6 - фильтр для выделения сульфата натрия.
Потоки: I - раствор арилсульфоната натрия; II - раствор едкого натpa; III - раствор продуктов щелочного плавления; IV - водяной пар; V - раствор фенолятов в смеси с кристаллами сульфита натрия; VI - сульфит натрия; VII - pacтвоp фенолятов натрия на нейтрализацию.
Какие возможны пути сокращения опасности перегревов? Один из них -- увеличение избытка щелочи. Главный недостаток этого приема увеличение себестоимости целевого продукта. Другой путь -- плавление водных растворов сульфоната и щелочи. Смешение водных растворов большой концентрации способ, широко практикуемый. При этом часто первый этап щеточного плавления обращается в выпарку на неприспособленном оборудовании и лишь несколько упрощается приготовление смеси, используемой для плавления. Правда, небольшое количество воды остается в плаве и снижает температуру плавления компонентов, уменьшает вязкость плава. Более эффективной может быть переработка 15-30%-ных водных растворов щелочей и сульфонатов при 360-380°С под давлением. При этом вода не испаряется, реакционная масса обладает высокой подвижностью, система полностью герметизована и исключается внешнее окисление.
Необходимость работы при давлении около 200 кгс/см2 не вызывает особых затруднений, так как используются трубчатые реакторы (рис. 2.3.). Схема становится компактной, полностью непрерывной, легко управляемой. Применение змеевика обеспечивает большую скорость потока и исключает местные перегревы. Выход фенола может быть доведен до 98%.
По-видимому, это наиболее перспективный путь непрерывного оформления процесса. Частным вариантом этой схемы является термическое разложение сульфонатов в смеси с расплавом фенолятов.
Похожие статьи
-
Получение фенолов щелочным плавлением сульфокислот - Синтез фенола
Щелочное плавление сульфокислот ароматических углеводородов -- один из старейших способов приготовления фенолов. Он и сейчас вызывает определенный...
-
Выделение фенолов из фракций смол коксования и полукоксования твердых топлив Выделение фенолов из фракций смол необходимо не только из-за ценности, но и,...
-
Важнейшие способы синтеза фенолов - Синтез фенола
При использовании в качестве сырья углеводородов ароматического ряда синтез фенолов можно представить в общем, виде как окисление углеводородов. Прямое...
-
Определение температуры плавления Температуру плавления определяем с помощью малогабаритного нагревательного стола типа "Boetinus" с наблюдательным...
-
Реактивы: Фенол (техн.), формалин (техн.), аммиак (30%-й раствор). Оборудование: Колба круглодонная емкостью 100 см3, холодильник Либиха, пипетка на 1...
-
Процесс плавления дисперсии - Синтез полиуретанов
Проблемы, связанные с аминным расширением цепи удается избежать в этом процессе. NCO-концевые полиуретановые преполимеры подвергают взаимодействию с...
-
Получение фенолов из отходов переработки нефти - Синтез фенола
Отходы переработки нефти могут явиться источником крезолов и ксиленолов. Ресурсы фенолов в нефти невелики и составляют сотые и даже тысячные доли...
-
Введение, Классификация Фенолов, Физические свойства фенола, Химические свойства - Синтез фенола
Фенол химический синтез Целью данной курсовой работы является изучение способов синтеза фенолов, в частности фенола. Свойства фенолов специфичны, поэтому...
-
Методы, применяющиеся для синтеза мультиферроиков - Мультиферроики
Для синтеза мультиферроиков используются различные методы синтеза. К ним относятся: спекание, гидротермальный синтез, соосаждение, золь-гель метод,...
-
Образование фенолятов, Реакции ароматического ядра фенолов - Спирты и фенолы
Образование простых эфиров фенолов алкилированием фенолятов: ArONa + RI > ArOR + NaI ArONa + (CH3O)2SO2 > ArOCH3 + CH3O-SO2ONa Образование...
-
Синтез фуллеренов - История открытия фуллеренов, их свойства
Первые фуллерены выделяли из конденсированных паров графита, получаемых при лазерном облучении твердых графитовых образцов. Фактически, это были следы...
-
NаСl + NН4НСО3 NаНСО3 + NН4Сl Равновесие которой почти нацело смещено вправо (вследствии очень малой растворимости NаНСО3 в растворе NН4Сl)....
-
Эфиры карбоновых кислот очень редко получают из хлорангидридов, так как последние являются дорогостоящими веществами. В отличие от этого эфиры угольной...
-
Физические свойства Очень чистый Na2O2 бесцветен, обычно полученный продукт чуть желтоватого цвета. Tпл = 6750 c (разлагается). Гексагональная...
-
Фенол - Разработка технологической схемы получения анизола и крезола
Фено?л (оксибензол, устар. карболовая кислота) C6H5OH -- бесцветные игольчатые кристаллы, розовеющие на воздухе из-за окисления, приводящего к...
-
Введение, Методы - Синтез оксида свинца
Целью моей курсовой работы является выполнение синтеза предложенного вещества. В данном случае - оксида свинца (IV) - PbO2. Далее будут рассмотрены...
-
Температура плавления и плотность металлов и сплавов - Структура и свойства металлических расплавов
От температуры плавления металла зависит способ его плавки, материал футеровки плавильной печи или тигля и линейной формы. Температура плавления и...
-
Итак, изомерные диоксибензолы носят следующие названия: о-диоксибензол - пирокатехин, м-изомер - резорцин и п-изомер - гидрохинон. Это хорошо растворимые...
-
Общая методика. В трехгорловую колбу емкостью 50 мл, снабженную мешалкой, обратным холодильником и термометром, помещаем 20.0 мл моногидрата и нагреваем...
-
Таблица 2 - Структура сырья в производстве метанола, %. Сырье В мире Беларусь и Россия Природный газ 73,8 70,7 Нефть и нефтепродукты 24,4 4,0 Отходы...
-
Химизм реакции фенола с альдегидами Фенолы реагируют с альдегидами в кислой или щелочной среде, при этом образуются смолообразные олигомеры и вода....
-
Процесс приготовления, Ацетон процесс - Синтез полиуретанов
Самый ранний способ получения водной дисперсии полиуретана был ацетон процесс, который по-прежнему остается технически важным [10]. В последние пару...
-
Способы получения насыщенных растворов - Синтез ацетата натрия ("Горячий лед")
Простейший способ приготовления насыщенных растворов - длительное настаивание растворителя с избытком растворяемого вещества, лучше всего при...
-
Химические свойства спиртов - Спирты и фенолы
Ряд химических свойств спиртов является общим для всех спиртов; имеются также и реакции, по-разному протекающие для первичных, вторичных и третичных...
-
Применение H2O2 связано с его окислительными свойствами и безвредностью продукта его восстановления (H2O). Его использую для отбеливания тканей и мехов,...
-
Понятие кристаллизации Кристаллизамция -- процесс фазового перехода вещества из жидкого состояния в твердое кристаллическое с образованием кристаллов....
-
Бромистый этил представляет бесцветную прозрачную жидкость, обладающую эфирным запахом и сначала сладким, потом жгучим вкусом. Кипит при 38,4°С. В воде...
-
Процесс нитрования углеводородов смесью азотной и серной кислот протекает в гетерогенной среде, так как образуются две фазы - органическая...
-
Методы неорганического синтеза - Синтез ацетата натрия ("Горячий лед")
НЕОРГАНИЧЕСКИЙ СИНТЕЗ, получение неорганических соединений. Как правило, состоит из нескольких последовательных или параллельных процессов -...
-
Синтез бромэтана проводили в соответствии с методикой, изложенной в источнике [2]. ХОД РАБОТЫ - Приготовление исходных реактивов и собирание прибора Рис....
-
Для получения модифицированной квантовой точки (гибридного соединения) были использованы квантовые точки CdS (КТ, QD) с диаметром 2,5 нм и...
-
Кинетика процесса нитрования - Синтез пара-нитродифенила. Теоретические основы нитрования
Нитрование ароматических углеводородов смесями азотной и серной кислот протекает по ионному механизму. В. В. Марковников указал, что при взаимодействии...
-
Целью данной курсовой работы является проведение синтеза ацетата натрия (CH3COONa). Задачами курсовой работы являются: изучение методики неорганического...
-
К числу физических факторов, вызывающих коррозию цементного камня и бетона, относят их попеременное увлажнение и высыхание, которое сопровождается...
-
Экспериментальная часть - Синтез пара-нитродифенила. Теоретические основы нитрования
A. Реагенты и оборудование Для проведения синтеза использовались следующие реагенты: Дифенил C12H10 Молекулярная масса: 154.2 Температура кипения: 256°C...
-
Использование предшественников при производстве аминокислот позволяет успешно обходить метаболический контроль, осуществляющийся по механизму обратной...
-
Электронные спектры поглощения соединений (9а, б, 10а, б, 12а, б, 13а, б 15а, б и 16а, б) в концентрированной серной кислоте характеризуются наличием...
-
Органические кислоты в различных условиях могут разлагаться с образованием предельного углеводорода по общей схеме O R-C RH + CO2 Кислота OH Углеводород...
-
Синтез гетероциклических соединений Синтез 4-амино-1,2-бензотиазола К раствору 5-8 г (31 ммоль) 2,6-диметилтолуола в 15 мл мезителена (температура...
-
Синтез в живых системах - Простагландины. Строение. Биороль
Простагландины не накапливаются в тканях, а синтезируются в ответ на биологический стимул из полиненасыщенных жирных кислот: простагландины с одной...
Щелочное плавление сульфокислот - Синтез фенола