Контрольная работа 2, Аналитическая часть., Практическое задание. - Математическая модель кинетики процесса
Аналитическая часть.
Какие законы физики и химии используются при разработке ММ кинетики химических реакций?
Ответ:
Для вывода уравнения скорости химической реакции используется закон действующих масс (основной постулат химической кинетики).
Закон Аррениуса-Обоснование зависимости скорости реакции от температуры было получено С. Аррениусом. Им была сформулирована теория активных столкновений между молекулами: всякая реакция протекает через промежуточную стадию, связанную с переходом состояния молекул от нормальной (средней) энергии к состоянию с повышенной энергией.
Практическое задание.
Построение динамической ММ на основании заданного механизма и кинетических констант в среде MathCad и исследование в соответствии с заданным вариантом задания. Необходимо привести матрицы стехиометрических коэффициентов, матрицы частных порядков реакций по компонентам, уравнения скоростей реакций, систему дифференциальных уравнений. Проведите вычислительный эксперимент. Получите таблицы и графики изменения концентраций компонентов. На основании полученных результатов сделайте вывод о влиянии варьируемых параметров на выходные характеристики.
В периодическом реакторе идеального смешения происходит получение водорода из исходных реагентов метан/водяной пар по следующему механизму:
СН4 +2H2О>К1 >СО2 +4Н2
СО2 +4Н2>К2 > СН4 +2H2О
Разработать математическую модель кинетики процесса и получить решение при следующих условиях:
- - интервал времени ф = 100 мин; шаг по времени Дt = 1 мин; - начальные концентрации ССН4 = 1,0 моль/л; СH2O = 1,0 моль/л; - предэкспоненциальные множители: К01 =2-105; К02 =3-106; - энергия активации Е1 = 124100 Дж/моль, Е2 = 180000 Дж/моль; - температура Т = 1100 K.
Частные порядки по компонентам во всех реакциях равны единице. Оценить влияние на выход целевого компонента:
- - изменения концентрации метана от 1 до 5 моль/л; - изменения температуры реакции от Т = 900 К до Т = 1400 К.
Определить время пребывания фопт, обеспечивающее максимально возможный выход целевого продукта для всех вариантов исследования процесса. Рассчитать рабочий объем реактора V для производительности аппарата G =200 л/мин. V = фопт-G
Решение:
В реакторе периодического действия протекает процесс получения продукта "Н2".
Для рассматриваемого примера матрица стехиометрических коэффициентов будет иметь следующий вид:
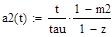









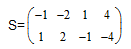
Матрица частных порядков примет следующую форму:

В соответствии с матрицами записываются уравнения для скоростей реакций:
W1=k1*CA*C2B
W2=k2*CC*C4D
Уравнения для скоростей изменения концентраций компонентов выглядят следующим образом:




DCA/dt=-w1+w2
DCB/dt=-2*w1+2*w2
DCC/dt=w1-w2
DCD/dt=4*w1-4*w2
При записи уравнений в MathCad концентрация компонента A обозначается буквой c00, компонента B - c01, компонента C - c02. Для решения системы обыкновенных дифференциальных уравнений используется встроенная функция Rkadapt (метод Рунге ? Кутты с переменным шагом), аргументами которой являются вектор-столбец начальных концентраций c00 и С01, начальное и конечное значение диапазона времени исследования (в данном случае от 0 до 100 минут), количество шагов по времени (в данном случае 100 шагов) и название решаемой системы (в данном случае она называется D).

Похожие статьи
-
(а) Зависят ли энергия активации и предэкспоненциальный множитель от природы реагентов? от их концентраций? от температуры? от присутствия посторонних...
-
Аналитическая часть., Практическое задание. - Математическая модель кинетики процесса
Какие параметры характеризуют ММ идеального смешения, идеального вытеснения, ячеечную модель, однопараметрическую диффузионную модель? Ответ: Идеальное...
-
(а) На основе уравнения ЗДМ объясните физический смысл константы скорости. (б) Зависит ли константа скорости от концентраций реагентов? от их природы? от...
-
К сожалению, многие учебники химии построены не вполне логично, в частности, одно и то же слово может использоваться в разных смыслах, поэтому...
-
Основные уравнения модели - Математическое моделирование процесса ректификации
Модель содержит следующие уравнения. Для тарелки i: (число тарелок равно N, нумерация тарелок - снизу вверх, куб считается нулевой тарелкой, дефлегматор...
-
Структура математической модели химического реактора - Химические процессы и реакторы
Математические модели высоких уровней иерархии включают в себя, как правило, несколько уравнений, как конечных, не содержащих операторов...
-
Общие понятия и определения. Термодинамический и кинетический критерий реакционной способности химической системы. Скорость химической реакции. Факторы,...
-
В 1974г. группа аргентинских ученых во главе с профессором А. Эррерой получила предварительные результаты работы над латиноамериканской моделью...
-
Пусть есть математическое ожидание цены состояния объекта при условии, что в момент времени tдопустимое экологическое состояние не достигнуто и цена...
-
Уравнение динамики теплообменника: Передаточные функции объекта получим по его уравнению динамики. Для этого запишем уравнение по заданному каналу. Затем...
-
Термодинамика - наука о взаимопревращениях различных форм энергии и законах этих превращений. Термодинамика базируется только на экспериментально...
-
Скорость гомогенных химических реакций - Химические процессы и реакторы
Скорость химической реакции W RJ принято выражать количеством (моль) N J одного из реагентов или продуктов, прореагировавшим (или образовавшимся) в...
-
Объем выпуска продукции Y зависит от количества вложенного труда x как функция . Цена продукции v, зарплата p. Другие издержки не учитываются. Найти...
-
Математическое описание аналитической модели При рассмотрении системы ПВО взаимопомощь между каналами состоит в том, что одну цель могут одновременно...
-
Решение симплекс-методом с помощью симплекс-таблиц - Математические методы и модели в экономике
Определим оптимальный план выпуска продукции, решив задачу линейного программирования (ЗЛП). Для этого сначала приведем модель к каноническому виду...
-
Подобно предыдущему обозначим. Тогда аналогичные рассуждения приводят к соотношению . (1.10) Проделывая те же преобразования, что и при выводе уравнения...
-
Методы построения решений по математическим моделям - Математическое моделирование в электромеханике
Системы дифференциальных уравнений, полученные для конкретных ти-пов электрических машин, содержат в скрытом виде исчерпывающую инфор-мацию о всех...
-
В воздушном зазоре электрических машин всегда, наряду с основной гармонической составляющей вращающегося магнитного поля, присутствуют гармонические...
-
Необходимо составить математическое описание теплообменника, в котором жидкий продукт нагревается насыщенным водяным паром (расход, кг/с), до температуры...
-
В большинстве случаев структурная неопределенность вызвана неполнотой знания аналитической структуры уравнений модели объекта управления. При не...
-
Система усовершенствованных моделей позволяет удовлетворительно воспроизводить кинетику СО-токсичности ДВС при изменении нагрузки, цикловой подачи...
-
Прежде чем рассмотреть отдельные типы химических реакторов в соответствии с приведенной классификацией, составим уравнение материального баланса по...
-
Химическое равновесие - Скорость химических процессов. Химическое равновесие, принцип Ле-Шателье
Химическое равновесие и его признаки. Равновесие истинное и заторможенное (ложное). Принцип Ле-Шателье. Константа равновесия и ее связь с...
-
Задание для исследования - Численное нахождение корня уравнения методом Рунге-Кутта
Исследовать решение обыкновенных дифференциальных уравнений методом Рунге-Кутты. Подробное описание Метод этот пригоден для решения как одиночных...
-
Реактор идеального смешения - Химические процессы и реакторы
Для модели идеального смешения принимается ряд допущений. Допускается, что в результате интенсивного перемешивания устанавливаются абсолютно одинаковые...
-
Краткая теория Основное уравнение гомогенной кинетики - закон действующих масс, ЗДМ (хотя реально подставляются не массы, а молярные концентрации):...
-
Основные понятия теории экономико-математического моделирования Кибернетический подход к исследованию экономико-математических систем Обычно...
-
КИНЕТИКА ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ - Аминокислоты и ферменты
Одним из характерных проявлений жизни является удивительная способность живых организмов кинетически регулировать химические реакции, подавляя стремление...
-
Рассмотрим случай, когда цена затрачиваемых мероприятий изменяется непрерывно со временем t. Будем предполагать, что строго монотонно убывает со временем...
-
Для трехотраслевой экономической системы заданы матрица коэффициентов Прямых материальных затрат И вектор конечной продукции Найти коэффициенты полных...
-
В основе метода площадей лежит предположение, что объект может быть описан линейным дифференциальным уравнением с постоянными коэффициентами, а его...
-
Балансовые модели - Математическое моделирование экономических процессов
Балансовые модели предназначены для анализа и планирования производства и распределения продукции на различных уровнях - от отдельного предприятия до...
-
Поскольку показательная функция относится к классу нелинейных по оцениваемым параметрам, то построению функции парной показательной регрессии X = A - B X...
-
Кинетика процесса нитрования - Синтез пара-нитродифенила. Теоретические основы нитрования
Нитрование ароматических углеводородов смесями азотной и серной кислот протекает по ионному механизму. В. В. Марковников указал, что при взаимодействии...
-
Математическое моделирование процесса запаздывания нарастания мощности автономного источника энергии от мощности потребителя Сегодня существует...
-
Прототипом разработанной автором системы моделей служит "точечная" модель [1], представляющая собой пространственно осредненный вариант уравнений горения...
-
Метод Гомори последовательных отсечений - Математическое моделирование экономических процессов
При решении многих задач (планирование мелкосерийного производства, распределение кораблей по путям сообщения, выработка суждений типа "да-нет" и т. п.)...
-
В настоящей работе растворы готовились весовым методом: путем растворения точно взвешенных навесок в мерной посуде. Концентрации тестируемых соединений в...
-
Порядок расчетов - Математическое моделирование процесса ректификации
Решение приведенных выше уравнений математической модели ректификационной колонны проводят в следующей последовательности: 1. Задаются данные,...
-
Теория игр - Математическое моделирование экономических процессов
Одна из задач теории оптимальных решений - принятие решения в условиях неопределенности. Для обоснования решений разработаны специальные математические...
Контрольная работа 2, Аналитическая часть., Практическое задание. - Математическая модель кинетики процесса