АДРЕНЕРГИЧЕСКИЕ РЕЦЕПТОРЫ И ИХ РОЛЬ В РЕГУЛЯЦИИ КРОВООБРАЩЕНИЯ - Инотропные и вазоактивные средства в реаниматологии и интенсивной терапии
Начало разработки современной концепции рецепторов и их значения в регуляции функциональной активности клеток и нервных окончаний связано с именем JN Langley, предложившего в 1905 году объяснение действия кураре на скелетную мускулатуру.
В 1948 году Ahlquist опубликовал в "American Journal Of Physiology" Ставшую классической статью "Изучение адренотропных рецепторов". которую первоначально не приняли для публикации в Journal of Pharmacology and Experimental Therapy, как "не соответствующую признаным принципам физиологии" (Wenger And Greenbaum, 1984). При исследовании физиологических реакций на воздействие различных адренергических агонистов Alquist получил результаты "подтверждающие теорию о том, что существует всего лишь один адренергический нейрогормон -- симпатии, и что симпатии фактически идентичен эпинефрину (адреналину)".
Автор впервые разделил адренотропные рецепторы на два типа, которые он обозначил как a--и b. Симпатомиметические амины, стимулирующие--a-рецепторы, вызывали вазоконстрикцию, тогда как стимуляторы--b-рецепторов вызывали вазодилятацию. Стимуляцию сердца Alquist связывал с b-эффектом, поскольку ее вызывали главным образом те же амины, которые обладали вазодилятирующими свойствами.
Многочисленные работы, последовавшие за этим классическим исследованием, позволили сформировать современную продолжающую развиваться концепцию адренергических рецепторов. На этой концепции основаны наши представления о регулировании функции сердечно-сосудистой системы в физиологических и патологических условиях, а также выбор медикаментозных средств для терапии тяжелых нарушений кровообращения и сердечной недостаточности.
Согласно современным представлениям все воздействия симпатической нервной системы на сердце и сосуды осуществляются через рецепторы, расположенные на мембране клетки (таблица 2). Главным образом это 3 типа рецепторов: ?-адренергические, ?-адренергические и рецепторы, с которыми взаимодействуют основные нейротрансмиттеры норадреналин (норэпинефрин) и допамин, а также адренергический (симпатомиметический) гормон адреналин (эпинефрин), выбрасываемый в кровь мозговым слоем надпочечников.
Таблица АДРЕНЕРГИЧЕСКИЕ РЕЦЕПТОРЫ И ИХ ЧУВСТВИТЕЛЬНОСТЬ К РАЗЛИЧНЫМ СИМПАТОМИМЕТИЧЕСКИМ АМИНАМ
|
Рецептор |
Дозы |
Добутамин |
Допамин |
Адреналин |
Норадреналин* |
Изопротеренол |
Эфедрин |
Мезатон |
|
a1 |
Малые |
+ |
+ |
+ |
+++ |
0 |
++ |
+ |
|
-- |
Большие |
++ |
+++ |
+++ |
++++ |
0 |
+++ |
+++ |
|
a2 |
Малые |
0 |
+ |
+ |
+++ |
0 |
- |
- |
|
-- |
Большие |
0 |
+++ |
++ |
+++ |
0 |
- |
- |
|
b1 |
Малые |
+++ |
++ |
+++ |
+ |
++ |
+ |
0 |
|
-- |
Большие |
++++ |
++ |
++ |
++ |
++++ |
+ |
0 |
|
b2 |
Малые |
+ |
+ |
++ |
0 |
+++ |
+ |
0 |
|
-- |
Большие |
+++ |
0 |
0 |
0 |
+++ |
++ |
0 |
|
DA1 |
Малые |
0 |
++++ |
0 |
0 |
0 |
0 |
0 |
|
Большие |
0 |
++ |
0 |
0 |
0 |
0 |
0 | |
|
DA2 |
Малые |
0 |
++ |
0 |
0 |
0 |
0 |
0 |
|
Большие |
0 |
+ |
0 |
0 |
0 |
0 |
0 |
a-Адренергические рецепторы подразделяются на два подтипа: a1 - адренергические рецепторы и a2-адренергические рецепторы. В отношении локализации этих подтипов рецепторов существуют некоторые разногласия. Вначале полагали, что a1-адренергические рецепторы являются преимущественно постсинаптическими, тогда как a2 - представляют собой только пресинаптические рецепторы. Однако теперь уже описаны и постсинаптические a2-рецепторы. Постсинаптические a1-адренорецепторы, обнаруженные в сердце, играют важную роль в реализации инотропного эффекта добутамина, поскольку их стимуляция увеличивает силу сокращения миокарда, не повышая частоту сокращений. Положительный инотропный эффект a1-агонистов проявляется медленнее, чем эффект b-агонистов. зато длится дольше. При исследовании миокарда больных с ЛЖ сердечной недостаточностью было показано, что плотность и функциональная активность a1-адренорецепторов v них сохраняются, тогда как число b1 - рецепторов в миокарде уменьшается [12]. Это наблюдение представляется чрезвычайно важным. поскольку открывает возможно еще один подход к терапии хронической сердечной недостаточности.
Пресинаптические--a2-рецепторы стимулируются главным образом норадреналином, освобождаемым в окончаниях симпатических нервов, хотя, по видимому, они могут реагировать также и на повышение концентрации циркулирующего адреналина и на экзогенные катехоламины (Langer A. Shepperson. 1982). Активизация этих рецепторов приводит к подавлению выброса норадреналина на нервных окончаниях.
В кровеносных сосудах представлены оба типа адренорецепторов. Стимуляция постсипаптических a1 и a2.-адренорецепторов вызывает вазоконстрикцию, а функция пресинаптических сосудистых a2-рецепторов так же, как и в сердце -- заключается в ограничении выброса 'норадреналина в нервных окончаниях по принципу обратной связи.
Стимуляция находящихся в ЦНС--a2-адренорецепторов (напр. клонидином) приводит к подавлению выброса симпатомиметических агентов и тем самым оказывает гипотензивное и седативное действие. a-Адренорецепторы с различной плотностью распределены также в волосяных сосочках кожи, в мочевом пузыре, в матке, в сфинктерах желудочно-кишечного тракта. При передозировке a-адреномиметиков нередко можно наблюдать появление "гусиной кожи" в результате сокращения волосяных сосочков при стимуляции их ос-рецепторов.
Потенциальная активность адреномиметиков в отношении a-рецепторов распределена в таком порядке:
НОРАДРЕНАЛИН > АДРЕНАЛИН > ФЕНИЛЭФРИН > ИЗОПРОТЕРЕНОЛ, а в отношении--b-адренорецепторов в другом:
ИЗОПРОТЕРЕНОЛ > АДРЕНАЛИН > НОРАДРЕНАЛИН > ФЕНИЛЭФРИН.
Через b-адренорецепторы осуществляется регулирование функций сердца и состояния гладкой мускулатуры бронхов и сосудов, b-адрено-рецепторы в свою очередь разделяются на два подтипа -- b--1--и--b2. Их функция, количественное соотношение и распределение на поверхности клеток различаются в зависимости от локализации (Табл. 3).
Таблица 3
ЛОКАЛИЗАЦИЯ РЕЦЕПТОРОВ И ЭФФЕКТЫ, СВЯЗАННЫЕ С ИХ СТИМУЛЯЦИЕЙ
|
Рецептор |
Локализация |
Эффект |
|
b1 |
Миокард |
Повышение сократимости желудочков и предсердий |
|
b1-- |
Синусно-предсердный узел |
Повышение ЧСС |
|
b1 |
Предсердно-желудочковая проводящая система |
Увеличение предсердно-же-лудочковой проводимости |
|
b2 |
Артериолы |
Вазодилятаиия |
|
b2 |
Легкие |
Бронходилятаиия |
|
a |
Миокард |
Повышение сократимости |
|
a |
Артериолы |
Вазоконстрикция |
|
Допа |
Почки |
Увеличение кровотока и диуреза |
|
Допа |
Коронарные и мезентериальные сосуды |
Увеличение перфузии миокарда и кишечника |
В сердце представлены оба подтипа рецепторов, хотя преобладают b1-адре-нергические рецепторы. Имеются сообщения о том, что соотношение b1:b2Рецепторов в миокарде различных отделов сердца варьирует в широких пределах -- от 82:18 до 43:57 в правом предсердии: 66:34 в левом предсердии; от 87:13 до 62:38 в ПЖ и от 86:14 до 41:59 в ЛЖ. Примечательно, что в синусовом узле преобладают b2-адренергические рецепторы, что подтверждает предположение некоторых исследователей о ведущей роли b2-рецепторов в физиологической регуляции частоты сердечных сокращений. Стимуляция b - рецепторов вызывает положительные инотропный и хронотропный ответы сердечной мышцы. При стимуляции b2-адренергических рецепторов, которые располагаются преимущественно в легких и в сосудах, наблюдается выраженный бронхолитический и сосудорасширяющий эффекты.
Клеточные - эффекты--a--и--b рецепторов опосредуются через стимуляцию (b1и--b2) или угнетение--(a2) аденилатциклазной активности. Рецепторы--a1 передают сигнал от места его взаимодействия с агонистом через фосфолипазу-Ц с последующей реализацией положительного инотропного эффекта путем увеличения внутриклеточного потока Са (Рис. 1); этот механизм был описан совсем недавно и связан с преобразованием фосфоинозитола на клеточной мембране [Dhainaut JF. 1988: Fleming JW Et. al. 1992: Scalea ThM Et. al, 1992] .
Положительные инотропный и хронотропный эффекты стимуляции b-адренергических рецепторов реализуются через систему, так называемого, вторичного внутриклеточного посредника -- циклического аденозин 3'.5' монофосфата (ЦАМФ). Контрактильная функция кардиомиоцита регулируется путем интеграции различных электрических. нейрогуморальных и гормональных сигналов, в распознавании и передаче которых извне к эффектору внутри клетки участвуют три белковых компонента: сам рецептор, протеин G, выполняющий роль регулирующего фактора, и энзим аденилатциклаза.
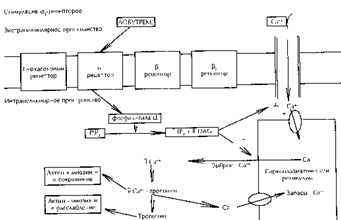
Рис.1 Реализация положительного инотропного эффекта стимуляции Добутрексом a1-адренорецепторов.
Согласно современным научным представлениям упрощенная модель стимуляции сократимости миокарда агонистами b-адренорецепторов выглядит так: гормоны или нейротрансмиттеры связываются с рецепторами на наружной поверхности мембраны клетки, взаимодействие b-адренергических рецепторов с их лигандами приводит к активации связанного с мембраной энзима -- аденилатциклазы. (Нужно отметить. что в отличие от--b-адренорецепторов, стимуляция которых приводит к повышению активности аденилатциклазы, агонисты a-- адренорецепторов снижают активность этого энзима в клетках миокарда). Аденилатциклаза катализирует преобразование аденозин 3' -- фосфата (АТФ) в циклический аденозин 3',5' монофосфат (цАМФ). который через ЦАМФ-зависимую протеинкиназу участвует в фосфорилировании протеинов и в реализации специфической деятельности кардиомиоцита (сократимость, расслабление, частота сокращений). Внутриклеточный энзим фосфодиэстераза вызывает расщепление ЦАМФ. что приводит к снижению концентрации этого нуклеотида и ослаблению эффектов стимуляции b-адренорецепторов. Ингибирование фосфодиэстеразы, на чем основано терапевтическое действие таких некатехоламиновых инотропов, как амринон, милринон и эноксимон. приводит к увеличению концентрации цАМФ и усилению эффектов. связанных со стимуляцией b-адренорецепторов.
Известно, что повторные или продолжительные воздействия агонистов на--b-рецепторы приводят к ослаблению их реакции (down-regulation). т. е. к развитию Тахифилаксии. Обычно толерантность сердца к вводимым b-стимуляторам развивается после 72 часов непрерывной инфузии ( Unverferth 1980), но в литературе имеются сообщения и о более раннем (через 24 часа) снижении чувствительности миокарда к вводимым инотропам. При продолжительной инфузии добутамин сохраняет свою гемодинамическую эффективность в большей степени, чем допамин. Это обусловлено тем, что допамин оказывает свое действие на миокард опосредованно через освобождение норадреналина в нервных окончаниях, запасы которого в процессе длительного лечения истощаются {MacCannel), а добутамин действует на bрецепторы непосредственно.
В основе феномена тахифилаксии лежит свойство адренергических рецепторов изменять свою конформацию, численность на поверхности мембраны клетки, способность к связыванию и сродство к воздействующему на них агонисту. Имеют значение также и некоторые ауторегуляторные процессы во всей популяции адренергических рецепторов. Сродство--a-адренергических рецепторов с агонистами находится под двойным контролем: с одной стороны оно регулируется гуаниннуклеотидазой, а с другой -- взаимоотношения рецептора с агонистом модулируются в зависимости даже от небольших изменений концентрации катехоламинов в плазме. Очевидно, что изменения сродства рецепторов к агонистам приводят к изменениям выраженности реакций как на эндогенные, так и на экзогенные катехоламины.
Плотность адренергических рецепторов на клеточной мембране не постоянна; она может изменяться при многих заболеваниях и палогических состояниях (таблица 4).
Изменения плотности и чувствительности рецепторов оказывают серьезное влияние на эффективность терапии больных, находящихся в критических состояниях, в частности, в состоянии шока. Снижение числа ?-адреноэргических рецепторов в миокарде у больных с хронической застойной сердечной недостаточностью выражается в конечном счете в понижении чувствительности сердца к катехоламинам. что весьма характерно для поздних стадий заболевания, наблюдается также и у больных с острой сердечной недостаточностью -- при продолжительной терапии катехоламинами чувствительность к ним миокарда снижается и тогда для поддержания приемлемого уровня кровообращения приходится постоянно наращивать скорость введения препаратов. Одним из клинических подтверждений этого феномена является наблюдение больных после трансплантации сердца. Пересаженное (денервированное) сердце, не испытывающее хронической атаки нейротрансмиттерами. оказывается более чувствительным к хронотропным воздействиям изопротеренола. чем больное сердце реципиента и чем здоровое сердце.
При септическом (эндотоксиновом) шоке наблюдается снижение чувствительности и плотности--b-адренорецепторов в печени и--a-адре-нергических рецепторов в сосудах, что, по крайне мере частично, может объяснить нарушения стабильности уровня сахара в крови и трудно поддающуюся коррекции вазодилятацию у септических больных.
Таблица 4
ИЗМЕНЕНИЯ ПЛОТНОСТИ РЕЦЕПТОРОВ НА ПОВЕРХНОСТИ КЛЕТОК ПРИ НЕКОТОРЫХ ЗАБОЛЕВАНИЯХ И СОСТОЯНИЯХ.
|
Заболевания и состояния |
Рецепторы |
Изменения |
|
Сердечная недостаточность |
b(сердце) |
Повышение' |
|
Сепсис |
a (печень, сосуды) |
Снижение |
|
Ишемия миокарда |
b(сердце) |
Снижение |
|
Ишемия миокарда |
a (сердце) |
Повышение |
|
Астма° |
b--(легкие лейкоциты). |
Снижение |
|
Новорожденные |
ab (сердце, лейкоциты, тромбоциты) |
Снижение |
|
При введении агонистов |
ab--(сердце, лейкоциты, Тромбоциты ) |
Снижение |
|
При введении антагонистов |
ab--(сердце, лейкоциты, тромбоциты) |
Повышение |
|
Гипертиреоидизм |
b (сердце |
Повышение |
|
Гипотиреоидизм |
b (сердце) |
Снижение |
|
Глюкокортикойды |
b--(сердце, лейкоциты) |
Повышение |
' - плотность--b адренорецепторов снижается при тяжелых формах сердечной недостаточности
° -- при чрезмерной использовании--b-адреномиметиков в терапии астматических приступов
Специфические эффекты катехоламинов -- инотропные, хронотропные, сосудистые -- могут быть ослаблены не только в связи с изменениями плотности адренорецепторов на наружной поверхности мембраны, но и вследствие пострецепторных внутриклеточных изменений. Такие условия наблюдаются, например, у новорожденных или при длительном воздействии катехоламинов, а также при хроническом использовании блокаторов a- и b-адренорецепторов. Снижение эффективности экзогенных катехоламинов при длительном их применении у больных с тяжелыми нарушениями кровообращения и метаболизма обусловлено также и изменениями энергетического обеспечения миокардиальных клеток.
Поскольку и механизм передачи сигнала, и реализация специфической деятельности клетки вплотную связаны с АТФ, понятно, что их осуществление возможно лишь при условии достаточной энергообеспеченности. При гипоксии и ишемии миокарда, когда энергетика клетки страдает и сокращается внутриклеточный пул фосфатов, эффективность стимуляции b-адренорецепторов снижается. Это также является одной из причин развивающейся тахифилаксии миокарда к катехоламинам при длительном их применении у больных с критическими нарушениями кровообращения. Продукция цАМФ у больных в терминальной стадии застойной сердечной недостаточности резко снижена, с чем в значительной степени может быть связана толерантность миокарда этих больных к стимуляции--b-адренорецепторов катехоламинами (Feldman Et аl.. 1987) и ничтожная эффективность инотропной терапии. Однако в литературе по поводу роли дефицита аденилатциклазы и цАМФ в развитии толерантности миокарда к катехоламинам мнения авторов расходятся (Bristow et. al., 1982)
Следует отметить, что a1-адренергические рецепторы, являющиеся, также как и b1-рецепторы, медиаторами положительных инотропных эффектов, подвержены тахифилаксии значительно меньше. Однако объем знаний по этому чрезвычайно важному с терапевтической точки зрения вопросу пока еще весьма ограничен.
Восстановление чувствительности к b-агонистам происходит спустя 7--10 дней после окончания длительной инфузии добутамина.
Похожие статьи
-
Добутамин (ДОБУТРЕКС) Добутамин является синтетическим катехоламином, который был создан для лечения больных с застойной сердечной не достаточностью...
-
Норадреналин - Инотропные и вазоактивные средства в реаниматологии и интенсивной терапии
Норадреналин (норэпинефрин} является естественным химическим нейромедиатором в симпатической нервной системе. Через стимуляцию a-...
-
Адреналин - Инотропные и вазоактивные средства в реаниматологии и интенсивной терапии
Адреналин (эпинефрин) является одним из важнейших эндогенных гормонов, продуцируемым главным образом надпочечниками в ответ на стресс. В отличие от...
-
Допамин - Инотропные и вазоактивные средства в реаниматологии и интенсивной терапии
Допамин (дофамин) является естественным предшественником норадреналина. Он оказывает дозо-зависимое влияние на a и--b-адренергические рецепторы...
-
В силу морфологических и функциональных особенностей правый желудочек сердца в отличие от левого плохо приспособлен к преодолению нагрузки давлением и...
-
Гиповолемия может быть связана с эндогенной и экзогенной кровопотерей (геморрагический шок --разновидность гиповолемического) и с сокращением объема...
-
Изопротеренол - Инотропные и вазоактивные средства в реаниматологии и интенсивной терапии
Изопротеренол (изупрел, новодрин) является синтетическим амином с изолированным--b-адреномиметическим действием....
-
В основе этих синдромов лежит нарушение насосной функции сердца (миокардиальная недостаточность, нарушения ритма) при достаточной преднагрузке...
-
Эти некатехоламиновые препараты представляют собой еще одну группу инотропных средств, механизм действия которых связан с селективным ингибированием...
-
Респираторная поддержка с использованием современных способов и режимов искусственной вентиляции легких является одним из основных методов терапии...
-
ВВЕДЕНИЕ - Инотропные и вазоактивные средства в реаниматологии и интенсивной терапии
Инотропные и вазоактивные препараты широко используются в клинической практике и по праву могут быть отнесены к числу жизненно важных медикаментозных...
-
Мезатон. Гутрон - Инотропные и вазоактивные средства в реаниматологии и интенсивной терапии
Эти препараты с изолированным (?-миметическим свойством оказывают прямое вазоконстрикторное действие и повышают артериальное давление, не влияя...
-
В распоряжении клиницистов имеется несколько препаратов, эффективно стимулирующих сердце и оказывающих мощное влияние на сосуды. В повседневной практике...
-
Сердечные гликозиды - Инотропные и вазоактивные средства в реаниматологии и интенсивной терапии
Препараты дигиталиса широко используются в терапии сердечной недостаточности. В основе механизма их действия лежит усиление внутриклеточного транспорта...
-
Эфедрин, Мезатон - Инотропные и вазоактивные средства в реаниматологии и интенсивной терапии
Этот природный алкалоид по химическому составу и характеру симпатомиметического действия очень похож на адреналин. Эффекты стимуляции--a-...
-
Дозы Допамина - Инотропные и вазоактивные средства в реаниматологии и интенсивной терапии
"Ренальные " дозы -- 1--2.5 мкг/кг/мин Селективная стимуляция почечных допаминовых рецепторов. Повышение клубочковой фильтрации и диуреза. Малые дозы --...
-
В обычных условиях системная доставка или, транспорт, кисло рода к тканям (ТО2), т. е. суммарное количество кислорода, пере носимое к потребляющим его...
-
Септический шок - Инотропные и вазоактивные средства в реаниматологии и интенсивной терапии
Септический шок, как мы уже отмечали, представляет собой тяжелое нарушение распределения сердечного выброса со снижением артериального давления и...
-
Обструктивный шок обусловлен механическими препятствиями кровотоку. Примерами такого шока могут быть массивная тромбоэмболия легочной артерии, синдром...
-
Внутривенные, внутрисердечные или интратрахеальные повторные введения Адреналина (0,5--3,0 мг, т. е. 0,5--3,0 мл 0,1% раствора) являются одним из...
-
Гемодинамический мониторинг АД -- Артериальное давление мониторируют неинвазивным (метод Короткова и др.) и прямым (инвазивным) способом. Измерение АД...
-
ДОЗЫ И СПОСОБЫ ВВЕДЕНИЯ - Инотропные и вазоактивные средства в реаниматологии и интенсивной терапии
В силу особенностей фармакокинетики инотропные и вазоактивные средства при лечении больных с тяжелыми нарушениями кровообращения обычно назначают в виде...
-
С расстройствами кровообращения различной степени - от умеренных изменений АД и сосудистого коллапса до тяжелого шока - приходится сталкиваться врачам...
-
ЛИТЕРАТУРА - Инотропные и вазоактивные средства в реаниматологии и интенсивной терапии
1. Василенко НИ., Эделева Н. В., Довженко Ю М. Журба Н. М Особенности функционирования системы кислородообеспечения в 1-е сутки у пострадавших с...
-
Боли в области сердца, Одышка - Эссенциальная артериальная гипертензия (гипертоническая болезнь)
Боли в области сердца у больных ГБ часто носят функциональный характер (кардиалгии) и связаны, вероятно, с понижением порога восприятия афферентных...
-
Одним из представителей РОФ третьего эшелона является Цп - исключительно активный гликопротеин 2 - глобулиновой фракции сыворотки крови человека и высших...
-
Реализация функциональной активности фагоцитирующих клеток находится, в том числе, под контролем различных отделов нервной системы и регуляторных...
-
Регуляция дыхательных движений - Физиология и гигиена органов дыхания у детей
Регуляция дыхания осуществляется центральной нервной системой, специальные области которой обусловливают Автоматическое дыхание - чередование вдоха и...
-
Блокаторы в-адренорецепторов, ингибиторы АПФ, антагонисты кальция и диуретики относятся к числу основных лекарственных средств, использующихся в...
-
Молекулярные механизмы регуляции клеточной смерти - Биологические механизмы жизненного цикла клетки
Апоптоз - многоэтапный процесс. Первый этап - прием сигнала, предвестника гибели в виде информации, поступающей к клетке извне или возникающей в недрах...
-
РОФ - функционально разнородная группа белков, способных быстро изменять свою концентрацию при различных нарушениях гомеостаза независимо от природы и...
-
Осмотр шеи и кожи, Осмотр тела - Основные методы обследования больного при различных заболеваниях
Недостаточность клапанов аорты сопровождается видимой на глаз пульсацией сонных артерий ("пляской каротид"), которая сопровождается одновременным с...
-
Связь между строением вириона и началом инфекции - Строгие постулаты Коха
Длинные нити (фибриллы) отростка служат для специфического узнавания фагом определенных участков на поверхности клетки-хозяина, к которым он...
-
Сшивки с белками - Фотохимические превращения ДНК. Люминесцентные метки и зонды
При наличии на поверхности носителя функциональных групп, способных вступать в химические реакции с функциональными группами фермента с образованием...
-
Клинические проявления - Хроническая почечная недостаточность
Проявления ХПН зависят от: 1) стадии ХПН;2) выраженности расстройств различных компонентов гомеостаза. В случае отсутствия артериальной гипертензии...
-
Классификация - Нейроэндокринные синдромы в гинекологии. Седечная аритмия
В зависимости от нарушенной функции сердца выделяют следующие группы аритмий: Нарушения автоматизма Номотопные (водитель ритма -- в синусовом узле)...
-
Аутоиммунные процессы, Ожирение и питание - Изменение при сахарном диабете
На возможность значения аутоиммунного процесса (Nerup J. et all, 1978) в развитии диабета указывают ряд данных: 1) присутствие в островках поджелудочной...
-
Глюкагон - Биохимия поджелудочной железы
Й. Строение и биосинтез гормона 1. Немного истории: Глюкагон впервые был получен в коммерческих препаратах инсулина в 1923г., однако лишь в 1953г....
-
Диуретики - Эссенциальная артериальная гипертензия (гипертоническая болезнь)
Диуретики широко применяются для лечения больных эссенциальной АГ. Хотя эти лекарственные средства обладают достаточно высокой эффективностью, их...
-
Ингибиторы АПФ - Эссенциальная артериальная гипертензия (гипертоническая болезнь)
Ингибиторы АПФ -- большая группа лекарственных средств, обладающих широким спектром действия на многочисленные механизмы функциональных и структурных...
АДРЕНЕРГИЧЕСКИЕ РЕЦЕПТОРЫ И ИХ РОЛЬ В РЕГУЛЯЦИИ КРОВООБРАЩЕНИЯ - Инотропные и вазоактивные средства в реаниматологии и интенсивной терапии