Химическое равновесие в растворах, Термодинамика растворения. Растворение газов в жидкостях. Закон Генри. Давление пара растворов. Закон Рауля - Систематика химических элементов
Термодинамика растворения. Растворение газов в жидкостях. Закон Генри. Давление пара растворов. Закон Рауля
Молекулярным (истинным) раствором называется гомогенная система, состоящая из двух и более компонентов. От молекулярных растворов следует отличать Коллоидные растворы (суспензии, эмульсии, аэрозоли), которые представляют собой многокомпонентные гетерогенные системы.
Растворы могут находиться в трех агрегатных состояниях: газообразном, твердом, жидком. Всякий раствор состоит из растворенного вещества и растворителя. Растворителем считают тот компонент, который находится в том же агрегатном состоянии, что и раствор. Если же оба компонента находятся в одинаковом агрегатном состоянии, то растворителем считается тот компонент, который находится в большем количестве.
С термодинамической точки зрения все компоненты раствора равноценны и их деление на растворенное вещество и растворитель является условным.
Жидкие растворы (как и любые жидкости) обладают элементами кристаллической структуры. Для них существует понятие Ближнего порядка, т. е. каждая частица раствора окружена определенным числом других частиц, расположенных от данной на строго определенных расстояниях. Для более удаленных частиц определенность расстояний не существует, т. е. растворы, как и жидкости, не обладают Дальним порядком, характерным для кристаллов.
Растворы считаются системами, занимающими промежуточное положение между химическими соединениями и механическими смесями.
Раствор, находящийся в равновесии с растворяющимся веществом (динамическое равновесие), называется Насыщенным раствором. Ненасыщенный раствор содержит меньше, а Пересыщенный - больше вещества, чем насыщенный.
Большинство кристаллов растворяется в жидкостях с поглощением теплоты, однако при растворении таких веществ, как гидроксид натрия - NaOH, карбонат калия - К2СО3, сульфат меди - CuS04, происходит заметное увеличение температуры раствора. Выделяется теплота также при растворении некоторых жидкостей и всех газов.
Количество теплоты, которое поглощается или выделяется при растворении одного моль вещества, называется Теплотой растворения Этого вещества. Если при растворении теплота поглощается, то теплота растворения имеет отрицательное значение и положительное, если выделяется.
При растворении кристаллов происходит их разрушение, что требует затрат энергии, поэтому растворение должно было бы сопровождаться поглощением теплоты. Если наблюдается обратный эффект, то это показывает, что одновременно с растворением происходит взаимодействие между растворителем и растворенным веществом, при котором в виде теплоты выделяется больше энергии, чем ее расходуется на разрушение кристаллической решетки.
При растворении кристаллического вещества в воде происходит сближение его частиц с дипольными молекулами воды, потенциальная энергия уменьшается, и теплота выделяется, т. е. растворение сопровождается сжатием, которое рассматривается как уплотнение молекул растворителя вокруг каждой частицы растворяемого вещества. При этом частицы химически связываются с молекулами растворителя, образуя соединение, которое называется Сольватом.
Совокупность молекул растворителя, окружающих частицу, называется Сольватной оболочкой. Взаимодействие молекул растворителя с частицами растворенного вещества называется Сольватацией.
Если растворителем является вода, то сольватация называется Гидратацией, а сольватную оболочку называют Гидратной.
Таким образом, при растворении вещества общий тепловой эффект складывается из теплового эффекта собственно растворения и теплового эффекта сольватации. Поскольку первый из этих процессов эндотермичен, а второй - экзотермичен, то общий тепловой эффект процесса растворения может быть как положительным, так и отрицательным.
Закон Генри
Растворение газов в воде представляет собой экзотермический процесс. Поэтому растворимость газов с повышением температуры уменьшается.
При растворении газа в жидкости устанавливается равновесие:
Газ + Жидкость Насыщенный раствор
При этом объем системы существенно уменьшается. Следовательно, повышение давления должно приводить к смещению равновесия вправо, т. е. к увеличению растворимости газа.
Генри сформулировал эту закономерность в более общем виде: парциальное давление пара растворенного вещества над раствором пропорционально молярной доле растворенного вещества в растворе (закон Генри):
P = kX, (43)
Где K - константа Генри (или коэффициент Генри).
Следствие из закона Генри: объем газа, растворяющегося при постоянной температуре в данном объеме жидкости, не зависит от его парциального давления.
Газы подчиняются закону Генри при невысоких давлениях и в случае отсутствия химического взаимодействия между молекулами газа и молекулами растворителя.
Закон Рауля
При данной температуре давление насыщенного пара над жидкостью - величина постоянная. При растворении какого-либо вещества в данной жидкости давление насыщенного пара этой жидкости над раствором понижается, т. е. давление насыщенного пара растворителя над раствором всегда ниже, чем над чистым растворителем при той же температуре. Разность этих давлений получила название Понижение давления пара над раствором.
В 1887 г. французский физик Рауль установил закон, связывающий понижение давления пара (над разбавленными растворами неэлектролитов) с концентрацией растворенного вещества (закон Рауля): Относительное понижение давления насыщенного пара растворителя над раствором равно молярной доле растворенного вещества:
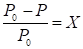
. (44)
Явление уменьшения давления пара растворителя над раствором можно объяснить следующим образом. Равновесие между водой и паром выражается схемой (Н2О)Жидк = (Н2О)Пар. Если теперь растворить в воде некоторое количество вещества, то концентрация молекул воды в растворе уменьшится и пойдет процесс, который ее увеличивает, т. е. процесс конденсации пара. Новое равновесие устанавливается при более низком давлении насыщенного пара растворителя.
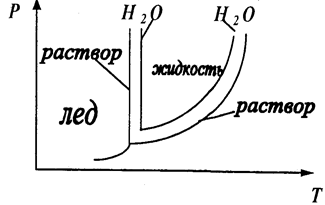
Рис. 18
Похожие статьи
-
Влияние разбавления раствора - Химическая кинетика, равновесия, термодинамика
Это, как и в предыдущем параграфе, изменение концентрации, но не одного вещества, а одновременно всех растворенных веществ. Допустим, что объем раствора...
-
Допустим, реакция aA + bB <> хХ + yY - гомогенная и идет в одну стадию. Тогда скорость прямой реакции vПр = KПр [A]A{B]B, а скорость обратной...
-
Влияние давления - Химическая кинетика, равновесия, термодинамика
Существенно, прежде всего, для реакций с участием газов. Снижение давления ведет к увеличению объема и уменьшению концентраций всех газов, после чего...
-
Тепловые эффекты при растворении. Механизмы растворения веществ в воде - Растворы
Растворение веществ сопровождается различными тепловыми эффектами в зависимости от природы вещества. При растворении в воде, например, гидроксида калия...
-
Осмотическое давление раствора - Характеристика основных видов растворов
В 1748 году было обнаружено явление перехода растворителя через мембрану из менее концентрированного раствора в более концентрированный, которое назвали...
-
Свойства растворов неэлектролитов. Замерзание и кипение растворов. Законы Рауля - Основы химии
По наличию или отсутствию электрической проводимости растворы веществ делят на электролиты - проводящие электрический ток, и неэлектролиты - не...
-
Фактически это следствие первого начала термодинамики, но сформулирован раньше, чем первое начало. Тепловой эффект изобарного (или изохорного) процесса...
-
КОЛЛИГАТИВНЫЕ СВОЙСТВА РАСТВОРОВ - Растворы
Коллигативными свойствами называют физико-химические свойства растворов, которые обусловлены Природой растворителя и числом частиц растворенного вещества...
-
Закон действующих масс. Правило Вант-Гоффа - Систематика химических элементов
Скорость химической реакции зависит, прежде всего, от природы реагирующих веществ, а также от условий протекания реакции: концентрации, температуры,...
-
Теплота образования. Теплота сгорания. Следствия из закона Гесса - Систематика химических элементов
Теплотой образования называется тепловой эффект при образовании из простых веществ одного моль соединения. При этом теплота образования простых веществ...
-
Энтальпия. Закон Гесса. Тепловой эффект химической реакции Атом валентность кристалл химический Примем, что единственным видом работы, которую совершает...
-
Растворимость веществ - Растворы
Растворение - самопроизвольный (так как идет с увеличением энтропии в системе) обратимый процесс. Однако растворение возможно только до определенного...
-
Фазовое равновесие. Правило фаз. Диаграмма состояния однокомпонентной системы Гетерогенные равновесия, связанные с переходом веществ из одной фазы в...
-
РАСТВОРЫ. РАСТВОРИМОСТЬ, Общая характеристика и классификация растворов - Растворы
Общая характеристика и классификация растворов Растворы имеют большое значение для живых организмов (питательные вещества усваиваются в виде растворов;...
-
Разбавленные Растворы неэлектролитов (веществ, растворы или расплавы которых не проводят электрический ток) обладают рядом свойств, количественное...
-
Опытным путем, задолго до появления молекулярно-кинетической теории, был открыт целый ряд законов, описывающих равновесные изопроцессы в идеальном газе....
-
ВИДЫ РАСТВОРОВ. РАСТВОРИМОСТЬ. ПРОЦЕСС РАСТВОРЕНИЯ - Характеристика основных видов растворов
Растворы - гомогенные системы, состоящие из двух или более компонентов (растворителя, растворенного вещества и продуктов их взаимодействия), состав...
-
Ниже рассматривается наиболее важный изобарно-изотермический случай. Если реакция идет в изохорно-изотермических условиях, то вместо энергии Гиббса нужно...
-
Принцип Ле Шателье - Систематика химических элементов
Химическое равновесие, отвечающее равенству скоростей прямой и обратной реакций и минимальному значению энергии Гиббса (G0Т=0), является наиболее...
-
Второе начало термодинамики. Энтропия Из предыдущих глав мы знаем много обратимых процессов, но есть и необратимые, например: - переход тепла от горячего...
-
МЕТОДЫ ОСАЖДЕНИЯ, ИОННОГО ОБМЕНА, МЕМБРАННЫЕ МЕТОДЫ - Химические свойства и строение воды
Современные технологии позволяют изготавливать объемные или плоские фильтрующие материалы с однородными каналами практически любого размера. Мембранный...
-
Термодинамика. Химическая термодинамика. Термодинамические системы. Энергия. Внутренняя энергия Термодинамика изучает взаимное превращение теплоты,...
-
Необратимые и обратимые реакции. Химическое равновесие Когда при химическом взаимодействии хотя бы одно из веществ расходуется полностью, реакцию считают...
-
Еще три следствия из закона Гесса - Химическая кинетика, равновесия, термодинамика
2. Тепловой эффект процесса равен разности между суммами теплот сгорания исходных веществ и продуктов с учетом коэффициентов в уравнении реакции. (при...
-
Второе начало термодинамики. Энтропия Объединенное уравнение первого и второго начал термодинамики Рис. 12 Из выражения первого начала термодинамики U =...
-
Гомогенные равновесия в растворах электролитов Константа ионизации (диссоциации) слабого основания на примере аммиака (запись NH3*H2O предпочтительнее,...
-
Электролиз - физико-химический процесс, состоящий в выделении на Электродах составных частей растворенных веществ или других веществ, который возникает...
-
Первое начало термодинамики. Энтальпия - Химическая кинетика, равновесия, термодинамика
Это закон сохранения энергии. Подводимая к системе теплота Q расходуется на изменение ее внутренней энергии и на совершение работы А: Q = U + А Здесь U =...
-
Выбор оптимальных условий проведения реакций - Химическая кинетика, равновесия, термодинамика
Если наша цель - получить максимальный выход продукта за определенное небольшое время, а реакция медленная и обратимая, то нужно одновременно учитывать...
-
Истинное и ложное равновесие Все химические реакции в той или иной степени обратимы. Если возможна реакция aA + bB хХ + yY, то возможна и обратная...
-
В предыдущих разделах рассмотрены отдельные аспекты кинетики, а теперь пора подвести общие итоги: от чего зависят скорости реакций и как можно ими...
-
Влияние различных факторов на растворимость веществ - Растворы
Растворимость зависит от природы растворяемого вещества и растворителя, температуры, давления и влияния посторонних веществ. Природа веществ, образующих...
-
(а) На основе уравнения ЗДМ объясните физический смысл константы скорости. (б) Зависит ли константа скорости от концентраций реагентов? от их природы? от...
-
В технике в большинстве случаев инженер имеет дело с дисперсными системами, которые состоят из дисперсной фазы и дисперсионной среды. Дисперсная фаза -...
-
Основы химической термодинамики. Первое начало термодинамики Термодинамические системы и термодинамические параметры. Функции состояния. Парциальные...
-
Растворы - термодинамические устойчивые системы переменного состава, состоят не менее чем из двух компонентов и продуктов их взаимодействия. Это...
-
Общие сведения Гетерогенные реакции еще труднее для изучения, чем гомогенные, и в обычных учебниках общей химии им уделяется мало внимания, хотя они...
-
Влияние концентрации - Химическая кинетика, равновесия, термодинамика
При возрастании концентрации какого-то из веществ (исходных или продуктов) равновесие смещается в сторону его расходования, а при уменьшении концентрации...
-
Краткая теория Основное уравнение гомогенной кинетики - закон действующих масс, ЗДМ (хотя реально подставляются не массы, а молярные концентрации):...
-
Общие сведения Термодинамика - наука о превращениях энергии в различных процессах, как физических, так и химических, и о направлении процессов, о...
Химическое равновесие в растворах, Термодинамика растворения. Растворение газов в жидкостях. Закон Генри. Давление пара растворов. Закон Рауля - Систематика химических элементов