Принцип Ле Шателье - Систематика химических элементов
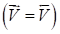
Химическое равновесие, отвечающее равенству скоростей прямой и обратной реакций и минимальному значению энергии Гиббса (G0Т=0), является наиболее устойчивым состоянием системы при заданных условиях и остается неизменным до тех пор, пока сохраняются постоянными параметры, при которых равновесие установилось. При изменении условий равновесие нарушается и смещается влево или вправо. Через некоторое время система вновь становится равновесной, т. е. она переходит из одного состояния в другое. Новое равновесие характеризуется новым равенством скоростей прямой и обратной реакций и новыми равновесными концентрациями всех веществ в системе.
Химическое равновесие является подвижным (динамическим). Оно смещается в ту или иную сторону потому, что изменение условий по-разному влияет на скорости прямой и обратной реакций, тем самым нарушая равенство скоростей. Если при изменении внешних условий химическое равновесие нарушается так, что скорость прямой реакции
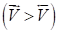
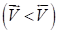
Становится больше скорости обратной реакции, то равновесие смещается вправо. Если же равновесие нарушается так, что скорость прямой реакции становится меньше, чем скорость обратной реакции, то равновесие смещается влево. Направление смещения равновесия в общем случае определяется принципом Ле Шателье:
Если на систему, находящуюся в равновесии, оказать внешнее воздействие, то равновесие смещается в том направлении, которое ослабляет эффект внешнего воздействия.
Смещение равновесия может быть вызвано изменением температуры, концентрации одного из реагентов, давления. Температура - тот параметр, от которого зависит величина константы равновесия химической реакции. При повышении температуры уменьшается константа равновесия экзотермического процесса H0Т <О или U0Т <0, при понижении температуры увеличивается. Это значит, что при повышении температуры равновесие экзотермической реакции смещается влево, поскольку прямая реакция идет с выделением теплоты.
Скорость как экзотермической, так и эндотермической реакции при повышении температуры растет, а при понижении уменьшается. Однако изменение скоростей и при повышении (или понижении) температуры не одинаково, поэтому варьируя температуру, можно смещать равновесие в заданном направлении.
Смещение равновесия может быть вызвано изменением концентрации одного из компонентов: добавлением вещества в равновесную систему или выводом его из системы. По принципу Ле Шателье, при изменении концентрации одного из участников реакции равновесие смещается в сторону, компенсирующую изменение, т. е. при повышении концентрации одного из исходных веществ - вправо, а при повышении концентрации одного из продуктов реакции - влево.
Действительно, при увеличении концентрации исходного вещества А (или В) в равновесной системе А+В <=> C+D равенство скоростей =нарушается, так как возрастает скорость прямой реакции
=К1СAСB;
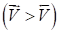
Равновесие смещается вправо. Если же увеличить концентрацию продукта реакции С (или D), то возрастет скорость обратной реакции
= К1СCСD,
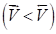
Равновесие смещается влево.
Если в обратимой реакции участвует хотя бы одно газообразное вещество, смещение равновесия может быть вызвано изменением давления. Повышение давления при T=const равносильно сжатию газа, т. е. увеличению его концентрации. При увеличении концентрации газообразного компонента скорость реакции в соответствии с законом действующих масс растет, что приводит к смещению равновесия в направлении уменьшения концентрации газообразного компонента. При понижении давления при T = const газ расширяется, и его концентрация в системе падает. Это вызывает понижение скорости реакции; равновесие смещается в направлении увеличения давления газа.
Если в реакции участвуют несколько газообразных веществ, то при изменении давления одновременно и одинаково изменяются все их концентрации. Однако смещение равновесия может при этом не произойти.
Итак, в соответствии с принципом Ле Шателье при повышении давления равновесие смещается в сторону образования меньшего количества молей газообразных веществ в газообразной смеси и, соответственно, в сторону уменьшения давления в системе. Наоборот, при внешнем воздействии, вызывающем понижение давления, равновесие смещается в сторону образования большего количества молей газа, что и противодействует внешнему воздействию и вызывает увеличение давления в системе.
На основе принципа Ле Шателье можно подобрать такие условия осуществления химического равновесия, которые обеспечивают наибольший выход продуктов реакции. Принцип Ле Шателье справедлив не только для химических равновесий; он приложим и к процессам фазовых превращений: к испарению, конденсации и др.
Похожие статьи
-
Необратимые и обратимые реакции. Химическое равновесие Когда при химическом взаимодействии хотя бы одно из веществ расходуется полностью, реакцию считают...
-
Смещение химического равновесия. Принцип Ле-Шателье - Основы химии
Положение химического равновесия зависит от следующих параметров реакции: температуры, давления и концентрации. Влияние, которое оказывают эти факторы на...
-
Закон действующих масс. Правило Вант-Гоффа - Систематика химических элементов
Скорость химической реакции зависит, прежде всего, от природы реагирующих веществ, а также от условий протекания реакции: концентрации, температуры,...
-
Скорость химической реакции. Энергия активации химической реакции Химическая термодинамика изучает возможность, направление и пределы самопроизвольного...
-
Смещение равновесия Смещение равновесия - это изменение состояния равновесия (изменение равновесного соотношения количеств исходных веществ и продуктов)...
-
Теплота образования. Теплота сгорания. Следствия из закона Гесса - Систематика химических элементов
Теплотой образования называется тепловой эффект при образовании из простых веществ одного моль соединения. При этом теплота образования простых веществ...
-
Теплота. Работа. Первое начало термодинамики - Систематика химических элементов
Все изменения внутренней энергии при ее переходе от одной системы к другой можно разбить на две группы. В первую группу входят формы перехода энергии за...
-
Термодинамика. Химическая термодинамика. Термодинамические системы. Энергия. Внутренняя энергия Термодинамика изучает взаимное превращение теплоты,...
-
Реакторами идеального (полного) смешения называются реакторы непрерывного действия, в которых осуществляется турбулентный гидродинамический режим. В них...
-
Свободная энергия Гельмгольца. Свободная энергия Гиббса - Систематика химических элементов
Химические процессы обычно протекают либо при постоянном объеме и температуре (закрытые системы), либо при постоянном давлении и температуре (открытые...
-
Истинное и ложное равновесие Все химические реакции в той или иной степени обратимы. Если возможна реакция aA + bB хХ + yY, то возможна и обратная...
-
Энтальпия. Закон Гесса. Тепловой эффект химической реакции Атом валентность кристалл химический Примем, что единственным видом работы, которую совершает...
-
ХИМИЧЕСКАЯ КИНЕТИКА И ХИМИЧЕСКОЕ РАВНОВЕСИЕ - Неограническая химия
Задание 4.1: 4.1.1. Проанализируйте данную Вам реакцию (табл. IV.1) и укажите, какой она является: гомогенной или гетерогенной. 4.1.2. Запишите...
-
Химическим равновесием называется такое состояние химической системы, при котором количества исходных веществ и продуктов не меняются со временем. 1....
-
Энергия и длина связи. Обменный механизм образования ковалентной связи. Свойства ковалентной связи. Валентность. Донорно-акцепторный механизм образования...
-
Второе начало термодинамики. Энтропия Объединенное уравнение первого и второго начал термодинамики Рис. 12 Из выражения первого начала термодинамики U =...
-
Рассмотрим реакцию между веществами А и В, протекающую по схеме: А А + в В = с С + d D Количественно зависимость между скоростью реакции и концентрациями...
-
Химические свойства - Биогенные элементы. Сера
Сера вступает в реакцию со всеми металлами, в результате чего образуются сульфиды. В большинстве случаев для химической реакции необходим катализатор, в...
-
При нагревании (подводе тепла) равновесие смещается в сторону протекания эндотермической реакции (поглощения этого тепла), а при охлаждении - в сторону...
-
В зависимости от направления перекрывания атомных орбиталей различают два вида ковалентной связи: -связь возникает при перекрывании атомных орбиталей...
-
Скорость реакции определяется изменением молярной концентрации одного из реагирующих веществ: V=dC/dtV. Факторы, влияющие на скорость химических...
-
Катализ - Концепции современного естествознания: химическая составляющая
Наиболее сильное влияние на скорость реакции оказывает присутствие в реагирующей системе Катализатора -- вещества, которое повышает (а иногда и уменьшает...
-
Роберт Боиль - Становление понятия о химическом элементе
Боиль жил в эпоху великих общественных и духовных преобразований. Однако несмотря на сильные религиозные тенденции, Бойль научными работами расчистил...
-
Ван-дер-Ваальсовы силы: ориентационная, индукционная и дисперсионная составляющие. Полная энергия межмолекулярного взаимодействия Молекула - Химически...
-
К сожалению, многие учебники химии построены не вполне логично, в частности, одно и то же слово может использоваться в разных смыслах, поэтому...
-
Основы химической термодинамики. Первое начало термодинамики Термодинамические системы и термодинамические параметры. Функции состояния. Парциальные...
-
Актуальность темы. В современных условиях глобальной конкуренции на все более интегрирующихся мировых рынках, развитие химической промышленности...
-
Периодическое изменение свойств атомов химических элементов - Систематика химических элементов
Химические свойства атомов элементов проявляются при их взаимодействии. Типы конфигураций внешних энергетических уровней атомов определяют основные...
-
Если атом находится в основном (т. е. в невозбужденном) состоянии, то его электроны занимают самые низкие по энергиям орбитали. Однако в многоэлектронном...
-
Строение атома, Квантовые числа. Атомные орбитали - Систематика химических элементов
Квантовые числа. Атомные орбитали Состояние электрона в атоме любого химического элемента характеризуется четырьмя квантовыми числами: главным,...
-
Роберт Бойль, Михаил Васильевич Ломоносов - Становление понятий о химическом элементе
Бойль жил в эпоху великих общественных и духовных преобразований. Однако несмотря на сильные религиозные тенденции, Бойль научными работами расчистил...
-
ХИМИЧЕСКИЕ СВОЙСТВА АЛЮМИНИЯ. ПРИМЕНЕНИЕ - Химические элементы главной подгруппы III группы
Легкий, мягкий, быстро окисляющийся металл серебристо-белого цвета Алюминий -- очень активный металл. В ряду напряжений он стоит после щелочных и...
-
Введение, Общая характеристика химического элемента, Физические свойства - Биогенные элементы. Сера
Семра -- элемент шестой группы третьего периода главной подгруппы периодической системы химических элементов Д. И. Менделеева, с атомным номером 16....
-
Допустим, реакция aA + bB <> хХ + yY - гомогенная и идет в одну стадию. Тогда скорость прямой реакции vПр = KПр [A]A{B]B, а скорость обратной...
-
Кинетика химических реакций - Концепции современного естествознания: химическая составляющая
Одна из особенностей химических реакций заключается в том, что они протекают во времени. Одни реакции протекают медленно, месяцами, как, например,...
-
Краткая теория В старом учебнике Глинки вопрос хорошо изложен на качественном уровне, но не хватает строго количественного описания влияния температуры...
-
Физико-химические свойства хрома - Хром. Элемент периодической системы химических элементов
Хром является серебристо-белым, твердым, блестящим, но в то же время довольно хрупким металлом. Ранее считалось, что хром практически не обладает...
-
(а) На основе уравнения ЗДМ объясните физический смысл константы скорости. (б) Зависит ли константа скорости от концентраций реагентов? от их природы? от...
-
По характеру химической связи кристаллы делятся на 4 группы: молекулярные, ковалентные, ионные и металлические. В соответствии с этой классификацией...
-
Кристаллическая решетка. Координационное число Кристаллы - Твердые тела, обладающие трехмерной периодической структурой, которая называется...
Принцип Ле Шателье - Систематика химических элементов