Ситуационная задача № 1 - Химико-токсикологический анализ органов трупа
Вариант 1
На СХЭ доставлены внутренние органы трупа (желудок с содержимым, печень, почки, мозг, жировая ткань, легкое), кровь, моча, две склянки с остатками вязкой жидкости винно-красного цвета. Биообъекты не подвержены гнилостному разложению.
Обстоятельства дела
К., будучи в состоянии среднего алкогольного опьянения, вошел в лабораторию, где выполнял свое первое научное исследование его знакомый - аспирант - патологоанатом. Был вечер. Знакомый К., заканчивая работу, сказал, что подозрения на отравление ликером не подтверждаются и указал на стоящие рядом две склянки. К. (по специальности художник) решил, что остатки "ликеров" теперь можно забрать и использовать по прямому назначению. Аспирант очень торопился на другую работу в бюро СМЭ, и не заметил исчезновения двух склянок.
Приятели, поговорив немного, разошлись по своим делам. Вечером следующего дня аспирант не смог найти обе склянки с "ликерами", содержимое которых далее должен был анализировать другой аспирант - судебный химик. Через три дня аспирант опять дежурил в бюро СМЭ, куда привезли для СМЭ труп его знакомого К.
Цель исследования: провести СХЭ внутренних органов трупа на наличие "Летучих ядов".
Приведите схему химико-токсикологического анализа представленных объектов экспертиза труп яд токсический
Информация:
При проведении СМЭ эксперт установил, что смерть произошла около 20 часов тому назад, обнаружил в сосудах мозга и оболочек кристаллы, напоминающие кристаллы оксалата кальция.
Результаты ХТА позволили установить сочетанное отравление несколькими веществами
При проведении химического анализа одного из "ликеров": реакция с гидроксидом меди (II) дает синее окрашивание и при действии окислителя образуется щавелевая кислота (Токсикант1).
При проведении химического анализа другого "ликера" было установлено, что в этой жидкости помимо Токсиканта 1 имеется и Токсикант 2. Токсикант 2 - это газообразное вещество, способное к полимеризации при низкой температуре и к реакции дисмутации в водных растворах.
Лаборатория оснащена по стандарту GLP современными приборами для проведения химико-токсикологического анализа. Выбор оптимальных методов анализа за Вами.
Какой способ выбранного Вами метода количественного анализа токсикантов Вы можете предложить?
Напишите схемы химических реакций, лежащих в основе химического метода анализа на обнаруженные токсиканты.
Решение
Для проведения СХЭ при исследовании внутренних органов, тканей и биологических жидкостей трупов требуется письменное постановление следователя (или судебно-следственных органов) или направление судмедэксперта. На экспертизу вместе с вещественными доказательствами направляют постановление органов дознания или следствия о назначении экспертизы; выписку из акта судебно-медицинского исследования трупа; копию карты стационарного больного. При повторных экспертизах направляют заверенную копию первичного "Акта судебно-химического исследования" (или заключения эксперта). Эксперт судебно-химического отделения знакомится со всеми сопроводительными документами и характеристиками поступающих объектов. Все данные о вещественных доказательствах регистрируются в регистрационном и рабочем журналах. Экспертиза от начала и до конца должна производиться одним лицом. При необходимости экспертиза или исследование могут производиться несколькими специалистами, что отражается в акте.
Нормативные документы, регламентирующие проведение экспертизы.
Федеральный закон от 31 мая 2001 г. № 73 - ФЗ " О государственной судебно-экспертной деятельности в Российской Федерации" (с изменениями от 30 декабря 2001 г.)
Приказ Минздравсоцразвития РФ от 12.05.2010 N 346н "Об утверждении Порядка организации и производства судебно-медицинских экспертиз в государственных судебно-экспертных учреждениях Российской Федерации"
Перед СХЭ составляется план, в котором указывается метод исследования, методики определения яда и регламентируется расход материала. Экспертиза ведется в установленные "Правилами..." сроки, т. е. в течение 30 суток. По результатам экспертизы составляют документы (в двух экземплярах): "Акт судебно-химического исследования" (если направление на экспертизу проводил судмедэксперт) или "Заключение эксперта" (если экспертиза проводилась на основании постановления органов дознания). "Акт СХЭ" состоит из вводной части, описания объектов исследования, исследовательской части и выводов. Содержание "Заключения эксперта" регламентируется приказом № 346 МЗСР РФ, а также статьей 191 Уголовно-процессуального кодекса (УПК) РФ. В Ст. 190 УПК указано, что следователь вправе присутствовать при производстве экспертизы. При составлении "Заключения эксперта" судебно-медицинский эксперт-химик подписывается в том, что в соответствии со статьей 307 УК РФ и 81 УЦПК РФ он несет административную и уголовную ответственность за отклонение или отказ от проведения экспертизы или заведомо ложные результаты экспертного исследования.
При подозрении на отравление ядовитым веществом в судебно-медицинскую лабораторию направляют комплекс внутренних органов: желудок с содержимым, один метр тонкой кишки из наиболее измененных отделов, одну треть печени, одну почку, а также всю мочу и не менее 200 мл крови. Каждый орган, кровь, мочу помещают в отдельные чистые и сухие стеклянные банки. Судебно-химическая экспертиза должна быть начата в день поступления объектов в лабораторию.
Исследуемый объект, после того как произведен наружный осмотр его, отмечены внешний вид и запах, а также проверена реакция среды по универсальному индикатору, смешивают с дистиллированной водой до густоты кашицы и помещают в круглодонную колбу, заполняя последнюю не более чем на 1/3 ее объема. Колбу с объектом закрепляют в штативе, предварительно обернув полоской бумаги ее горло, глубоко погружают в холодную водяную баню и закрывают пробкой так, чтобы конец стеклянной трубки, вводящей пар, доходил почти до дна колбы. Когда прибор подготовлен (все части его, за исключением парообразователя, соединены), парообразователь нагревают, доводя воду почти до кипения. Затем объект подкисляют виннокаменной или щавелевой кислотой по лакмусу до рН=2,0-2,5 и быстро закрывают пробкой. После этого парообразователь присоединяют к колбе с объектом и продолжают нагревать сначала парообразователь, а затем и водяную баню, в которой находится колба с объектом исследования. Дистилляция производится по возможности медленно, так, чтобы можно было считать капли в приемнике. Это до-стигается регулированием пламени горелок.

1-парообразователь, 2-колба с объектом исследования, 3-баня водяная, 4-холодильник шариковый, 5-приемник дистиллята.
Первую порцию дистиллята собирают в количестве 3 мл в 2 мл 5% раствора едкой щелочи, для чего конец форштосса вводят в приемник таким образом, чтобы он был погружен в щелочь, находящуюся в нем. Второй и третий дистилляты собирают в приемники без едкой щелочи в количестве 25 мл каждый. По окончании перегонки весь первый дистиллят исследуют па наличие синильной кислоты, остальные дистилляты на другие токсикологически важные вещества. В процессе исследования дистилляты хранят в закрытых пробками колбах.
При необходимости проведения количественного определения того или иного вещества отгонку дистиллята ведут до полного его изолирования из биологического материала, что узнается по получению отрицательного результата качественных реакций на это вещество (при исследовании последней порции дистиллята). В ряде случаев при специальном исследовании объекта на то или иное вещество с количественным его определением возможна дополнительная отгонка вещества и новой навески биологического материала.
По результатам ХТА установлено сочетанное отравление несколькими веществами. При проведении химического анализа одного из "ликеров": реакция с гидроксидом меди (II) дает синее окрашивание и при действии окислителя образуется щавелевая кислота (Токсикант 1) отсюда следует, что это этиленгликоль. При проведении химического анализа другого "ликера" было установлено, что в этой жидкости помимо Токсиканта 1 имеется и Токсикант 2. Токсикант 2 - это газообразное вещество, способное к полимеризации при низкой температуре и к реакции дисмутации в водных растворах следует предположить, что это формальдегид.
Формальдегид - газообразное вещество. Формалин - 40% раствор фор-мальдегида в воде, бесцветная прозрачная жидкость с резким удушливым запахом. Смешивается с водой и спиртом во всех отношениях. Формальдегид способен к полимеризации, особенно при храпении в помещениях с низкой температурой. При этом образуется полимер формальдегида - пара формальдегид или параформ. Из биологического материала при химико-токсикологических исследованиях формальдегид изолируют дистилляцией с водяным паром. При значительных количествах формальдегида дистиллят обладает характерным удушливым запахом. При наличии значительных количеств формальдегида, что может иметь место при недопустимом консервировании им объектов исследования, необходимо тщательно пересмотреть все материалы дела, даже запросить о способе консервирования, а по окончании анализа отметить возможные последствия неправильного консервирования. Границей отгонки является 60-65 мг формальдегида при исследовании 100 г трупного материала. Прием формальдегида внутрь (в большинстве случаев ошибочный) вызывает слюнотечение, жжение и боли в подложечной области, тошноту, рвоту, понос. В результате всасывания формальдегида наблюдаются потеря сознания, судороги, угнетение нервных центров, раздражение почек.
В случаях летального исхода при вскрытии находят гиперемию слизистой оболочки желудка, острый гастрит, энтерит, при приеме больших количеств формальдегида - ожог, струпья и язвы на слизистой оболочке желудка.
Введенный внутрь формальдегид выделяется частично в неизмененном состоянии, большая часть его окисляется до муравьиной кислоты, затем до углекислоты и воды.
Качественное обнаружение
1)Реакция с хромотроповой кислотой (реакция имеет отрицательное судебно-химическое значение). При взаимодействии формальдегида с хромотроповой кислотой (1,8-диоксинафталином-3,6-дисульфокислотой) концентрированная серная кислота одновременно является водоотнимающим средством и окислителем. Вначале серная кислота вызывает конденсацию формальдегида с хромотроповой кислотой, а затем окисляет образовавшийся продукт конденсации.

Методика. В пробирку вносят 1 мл исследуемого раствора, 0,2 мл 1%-го раствора хромотроповой кислоты в концентрированной серной кислоте, 5 мл концентрированной серной кислоты и взбалтывают. Появление фиолетовой или красно-фиолетовой окраски указывает на наличие формальдегида в исследуемом растворе.
Предел обнаружения: 1 мкг формальдегида в пробе.
Не дают этой реакции альдегиды уксусной, пропионовой, масляной кислот, хлоралгидрат и другие. Эту реакцию дают вещества, которые при гидролизе, дегидратации или окислении образуют формальдегид.
2)Реакция с резорцином (реакция имеет отрицательное судебно-химическое значение). Формальдегид реагирует с резорцином в таутомерной форме (кетоформе) с образованием окрашенного соединения:

Методика. В пробирку вносят 1 мл исследуемого раствора и 1мл 1%-го раствора резорцина в 10%-м растворе едкого натра. Смесь нагревают в течение 5-ти минут на водяной бане. Появление розовой или малиновой окраски указывает на наличие формальдегида.
Эту реакцию дают уксусный альдегид, акролеин, фурфурол и другие.
3)Реакция с кодеином в концентрированной серной кислоте.
При нагревании формальдегида с кодеином в присутствии концентрированной серной кислоты появляется синяя окраска. Эта реакция основана на том, что под влиянием концентрированной серной кислоты от кодеина отщепляется метоксильная группа, в результате чего образуется морфин, содержащий фенольную группу. При взаимодействии морфина с формальдегидом появляется синяя окраска.
Методика. В фарфоровую чашку вносят 1 мл исследуемого раствора и прибавляют 5 мл концентрированной серной кислоты. После охлаждения жидкости прибавляют 0,02-- 0,03 г кодеина. При наличии формальдегида сразу или через 5--10 мин появляется сине-фиолетовая или красно-фиолетовая окраска.
Предел обнаружения: 0,02 мкг формальдегида.
4) Реакция с фуксинсернистой кислотой (реакция имеет отрицательное судебно-химическое значение). Фуксинсернистая кислота (реактив Шиффа) с формальдегидом дает синюю или сине-фиолетовую окраску. Эта кислота с альдегидами образует хиноидный краситель розового цвета.

+ 2НСОН =

Методика. В пробирку вносят 1 мл исследуемого раствора и 2-3 капли концентрированной серной кислоты. Содержимое пробирки взбалтывают и охлаждают проточной водой, затем прибавляют 1 мл раствора фуксинсернистой кислоты. Появление сине-фиолетовой или красно-фиолетовой окраски указывает на наличие формальдегида.
Раствор может окрашиваться не сразу, а через 10-15 минут. Окраска может появляться не только под влиянием формальдегида, но и под влиянием окислителей (хлор, оксиды азота, кислород воздуха и другие). Поэтому появление окраски через 30 мин после прибавления реактивов не должно рассматриваться как положительный результат на формальдегид.
Эта реакция не специфична для обнаружения формальдегида. Ее дают ацетальдегид, нитробензальдегид и др. Не дает указанной окраски хлоралгидрат. В сильно кислой среде (рН 0,7) с фуксинсернистой кислотой реагирует только формальдегид.
5)Реакция восстановления ионов серебра. Из аммиачного раствора солей серебра формальдегид выделяет металлическое серебро:

Методика. В хорошо очищенную от жира пробирку вносят 5 капель 1%-го раствора нитрата серебра и по каплям прибавляют 10%-й раствор аммиака до растворения образовавшегося осадка гидроксида серебра. К полученному раствору прибавляют 1 мл исследуемого раствора, а затем смесь осторожно нагревают на пламени горелки. При наличии формальдегида происходит реакция образования "серебряного зеркала". Эта реакция успешно протекает при рН 8-9. Нагревание пробирки должно быть умеренным. При высокой температуре "серебряное зеркало" не образуется, а выпадает бурый осадок серебра.
Данную реакцию дают и некоторые другие восстанавливающие вещества
Этиленгликоль.
Этиленгликоль - двухатомный спирт, бесцветная, сиропообразная, сладковатая жидкость, без запаха. Температура кипения - 195°С. Хорошо растворяется в спирте, воде, ацетоне, плохо в эфире и жирах Этиленгликоль и его производные (целлозольфы, карбитолы) используются в качестве антифризов, тормозных и технических жидкостей. Вследствие доступности в быту возможны тяжелые отравления этиленгликолем, антифризами, тормозными жидкостями, растворителями. Обычно эти жидкости принимают во внутрь вместо алкогольных напитков. Примерно половина пострадавших в момент приема знали, что пьют техническую жидкость, так как существует ошибочное мнение, что они изготовлены на основе спирта. Смертельная доза этиленгликоля от 25- 30 до 100-150 мл. По характеру действия его относят к нервно-сосудистым и протоплазматическим ядам. В организме этиленгликоль окисляется в гликолевый альдегид, гликолевую кислоту, а затем в щавелевую кислоту, которая в виде оксалата кальция поражает в первую очередь печень и почки. Умирают от острой почечно - печеночной недостаточности, токсической дистрофии печени. На судебно-химическое исследование поступают печень, почка, мозг, желудок с содержимым, моча, остатки жидкости. При длительном лечении (более 5-6 суток) и смерти этиленгликоль может быть обнаружен только в виде оксалата кальция.
Этиленгликоль может поступать в организм через пищевой канал и кожу. В связи с малой летучестью этиленгликоля только незначительные количества его могут поступать в организм с вдыхаемым воздухом. После поступления этиленгликоля в организм он действует как сосудистый и протоплазматический яд, подавляющий окислительные процессы и вызывающий дегенеративные изменения сосудов.
Метаболизм этиленгликоля является сложным. Основной путь метаболизма этого препарата состоит в том, что он окисляется до альдегида гликолевой кислоты НО-СН2-СНО, который дальше окисляется до гликолевой кислоты НО-СН2- СООН, разлагающейся на оксид углерода (IV) и муравьиную кислоту. Часть этиленгликоля в организме превращается в щавелевую кислоту, которая может быть причиной повреждения почек в результате отложения оксалатов в почечных канальцах. Оксид углерода (IV), как метаболит этиленгликоля, выделяется из организма с выдыхаемым воздухом. Остальные метаболиты и часть неизмененного этиленгликоля выделяется из организма с мочой. Этиленгликоль перегоняется с водяным паром.
Выделение этиленгликоля из биологического материала. Метод выделения этиленгликоля из объектов химико-токсикологического анализа предложен Н. Б. Лапкиной и В. А. Назаренко. Этот метод основан на использовании бензола как селективного переносчика этиленгликоля из объектов в дистиллят. Бензол совместно с парами этиленгликоля и небольшим количеством водяного пара переносится в дистиллят. Вода, которая перегоняется при этом, практически содержит весь этиленгликоль.
На исследование берут печень трупа, в которой после отравления содержится больше этиленгликоля, чем в других органах. При острых отравлениях этиленгликолем исследованию подвергают и желудок с содержимым. Для изолирования этиленгликоля пользуются аппаратом, представленным на рисунке.

1-круглодонная колба, 2-приспособление для улавливания воды, 3-колодильник
К 10 г печени или содержимого желудка прибавляют 5 г кристаллической щавелевой кислоты, смесь растирают до получения тонкой кашицы, переносят в круглодонную колбу вместимостью 100 мл и прибавляют 50 мл бензола. Колбу закрывают вертикально поставленным холодильником 3, снабженным приспособлением 2 для улавливания воды. Затем колбу устанавливают на водяную баню и нагревают. Пары бензола и увлекаемые им вода и этиленгликоль конденсируются в холодильнике и попадают в специальное приспособление. Поскольку в этом приспособлении (насадке) бензол (плотностью 0,879) находится сверху воды, он стекает в колбу. Вода и находящийся в ней этиленгликоль остаются в насадке. После окончания отгонки разбирают прибор и пипеткой из насадки отбирают необходимое для анализа количество жидкости.
Обнаружение этиленгликоля. Для обнаружения этиленгликоля применяют цветные и микрокристаллоскопические реакции.
)Реакция окисления этиленгликоля периодатом и обнаружение образовавшегося формальдегида. В результате указанной реакции образуется формальдегид, который затем можно обнаружить при помощи соответствующих реакций.
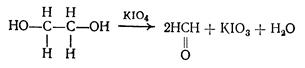
Методика. К 3-5 мл дистиллята прибавляют 5 капель 12%-го раствора серной кислоты, 5 капель 5%-го раствора периодата калия в 5%-м растворе серной кислоты и взбалтывают. Далее определяют выделившийся в результате реакции формальдегид.
- 2)Окисление этиленгликоля азотной кислотой и обнаружение щавелевой кислоты. При многократном выпаривании этиленгликоля с азотной кислотой образуется щавелевая кислота, которая с солями кальция образует кристаллы оксалата кальция, имеющие характерную форму. Эти кристаллы в ряде случаев могут появляться через 2-3 суток. 3)Реакция с сульфатом меди. От прибавления сульфата меди и щелочи к этиленгликолю образуется соединение, имеющее синюю окраску:

Методика. К 2-3 мл исследуемого раствора прибавляют 1-2 мл 10%-го раствора гидроксида натрия и несколько капель 10%-го раствора сульфата меди. Появление голубой окраски указывает на наличие этиленгликоля в растворе
Количественное определение формальдегида и этиленгликоля. Газо-жидкостная хроматография.
Газохроматографический анализ для этиленгликоля проводится в особых условиях, так как он имеет высокую температуру испарения и для его определения необходим программированный режим температуры. Формальдегид не требует особых условий расчет проводится по площади пика на хроматограмме в качестве внутреннего стандарта используют н - пропиловый спирт. В процессе хроматографического исследования компоненты разделяемой смеси перемещаются по колонке с током инертного носителя. Разделяемая смесь распределяется между газом носителем и нелетучим растворителем (неподвижной жидкой фазой), нанесенной на инертный носитель. В соответствии с коэффициентом распределения компоненты анализируемой смеси селективно и по-разному удерживаются неподвижной жидкой фазой до тех пор, пока не образуют отдельные полоски или хроматографические зоны. Эти полоски соответствуют отдельным компонентам разделяемой смеси, которые и регистрируются детектором. Современная система газохроматографисеского анализа основывается на детектировании исследуемых веществ с помощью масс-спектрометра, объединенного с газовым хроматографом с целью определения молекулярной массы, а в последнем случае - молекул структуры выходящих из колонки компонентов.
Подготовка проб для проведения газохроматографического анализа.
- 1. Дистилляция (простая перегонка) 2. Дериватизация
В настоящее время разработаны и используются методы прямого газохроматографического анализа " летучих " ядов, которые предполагают исследование равновесной парогазовой фазы или непосредственно ввод объекта в хроматограф. Метод прямого газохроматографического анализа более экономичен, чем этилнитритный, не требует расходования больших количеств реагентов. По затратам времени не отличается от этинилнитритного. При его использовании исключается загрязнение воздуха рабочих помещений вредными газами. С помощью обоих методов получаются весьма близкие результаты, отличающиеся не более чем на 10%. Не отмечается также отрицательного влияния продуктов гнилостного превращения биологического материала.
Похожие статьи
-
Задачи и методы количественного анализа - Основы аналитической химии
Количественный анализ - это совокупность химических, физико-химических и физических методов определения количественного соотношения компонентов, входящих...
-
Задачи и методы качественного анализа - Основы аналитической химии
Обнаружение или, как иногда говорят, "открытие" отдельных элементов или ионов, входящих в состав веществ - это задачи качественного анализа. Качественный...
-
Основные задачи анализа временных рядов. Базисная цель статистического анализа временного ряда заключается в том, чтобы по имеющейся траектории этого...
-
Изолирование пестицидов из биологических материалов наиболее часто осуществляется экстракцией различными органическими растворителями: пентан, н-гексан,...
-
Основные задачи анализа временных рядов - Динамические ряды
Принципиальные отличия временного ряда от последовательности наблюдений, образующих случайную выборку, заключаются в следующем: Во-первых, в отличие от...
-
Общие вопросы Привести объекты судебно-химического (химико-токсикологического) анализа. Дать понятие "вещественным доказательствам". Значение наружного...
-
Вариации коэффициентов целевой функции ЗЛП приводят к изменению направления вектора градиента. Так как при этом не затрагивается допустимое множество, то...
-
Алгоритм использует в качестве исходных данных документы, содержащие следующие сведения: X A, k,j, i - измеряемые показатели научной работы; X A, TG,...
-
Отбор пробы воды следует рассматривать как стадию, в значительной степени определяющую правильность последующего анализа, причем ошибки, допущенные в...
-
В России процесс окисления этиленгликоля с получением глиоксаля в промышленных масштабах не реализован, что обусловлено отсутствием соответствующих...
-
Методы анализа - Свойства флавоноидов
Качественное определение. Для обнаружения флавоноидов в ЛРС используют химические реакции и хроматографию. Химические реакции подразделяются на цветные и...
-
Особенности анализа органических соединений
Особенности анализа органических соединений: - Реакции с органическими веществами протекают медленно с образованием промежуточных продуктов. -...
-
Исследуемый раствор пропускают через колонку с катионитом. При последующем промывании колонки раствором едкой щелочи амфотерные металлы вымываются,...
-
Качественные методы анализа - Разработка технологической схемы получения анизола и крезола
Рециркуляционных реакционно-ректификационных процессов. При анализе сложных ХТС, характеризующихся большим числом параметров и переменных необходимо...
-
Количественный анализ - это совокупность, химических, физико-химических и физических методов определения количественного соотношения компонентов,...
-
Минимальное остовное дерево в связанном взвешенном неориентированном графе-это остовное дерево данного графа, в котором сумма весов, входящих в него...
-
Метод дихотомии требует менее всего итераций цикла для получения корней уравнения с заданной точностью. Если расчет ведется без помощи ЭВМ, то это...
-
Організаційна структура підприємства ЗАТ "Годинникар" є юридичною особою і діє на підставі статуту і законодавства України. Підприємство створено...
-
Ограничение чувствительность задача программирование Вариации правых частей ограничений приводят к изменению области допустимых решений ЗЛП, в действии...
-
Постановка задачи регрессионного анализа - Основы научных исследований
Основное назначение Регрессионного анализа (РА) - получение по экспериментальным данным зависимостей, аппроксимирующих эти данные в виде алгебраических...
-
В современных условиях повышается самостоятельность предприятий в принятии и реализации управленческих решений, их экономическая и юридическая...
-
Корреляционный статистический регрессионный Исходные данные: N 1 2 3 4 5 6 7 8 9 10 XI 15 16 19 23 25 26 29 34 38 49 YI 4 15 10 13 18 20 19 17 26 33 На...
-
Регрессия -- зависимость среднего значения какой-либо величины от некоторой другой величины или от нескольких величин. Задача регрессионного анализа...
-
Обычно, для различных интервалов энергий используют разные типы установок, которые предназначены для измерения спектров нейтронов методом времени...
-
Адсорбционные методы исследования свойств поверхности позволяют количественно охарактеризовать происходящие при адсорбции межмолекулярные взаимодействия,...
-
Моделирование. Детерминизм. Требования к моделированию В процессе исследования объекта часто бывает нецелесообразно или даже невозможно иметь дело...
-
Адсорбционные явления чрезвычайно широко распространены в живой и неживой природе. Толщи горных пород и почвы являются огромными колоннами с...
-
В общем случае все этапы кластерного анализа взаимосвязаны, и решения, принятые на одном из них, определяют действия на последующих этапах. Аналитику...
-
Итеративная кластеризация в SPSS - Кластерный анализ
Обычно в статистических пакетах реализован широкий арсенал методов, что позволяет сначала провести сокращение размерности набора данных (например, при...
-
Полярографический метод анализа
Полярография -- метод качественного и количественного химического анализа, основанный на получении кривых зависимости величины тока от напряжения в цепи,...
-
Выполнение реакции. В делительную воронку вносят 0,1 мл раствора исследуемого вещества, прибавляют 0,2 мл 0,1%-го раствора родамина 6Ж и 1мл...
-
Запасы этих растворов, несоответствующих показателям качества, исчисляются сотнями тысяч тонн и дальнейшее их хранение становится очень опасным для...
-
Время, отведенное на лекции - 2 часа. Цель лекции: Формирование знаний студентов об осадительном титровании, классификация методов титрования и...
-
Получение синтезированного газа - Анализ и технологическая оценка химического производства
Химические методы переработки нефти проводят при высоких температурах без катализатора (термический крекинг), при высоких температурах в присутствии...
-
Существуют разработки метода синтеза глиоксаля озонированием бензола эквивалентным количеством озона с дальнейшим гидрированием получаемых продуктов для...
-
МЕТОДЫ СРАВНИТЕЛЬНОГО ШКАЛИРОВАНИЯ - Многомерный статистический анализ
Шкалирование методом попарного сравнения - Это метод сравнительного шкалирования, при котором респонденту дается два объекта для выбора по определенному...
-
Методы анализа взаимосвязи - Статистическое изучение взаимосвязи социально-экономических явлений
Первым и обязательным этапом изучения взаимосвязи социально-экономических явлений является качественный анализ природы явления методами экономической...
-
Полимеризация двуокиси азота. Переработка нитрозных газов в азотную кислоту обычно происходит при температурах от О до 50 °С. В этих условиях двуокись...
-
Газовая хроматография - Основы качественного анализа
Этот метод представляет собой замечательное сочетание методов разделения и количественного анализа, поддающееся полной автоматизации. Смесь газов или...
-
Объемный (титриметрический) анализ, Нейтронно-активационный анализ - Основы качественного анализа
Это один из традиционных химических методов анализа. Для него нужно иметь раствор с точно известной концентрацией вещества, взаимодействующего с...
Ситуационная задача № 1 - Химико-токсикологический анализ органов трупа