Химическая технология как наука
Внешняя диффузная область протекания гетерогенного процесса в системе газ/твердое вещество.
Для расчета скорости процесса в системе газ/твердое вещество представим, что сферическая частица обдувается газовым потоком, движущимся со скоростью W.

Rs - радиус частицы.
Поскольку частица имеет шероховатую поверхность, вокруг частицы существует практически неподвижный пограничный слой газа, который оказывает основное сопротивление процессу диффузии газообразного реагента к поверхности твердой фазы. Толщина этого пограничного слоя - д, концентрация газообразного компонента на внешней поверхности пограничного слоя такая же, как и в ядре потока. Концентрация компонента на поверхности частицы ZBs.
Скорость процесса в области внешней диффузии (Uкд) (область конвективной диффузии) мы можем определить, используя первый закон Фика

Произведение коэффициента диффузии на отношение разности концентрации газообразного компонента и толщины пограничной пленки.
Отношение коэффициента диффузии к толщине пограничной пленки называется коэффициентом массоотдачи в области конвективной диффузии

Исходя из этих соотношений, мы можем сказать, что скорость гетерогенного процесса, протекающего в области конвективной диффузии, определяется природой газообразных компонентов, концентрацией газообразных компонентов и линейной скоростью подачи реагентов. Поскольку, именно линейная скорость подачи реагентов определяет величину толщины пограничной пленки.
Среди всех факторов, которые мы перечислили, наиболее существенно влияющим является линейная скорость подачи реагентов и основным управляющим фактором, применимым в области конвективной диффузии является скорость подачи реагентов.
Окончательно мы получаем

От этого уравнения нет толка, потому что ZBs неопределима, поэтому здесь говорят, что как только молекула газа достигла твердой частицы, наступает химическая реакция. Скорость химического превращения на несколько порядков выше, чем Uкд и получается тогда

ZB - концентрация газа в ядре газового потока.
Наше допущение позволяет рассчитать время полного превращения если процесс протекает в области конвективной диффузии, т. е. используется правило: какое количество газа подошло к поверхности твердой частицы, такое же количество твердого вещества и вступило во взаимодействие.
Соответственно скорость может быть выражена

Изменение массы вещества отнесенное к площади поверхности контакта фаз и промежутку времени в течение которого происходит это взаимодействие

Уравнение позволяет связать время обработки материала (ф), исходный радиус частицы Rs и радиус непрореагировавшей части или радиус непрореагировавшего ядра.




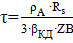
в области внешней диффузии
На интенсивность протекания процесса во внешней диффузионной области помимо ранее перечисленных факторов оказывает влияние и размер обработанных частиц.
Внутренняя диффузная область протекания гетерогенного процесса в системе газ/твердое вещество.
Основное сопротивление процессу во внутренней диффузной области сосредоточено при транспорте реагентов через слой продукта реакции, образующегося на поверхности твердой частицы.


Скорость процесса, протекающего во внутренней диффузной области, будет определяться концентрацией компонента на поверхности твердой частицы и размерам исходных твердых частиц.
Коэффициент диффузии во многом определяется пористой структурой слоя продукта, поскольку при прохождении через слой продукта молекулы газовых реагентов сталкиваются не только между собой, но и со стенками пор. Определяющим фактором управления при протекании процесса во внутридиффузной области является размер обработанных частиц.


не применяется для реальных реакций
При проведении процессов в кипящем слое внутридиффузная область практически никогда не наступает, потому что слой продукта механически удаляется с поверхности, и в химическую реакцию постоянно вступает обновленная поверхность твердой частицы, образующая более мелкие дисперсные частицы.
Как только молекула газового реагента подошла в поверхности раздела фаз она сразу вступает в химическую реакцию и, следовательно, его концентрация на поверхности раздела фаз равна 0.
И тогда получаем
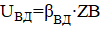
Формула позволяет определить скорость процесса, протекающего во внутридиффузной области.
И, используя методику, которую мы применяли для области конвективной диффузии, определить время полной обработки твердого материала

Основной момент: время полной обработки зависит от RS2, именно поэтому размер обработанных частиц является основным управляющим параметром. Граница раздела фаз меняется по времени.
Кинетическая область протекания гетерогенного процесса в системе газ/твердое вещество.
Ввиду сложного разделения под кинетической областью протекания гетерогенного процесса понимают этапы его протекания от адсорбции до химического взаимодействия, поэтому

Произведение константы скорости поверхностной химической реакции на концентрацию газообразного компонента на поверхности раздела фаз в степени порядка реакции(б) по этому компоненту. Соответственно, порядок реакции учитывает торможение, которое может возникнуть на стадии адсорбции, растворения в твердом веществе и диффузии к активному центру образования ядра новой фазы.
Есть противоречия:
Если б=1, можно вывести общее уравнения для скорости гетерогенного процесса. Используя правило, что независимо от лимитирующей стадии скорость всех стадий численно равно скорости самой медленной стадии и тогда:
U=kM-ZB
Произведение коэффициента массопередачи на концентрацию газообразных компонентов в ядре газового потока. При этом:

При этом очевидно, что если основное сопротивление массопередаче сосредоточено, либо в области КД, либо в области ВД, то коэффициент массопередачи будет практически численно равен

Вопрос. Хорошо ли будет для проведения процесса, если линейная скорость настолько велика, что
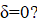
Плохо, так как при бесконечно большой UКД скорость химической реакции меньше и то количество исходных газообразных реагентов, которые подошли к поверхности раздела фаз, не успевает прореагировать, в результате степень превращения твердого вещества будет незначительна.
Этот факт хорошо показать на термообработке в кипящем слое, он существует в определенном диапазоне скоростей газового потока. Нижний предел - скорость начала взвешивания (WН. В). Верхний предел - скорость начала пневмотранспорта (WУ),уноса. Твердое вещество не реагирует на то, что его вынесло потоком из рабочей камеры.
Увеличивается коэффициент массопередачи, снижается время контакта.

Похожие статьи
-
Теоретические основы процесса Реакторы смешения - это емкостные аппараты с мешалкой или циркуляционным насосом. Человечество давно пользуется...
-
ХИМИЧЕСКАЯ КИНЕТИКА И ХИМИЧЕСКОЕ РАВНОВЕСИЕ - Неограническая химия
Задание 4.1: 4.1.1. Проанализируйте данную Вам реакцию (табл. IV.1) и укажите, какой она является: гомогенной или гетерогенной. 4.1.2. Запишите...
-
Скорость реакции определяется изменением молярной концентрации одного из реагирующих веществ: V=dC/dtV. Факторы, влияющие на скорость химических...
-
Автору кажется, что логично было бы начать изложение с термодинамики, и лишь потом на ее основе рассматривать кинетику и равновесия: если реакция...
-
Рассмотрим реакцию между веществами А и В, протекающую по схеме: А А + в В = с С + d D Количественно зависимость между скоростью реакции и концентрациями...
-
Кинетика химических реакций - Концепции современного естествознания: химическая составляющая
Одна из особенностей химических реакций заключается в том, что они протекают во времени. Одни реакции протекают медленно, месяцами, как, например,...
-
В предыдущих разделах рассмотрены отдельные аспекты кинетики, а теперь пора подвести общие итоги: от чего зависят скорости реакций и как можно ими...
-
Общие понятия и определения. Термодинамический и кинетический критерий реакционной способности химической системы. Скорость химической реакции. Факторы,...
-
Принцип Ле Шателье - Систематика химических элементов
Химическое равновесие, отвечающее равенству скоростей прямой и обратной реакций и минимальному значению энергии Гиббса (G0Т=0), является наиболее...
-
Исходные данные для расчета реакторов - Проектирование химического реактора идеального смешения
При выборе конструкции и определении размеров реактора необходимо принимать во внимание различные факторы и, прежде всего, располагать данными о скорости...
-
Краткая теория Основное уравнение гомогенной кинетики - закон действующих масс, ЗДМ (хотя реально подставляются не массы, а молярные концентрации):...
-
Реагенты Продукты, Все химические реакции обратимы, Вопросы - Химическое равновесие
Все химические реакции обратимы Это означает, что в реакционной смеси протекает как взаимодействие реагентов, так и взаимодействие продуктов. В этом...
-
Актуальность темы. В современных условиях глобальной конкуренции на все более интегрирующихся мировых рынках, развитие химической промышленности...
-
Истинное и ложное равновесие Все химические реакции в той или иной степени обратимы. Если возможна реакция aA + bB хХ + yY, то возможна и обратная...
-
Скорость химической реакции. Энергия активации химической реакции Химическая термодинамика изучает возможность, направление и пределы самопроизвольного...
-
Катализ - Концепции современного естествознания: химическая составляющая
Наиболее сильное влияние на скорость реакции оказывает присутствие в реагирующей системе Катализатора -- вещества, которое повышает (а иногда и уменьшает...
-
Общие сведения Гетерогенные реакции еще труднее для изучения, чем гомогенные, и в обычных учебниках общей химии им уделяется мало внимания, хотя они...
-
Химический состав морской воды - Химия воды
Вода как растворитель обладает свойством растворять различные вещества. Растворяющая способность воды определяется ее диэлектрической проницаемостью. Как...
-
Гомогенный и гетерогенный катализ - Систематика химических элементов
Вещества, увеличивающие скорость химической реакции, называются Катализаторами. Явление возрастания скорости реакции под действием таких веществ,...
-
Влияние разбавления раствора - Химическая кинетика, равновесия, термодинамика
Это, как и в предыдущем параграфе, изменение концентрации, но не одного вещества, а одновременно всех растворенных веществ. Допустим, что объем раствора...
-
Реакторами идеального (полного) смешения называются реакторы непрерывного действия, в которых осуществляется турбулентный гидродинамический режим. В них...
-
Необратимые и обратимые реакции. Химическое равновесие Когда при химическом взаимодействии хотя бы одно из веществ расходуется полностью, реакцию считают...
-
Закон действующих масс. Правило Вант-Гоффа - Систематика химических элементов
Скорость химической реакции зависит, прежде всего, от природы реагирующих веществ, а также от условий протекания реакции: концентрации, температуры,...
-
Стандартные методы, как правило, предусматривают использование количественного анализа, позволяющего установить точное содержание отдельных элементов и...
-
Процесс получения фосфорной кислоты, не смотря на крупнотоннажность производства и довольно длительное использование в различных сферах...
-
Химическая технология и тенденции ее развития - Этапы становления химии
Потребности общества породили химическую технологию. По выражению Бертло, химия начинает творить свой собственный объект исследования, создавая сотни...
-
Винилхлорид -- достаточно активное химическое соединение, чьи химические свойства определяются как наличием двойной связи, так и атома хлора. Наибольший...
-
Химия в содружестве с другими науками, дает обширный, фундаментальный материал для выработки ученого научно-философских взглядов на природу и окружающий...
-
Это самый распространенный вариант. В реакции твердое+твердое, твердое+жидкость или твердое+газ продукт образуется на поверхности раздела фаз, и если он...
-
Смещение химического равновесия. Принцип Ле-Шателье - Основы химии
Положение химического равновесия зависит от следующих параметров реакции: температуры, давления и концентрации. Влияние, которое оказывают эти факторы на...
-
Краткая теория В старом учебнике Глинки вопрос хорошо изложен на качественном уровне, но не хватает строго количественного описания влияния температуры...
-
Энтропия. Движущее начало химических процессов - Химическая термодинамика. Термохимия. Решение задач
Убедившись в полезности знания тепловых эффектов химических превращений, мы, тем не менее, не смогли ответить на вопрос: "Почему одни химические реакции...
-
Существует два основных способа получения полиарилатов: переэтерификация и взаимодействие хлорангидридов карбоновых кислот с двухатомными фонолами. 1....
-
Материальный баланс производства Основанием для получения уравнения реактора любого типа является материальный баланс, составленный по одному из...
-
Смещение равновесия Смещение равновесия - это изменение состояния равновесия (изменение равновесного соотношения количеств исходных веществ и продуктов)...
-
ТЕРМОХИМИЯ - Химическая термодинамика. Термохимия. Решение задач
Уравнения химических реакций, учитывающие тепловые эффекты, называются термохимическими уравнениями. Например: 2Н2(г.)+О2(г.) = 2Н2О(г.); ДН = - 476 кДж....
-
Теплота образования. Теплота сгорания. Следствия из закона Гесса - Систематика химических элементов
Теплотой образования называется тепловой эффект при образовании из простых веществ одного моль соединения. При этом теплота образования простых веществ...
-
Основы химической термодинамики. Первое начало термодинамики Термодинамические системы и термодинамические параметры. Функции состояния. Парциальные...
-
Введение - Химическая термодинамика. Термохимия. Решение задач
Химия изучает химическую форму движения материи, под которой понимают превращение одних веществ в другие. В результате химических процессов появляются...
-
Химическое равновесие - Скорость химических процессов. Химическое равновесие, принцип Ле-Шателье
Химическое равновесие и его признаки. Равновесие истинное и заторможенное (ложное). Принцип Ле-Шателье. Константа равновесия и ее связь с...
Химическая технология как наука