Кривые кондуктометрического титрования - Электрохимические методы анализа
В ходе титрования электропроводность будет заметно меняться, если вводить или удалять ионы с высокой подвижностью.
Чаще всего продуктом реакции является слабый электролит (кислотно-основное взаимодействие, комплексообразование) или малорастворимое соединение (реакция осаждения). Если принять это во внимание и воспользоваться табличными величинами л0, то можно спрогнозировать вид кривой титрования.
Вид кривых кондуктометрического титрования может быть различным. Он обусловлен следующими факторами.
1. Изменение числа ионов в титруемом растворе и числа зарядов в нем в ходе титрования.
Рассмотрим кривую титрования слабой одноосновной кислоты СН3СООН (титруемое вещество Х, находится в сосуде для титрования) раствором NaOH (титрант R, приливается из бюретки):
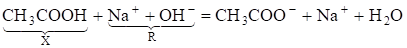
Как видно из уравнения реакции, в ходе титрования число зарядов увеличивается (исходное вещество - слабый электролит, среди продуктов есть два иона). Значит, электропроводность при титровании будет возрастать.
До начала титрования в растворе содержится мало ионов, т. к. СН3СООН слабо диссоциирует, поэтому значение ч должно быть невелико. В процессе титрования До т. э. образуется соль - сильный электролит. За счет этого в растворе появляются ионы СН3СОО - и Na+, причем по мере приближения к т. э. ионов становится больше. Следовательно, электропроводность будет возрастать. После т. э. при добавлении избытка титранта в растворе появляются ионы Na+ и очень подвижные ионы ОН - во все больших и больших количествах, поэтому ч будет возрастать более резко (рис. 15).
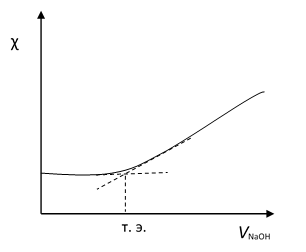
Рис. 15. Кривая кондуктометрического титрования слабой одноосновной кислоты СН3СООН раствором щелочи NaOH
2. Подвижность ионов, вступающих в реакцию и образующихся в ходе реакции.
В общем случае при титровании протекает реакция, в ходе которой образуется слабый электролит или малорастворимое соединение (МРС):
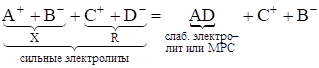
Как видно из уравнения реакции, в ходе титрования число зарядов в титруемом растворе не изменяется, их по два с каждой стороны.
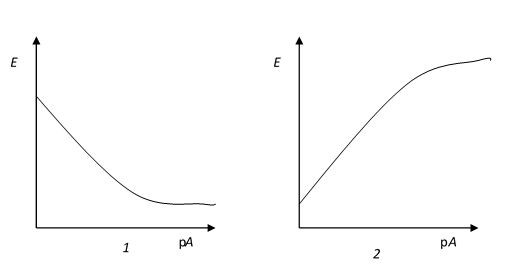
В этом случае ход кривой зависит от соотношения подвижностей ионов. Так, в процессе титрования До т. э. ионы А+, которые находились в растворе, связываются в молекулы слабого электролита или образуют малорастворимое соединение АD. С другой стороны, из бюретки в раствор поступает эквивалентное количество ионов С+. Электропроводность в ходе титрования До т. э. будет меняться следующим образом (рис. 16):
§ если, то ч уменьшается;
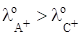
§ если, то ч остается постоянной;
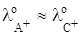
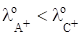
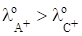
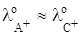
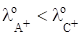
§ если, то ч увеличивается.
Рис. 16. Вид кривых кондуктометрического титрования в зависимости от соотношения подвижностей ионов
После т. э. во всех трех рассмотренных случаях электропроводность возрастает вследствие добавления избытка титранта - сильного электролита.
Похожие статьи
-
Кондуктометрическое титрование - Электрохимические методы анализа
Сущность метода заключается в том, что измеряют электрическую проводимость раствора в ходе титрования и строят кривую титрования. Кривая титрования...
-
Кондуктометрическое титрование - Электрохимические методы исследования
Несомненно, большими аналитическими возможностями обладает кондуктометрическое титрование. Титрование позволяет восполнить недостаток селективности...
-
Время, отведенное на лекции - 2 часа. Цель лекции: Формирование знаний студентов об осадительном титровании, классификация методов титрования и...
-
Эквивалентная электропроводность и подвижность ионов - Электрохимические методы анализа
Эквивалентная электропроводность ( Л ) - это электропроводность раствора, содержащего 1 моль экв электролита, измеренная при расстоянии между электродами...
-
Удельная электропроводность как аналитический сигнал - Электрохимические методы анализа
Удельная электропроводность (ч) - это электропроводность 1 см3 раствора, находящегося между электродами с площадью S = 1 см2 и расстоянием между ними L =...
-
Кривые титрования - Методы осаждения
Кривые титрования в аргентометрии обычно строят в координатах pAg -- V, Где pAg -- взятый с обратным знаком лога-рифм концентрации ионов Ag+, V -- Объем...
-
Теоретические основы кондуктометрического метода анализа - Электрохимические методы исследования
Кондуктометрические методы анализа основаны на измерении электропроводности исследуемых растворов. Существует несколько методов кондуктометрического...
-
Прямая кондуктометрия - Электрохимические методы анализа
Сущность метода Прямой кондуктометрии заключается в том, что концентрацию вещества определяют по результатам измерения электрической проводимости (или...
-
Методы кондуктометрии - Электрохимические методы исследования
Контактные методы. Измерения проводят с помощью контактных ячеек (рис. 3, а). При этом используют электроды из Pt, Ti, нержавеющей стали и др. Для...
-
Кондуктометрия, Основные узлы приборов - Электрохимические методы анализа
Кондуктометрия является старейшим, самым простым и наименее селективным из электрохимических методов анализа. Метод возник в 1885 г., когда Кольрауш...
-
Метод калибровочной кривой - Определение концентрации методом полярографии
Необходимо определить высоту волны данного иона в исследуемом растворе. Из приготовленного для анализа раствора берут аликвотную часть его и помещают ее...
-
Электрохимические методы анализа - Электрохимические методы анализа
Электрохимические методы анализа (ЭХМА) основаны на использовании процессов, которые протекают на поверхности электродов или в приэлектродном...
-
Это метод который нашел мировое применение для анализа лекарствнных средств. Он основан на свойстве галогенидов количественно осаждаться нитратом серебра...
-
Полярографический метод анализа
Полярография -- метод качественного и количественного химического анализа, основанный на получении кривых зависимости величины тока от напряжения в цепи,...
-
Методы анализа - Свойства флавоноидов
Качественное определение. Для обнаружения флавоноидов в ЛРС используют химические реакции и хроматографию. Химические реакции подразделяются на цветные и...
-
Классификация, Кривые осадительного титрования - Характеристика осадительного титрования
Наиболее широкое применение нашли следующие виды осадительного титрования: 1. Аргентометрия. Титрант - нитрат серебра, используется для количественного...
-
Вещество [Co] Лиганды и Комплексообразователь Координационное число 6 Для комплексов с координационным числом 6 характерно октаэдрическое расположение...
-
Количественный анализ - это совокупность, химических, физико-химических и физических методов определения количественного соотношения компонентов,...
-
Задачи и методы количественного анализа - Основы аналитической химии
Количественный анализ - это совокупность химических, физико-химических и физических методов определения количественного соотношения компонентов, входящих...
-
Элементы матричного анализа - Методы решения системы линейных уравнений
Вектором, как на плоскости, так и в пространстве, называется направленный Отрезок , то есть такой Отрезок , один из концов которого выделен и называется...
-
Пусть функция непрерывна в ограниченной замкнутой области S и требуется вычислить m-кратный интеграл . (1) Геометрически число I представляет собой...
-
Способ усреднения подынтегральной функции - Применение метода Монте-Карло в эконометрическом анализе
В качестве оценки определенного интеграла принимают , Где n - число испытаний; - возможные значения случайной величины X, распределенной равномерно в...
-
Задачи и методы качественного анализа - Основы аналитической химии
Обнаружение или, как иногда говорят, "открытие" отдельных элементов или ионов, входящих в состав веществ - это задачи качественного анализа. Качественный...
-
В настоящее время производственные методы получения формальдегида большим разнообразием не отличаются. Так, в реакциях восстановления СО и СО2 Водой...
-
Количественная характеристика трудовых ресурсов в первую очередь измеряется такими показателями, как общая, списочная, явочная и среднесписочная...
-
Неравенство Бонферрони часто используется при множественном тестировании на значимость, главная идея состоит в установке верхней границы FWER. Пусть -,...
-
Качественные методы анализа - Разработка технологической схемы получения анизола и крезола
Рециркуляционных реакционно-ректификационных процессов. При анализе сложных ХТС, характеризующихся большим числом параметров и переменных необходимо...
-
МЕТОДЫ СРАВНИТЕЛЬНОГО ШКАЛИРОВАНИЯ - Многомерный статистический анализ
Шкалирование методом попарного сравнения - Это метод сравнительного шкалирования, при котором респонденту дается два объекта для выбора по определенному...
-
Реагентный метод обессеривания - Сравнительный анализ методов обессеривания
Нефтеперерабатывающая промышленность в настоящее время использует химические и физико-химические методы очистки дизельного топлива от серасодержащих...
-
Химизм процесса гидроочистки - Сравнительный анализ методов обессеривания
Превращение серосодержащих соединений В неуглеводороных соединениях связи C-S и S-S менее прочны, чем связи С-С и С-Н, усредненные энергии связи которых...
-
Метод дихотомии требует менее всего итераций цикла для получения корней уравнения с заданной точностью. Если расчет ведется без помощи ЭВМ, то это...
-
ОПРЕДЕЛЕНИЕ МЕТОДА ФАКТОРНОГО АНАЛИЗА И ЧИСЛА ФАКТОРОВ - Многомерный статистический анализ
Определение метода факторного анализа. Различные методы факторного анализа различаются в зависимости от подходов, которые используются для выделения...
-
Способы улучшения качества дизельного топлива - Сравнительный анализ методов обессеривания
Специальные присадки Понижение содержания серы в дизельном топливе, как правило, приводит к уменьшению его смазывающих свойств, поэтому для дизельных...
-
Сера в дизельном топливе - Сравнительный анализ методов обессеривания
Сера и ее соединения в качестве естественной составляющей входят в состав сырой нефти в виде элементарной серы, сероводорода и различных органических...
-
Наиболее представительные ионы и соответствующие им структуры помещены в таблицы, их используют при интерпретации масс-спектров. Кроме того сравнивают...
-
В соответствии со вторым законом термодинамики элементарный акт флотации возможен, если свободная энергия Е2 системы после закрепления частицы на...
-
Следует отметить, что не существует особых сил, вызывающих адсорбцию. Адсорбция молекул на поверхности твердого тела происходит за счет сил притяжения со...
-
Методы непараметрической статистики - Основы теории систем и системного анализа
Использование классических распределений случайных величин обычно называют "параметрической статистикой" - мы делаем предположение о том, что...
-
Заключение - Электрохимические методы исследования
Кондуктометрия - совокупность электрохимических методов анализа, основанных на измерении электропроводности х жидких электролитов, которая...
-
Метод наименьших квадратов - Корреляционно-регрессионный анализ
Для определения коэффициентов уравнения регрессии b применяют разные методы (графический, метод средних), однако наибольшее распространение получил метод...
Кривые кондуктометрического титрования - Электрохимические методы анализа