Химизм процесса гидроочистки - Сравнительный анализ методов обессеривания
Превращение серосодержащих соединений
В неуглеводороных соединениях связи C-S и S-S менее прочны, чем связи С-С и С-Н, усредненные энергии связи которых равны 201, 218, 247 и 365 кДж/моль соответственно. Но поскольку процесс гидроочистки каталитический, то прочность связи следует оценивать с учетом энергии образования промежуточных комплексов катализатора с осколками, образовавшимися после разрыва связей. Эта энергия значительно компенсирует затрату энергии разрыва связи. Например, на никеле энергия разрыва связи C-S составляет 20 кДж/моль, С-N - 104 кДж/моль, а С-С - 201кДж/моль. Этим объясняется селективность процессов гидроочистки: почти количественная деструкция связей С-S без существенного затрагивания связей С-С, т. е. без заметной деструкции сырья.
Меркаптаны превращаются в углеводород и сероводород:
RSH + H2 RH + H2S
Сульфиды гидрируются через стадию образования меркаптанов:
RSR' R'SH R'H + H2S
Дисульфиды гидрируются до сероводорода и соответствующих углеводородов также через стадию образования меркаптанов:
RSSR' RSH + R'SH RH + R'H + 2H2S
В циклических сульфидах, например тиофане, вначале разрывается кольцо, затем отщепляется сероводород и образуется соответствующий углеводород:
CH3CH2CH2CH3 +H2S
Соединения тиофенового ряда представлены бензтиофеном, дибензтиофеном, алкилбибезтиофенами и диалкилдибензтиофенами - малоактивны. Их доля в составе серусодержащих соединений дизельных фракций достигает 50 - 60 %, что в пересчете на серу при общем ее содержании около 1,2 %(масс.) составляет 0,3 - 0,7 %(масс.). Устойчивость сераорганических соединений к гидрогенолизу с увеличением числа ароматических и нафтеновых колец в его молекуле возрастает.
Тиофен и бензтиофен сначала гидрируются до производных тетрагидротиофена, которые затем превращаются алканы и алкилпоизводные ароматических углеводородов:
CH3CH2CH(R)CH3 + H2S
+ H2S
Гидрогенолиз дибензтиофена происходит по схеме:

По реакции (1) гидрогенолиз дибензтиофена происходит преимущественно на алюмокобальтмолибденовом, а по реакции (2) и (3) - на алюмоникельмолибденовом катализаторе.
Превращение азотсодержащих соединений
Азот в нефтепродуктах находится в основном в гетероциклах - в виде производных пиррола и пиридина.
Гидрогенолиз связи C - N протекает труднее, чем связи C - S, поэтому в процессах гидроочистки азот удалить сложнее, чем серу. Легче всего гидрируются амины:
C6H5CH2NH2 C6H5CH3 + NH3
Анилин, содержащий аминогруппу, связанную с ароматическим кольцом, гидрируется значительно труднее:
C6H5NH2 C6H6 + NH3
Хуже всего удаляется азот из циклических структур. Пиррол гидрируется до бутана и аммиака:
CH3CH2CH2CH2NH2 CH3CH2CH2CH3 + NH3
Пиридин превращается в пентан и аммиак по схеме:
CH3CH2CH2CH2CH2NH2 CH3CH2CH2CH2CH3 + NH3
Так как сопряженная электронная система в молекуле пиридина значительно более устойчива, чем в молекуле пиррола, пиридин гидрируется труднее, чем пиррол.
Гидрирование бициклических и полициклических ароматических углеводородов начинается с кольца, содержащего гетероатом:
+ NH3
Превращение кислородсодержащих и металлоорганических соединений
Кислород в средних дистиллятах может быть представлен соединениями типа спиртов, эфиров, фенолов и нафтеновых кислот. В высококипящих фракциях кислород находится в основном в мостиковых связях и в циклах молекул. Наибольшее количество кислородсодержащих соединений концентрируется в смолах и асфальтенах.
При гидрогенолизе кислородсодержащих соединений образуются соответствующие углеводороды и вода:
RCOOH R CH3 + 2H2O
RC6H4OH RC6H5 + H2O
Смолы и асфальтены превращаются в низкомолекулярные соединения.
Гидроочистка от кислородсодержащих соединений протекает в тех же условиях, что и удаление сернистых примесей. В присутствии обычных катализаторов гидроочистки достигается практически полное гидрирование кислородсодержащих соединений.
Металлорганические соединения, присутствующие в нефтяных фракциях, разлагаются на активных центрах катализатора с выделением свободного металла, являющегося каталитическим ядом. Гидроочистка позволяет удалять большую часть металлорганических соединений. Так, ванадий удаляется на 98ч100%, а никель - 93ч96%.
Превращение углеводородов
В процессе гидроочистки одновременно с реакциями сернистых, азотистых и кислородных соединений протекают многочисленные реакции углеводородов:
Изомеризация парафиновых и нафтеновых углеводородов;
Насыщение непредельных углеводородов;
Гидрокрекинг;
Гидрирование ароматических углеводородов и другие.
Изомеризация парафиновых и нафтеновых углеводородов происходит при любых условиях обессеривания.
При температуре 350ч500°С происходит практически полное гидрирование непредельных соединений при сравнительно низком парциальном давлении водорода:
RCH = CH2 RCH2CH3
Интенсивность гидрокрекинга усиливается с повышением температуры и давления. При более высоких температурах и низких давлениях происходит частичное дегидрирование нафтеновых и дегидроциклизация парафиновых углеводородов. В некоторых случаях гидрогенизационного обессеривания эти реакции могут служить источником получения водорода для реакции собственного обессеривания, т. е. обеспечивают протекание процесса автогидроочистки.
В процессе гидрирования наиболее стойкими являются ароматические углеводороды. Гидрирование ароматических углеводородов с конденсированными кольцами может происходить в условиях процесса гидроочистки:
Наряду с последовательным гидрированием ароматических колец возможно расщепление образовавшихся насыщенных колец и выделение алкилзамещенных аренов:
+
+
Алкилбензолы на катализаторах с высокой гидрирующей активностью подвергаются дальнейшему гидрогенолизу, в основном с последовательным отщеплением метана:
Механизм и кинетика процесса гидроочистки
Механизм гидрирования сераорганических соединений в значительной степени зависит от их строения. Скорость гидрирования, в общем, возрастает в ряду: тиофены < тиофаны сульфиды < дисульфиды < меркаптаны.
Данных о гидрировании азот - и кислородорганических соединений очень мало. В таблице 4 приведены данные о гидрировании некоторых азот-, кислород - и сераорганических аналогов на Ni2S3 [4].
Таблица 4 - Степень превращения различных видов гетероатомных соединений в зависимости от температуры
|
Углеводород |
Превращение, % | ||
|
При 200С |
При 350С |
При 400С | |
|
Тиофан |
41 |
100 |
100 |
|
Тетрагидрофуран |
0 |
25 |
55 |
|
Тиофен |
0 |
15 |
39 |
|
Фуран |
0 |
0 |
10 |
|
Пиррол |
0 |
0 |
0 |
При одинаковом строении устойчивость относительно гидрирования возрастает в ряду соединений: сераорганические < кислородорганические < < азоторганические.
Кинетика гидроочистки реальных промышленных видов сырья весьма сложна. Сложность определятся различием в скоростях превращения различных классов сернистых соединений (иногда на порядок больше), а также изменением активности катализатора в ходе процесса. Кроме того, всегда, особенно в случае тяжелых продуктов, приходится считаться с большой вероятностью диффузионных ограничений. Наконец, влияют явления торможения реакций сероводородом при гидрогенолизе индивидуальных соединений. Несмотря на все перечисленные трудности, было выведено достаточно много кинетических уравнений для расчета скоростей гидроочистки.
В одной из первых работ [5] было предложено уравнение первого порядка:

,

Где и - парциальное давление сернистых соединений в гидрогенизате и в сырье, - константа скорости реакции, - условное время реагирования. Было показано, что до глубины обессеривания 95% и в случае узких фракций это уравнение удовлетворительно описывает скорость процесса. Однако для широких фракций оно не применимо, так как в этом случае скорость десульфуризации является суммой различных скоростей в уравнениях первого порядка для узких фракций. Константы скоростей десульфуризации, экстраполированные к нулевому парциальному давлению (бесконечное разбавление водородом), мало зависели от давления водорода, а соответствующие константы при парциальном давлении жидких продуктов 250 кПа - весьма существенно. Это интерпретировалось как явление более предпочтительной адсорбции жидких продуктов, вследствие чего при высоких парциальных давлениях последних поверхность катализатора становится труднодоступной для водорода и его давление начинает определять скорость реакции [5].
Позднее, вышеописанное уравнение было упрощено (не учитывалось влияние циркулирующего водорода):

,
Где и - концентрация серы в сырье и продукте, - объемная скорость подачи сырья, а - константа скорости реакции.
Наконец, была показана применимость уравнения первого порядка, как по сырью, так и по водороду, выведенного на основании изотермы Ленгмюра. Однако приложение его к скоростям гидрогенолиза индивидуальных соединений показало столь значительную разницу, что уравнение пришлось сильно усложнить. Поэтому для промышленного сырья, особенно для сырья широкого фракционного состава или высококипящего, подбирали любые эмпирические уравнения, лишь бы они давали лучшую сходимость, чем уравнения первого порядка.
Так, на основании результатов опытов обессеривания вакуумного остатка кувейтской нефти с 5,45% серы при 3,5 и 7,0 МПа было выведено следующее уравнение [5]:

,
Где - отношение содержания серы в продукте к содержанию ее в сырье,
- константа скорости реакции; - объемная скорость. При этом авторы не считают, что второй кинетический порядок - истинный, просто он является лучшим приближением суммы многих уравнений первого порядка для отдельных классов и групп сернистых соединений. Вывод о кажущемся втором порядке подтвержден и в других работах.
Оптимальная температура гидроочистки зависит от качества сырья, от условий ведения процесса, активности катализатора и находится в пределах 340 - 400 °С.
Нижний предел температуры очистки определяется в этом случае возможностью конденсации тяжелых фракций сырья и появлением жидкой фазы, что резко замедляет гидрирование.
По мере увеличения температуры при постоянстве остальных параметров процесса, степень гидрирования сернистых соединений и непредельных углеводородов возрастает, достигая максимальной величины при температуре 420С. При дальнейшем повышении температуры глубина гидрирования сернистых соединений снижается незначительно, а непредельных углеводородов - довольно резко.
На рисунке 1 показано влияние температуры на гидроочистку смеси фракций 200 - 350С прямогонной и дистиллята каталитического крекинга в соотношении 1:1. Исходное сырье содержало 1,3% мас. серы, 33% об. сульфируемых углеводородов, имело йодное число 12 и цетановое число 45. Процесс проводили на алюмокобальтмолибденовом катализаторе [6].
Пунктирные линии - непредельные углеводороды; сплошные линии - сернистые соединения.
Рисунок 1 - Влияние температуры на глубину гидрирования сернистых соединений и непредельных углеводородов при гидроочистке смеси дистиллятов прямой перегонки и каталитического крекинга.
По мере увеличения температуры с 300 до 380 - 420С содержание сульфирующихся углеводородов в гидрогенизате снижалось с 33 до 30 - 31 % об., а при дальнейшем повышении температуры до 460С несколько увеличивается вследствие частичного дегидрирования нафтеновых углеводородов. В соответствии с этим при повышении температуры с 300 до 380С цетановое число топлива возрастает на 1 - 2 пункта, а при дальнейшем возрастании температуры начинает несколько уменьшаться.
О влиянии температуры на глубину деароматизации можно судить по данным рисунка 2 .
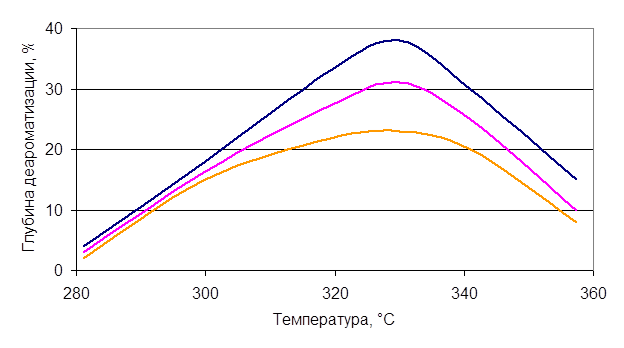
Рисунок 2 - Зависимость глубины деароматизации от температуры при разной объемной скорости подачи сырья.
Исследования проводились на катализаторе обладающем дополнительной гидрокрекирующей активностью, предназначенного для деароматизации прямогонного дизельного топлива. Они позволили выявить оптимальные значения технологических параметров. Оптимальная температура процесса составляет 330С. При ней достигается максимальная глубина деароматизации (рисунок 2). Существование максимума обусловлено снижением констант химического равновесия реакций гидрирования при увеличении температуры (таблица 3).
При гидроочистке фракций дизельного топлива повышение общего давления при заданном соотношении водород : сырье увеличивает глубину очистки до тех пор пока сырье находится преимущественно в газовой фазе, дальнейшее повышение давления ухудшает результаты процесса за счет диффузионных ограничений. При заданном общем давлении и повышении соотношения водород : сырье результаты очистки улучшаются до полного испарения сырья; при наличии жидкой фазы транспортирование водорода к поверхности катализатора обычно является лимитирующей стадией процесса и повышение парциального давления водорода увеличивает скорость диффузии за счет уменьшения доли сырья, находящегося в жидкой фазе, т. е. уменьшения толщины пленки жидкости на поверхности катализатора. После полного испарения сырья глубина гидроочистки с увеличением парциального давления водорода при неизменном общем давлении уменьшается вследствие снижения парциального давления сырья (рис. 3) .
1 - жидкофазный процесс; 2 - газофазный процесс.
Рисунок 3 - Влияние кратности циркуляции водорода на полноту обессеривания газойля 200 - 350С прямой перегонки
При гидроочистке дистиллятов вторичного происхождения - газойлей каталитического крекинга и коксования - глубина обессеривания, равная 90%, достигается при парциальном давлении водорода около 2 - 3 МПа. Однако эти продукты имеют низкие цетановые числа. Для получения дизельного топлива с цетановым числом не менее 45 требуется изменение условий гидроочистки и в первую очередь величины парциального давления водорода, т. е. необходим процесс гидрирования.
На рисунке 3 приведены основные результаты гидроочистки фракции 200 - 350С газойля каталитического крекинга, имеющего следующую характеристику: содержание серы - 1,53 %(масс.), количество сульфирующихся углеводородов - 47 %(об.), йодное число - 47, цетановое число - 37. Гидроочистку проводили на алюмокобальтмолибденовом катализаторе при температуре 380С и объемной скорости подачи сырья -
- 1,0 ч-1 . 1 - глубина обессеривания; 2 - содержание сульфирующихся углеводородов; 3 - цетановое число
Рисунок 4 - Влияние парциального давления водорода на глубину гидроочистки газойля каталитического крекинга.
Из рисунка 4 видно, что глубина обессеривания продукта, равная 90% (содержание серы 0,15 - 0,2 %(масс.)), достигается при парциальном давлении водорода около 2 МПа, т. е. гидрообессеривание протекает достаточно полно в условиях, аналогичных условиям гидроочистки прямогонных фракций.
Низкосернистые и достаточно высокоцетановые топлива можно получить при гидроочистке смеси дистиллятов прямой перегонки и вторичного происхождения. В этом случае достаточно приемлемые результаты достигаются при парциальном давлении водорода 3 - 3,5 МПа, т. е. облагораживание таких смесей можно проводить на промышленных установках гидроочистки, рассчитанных на общее давление 5 МПа.
Объемная скорость подачи сырья в зависимости от его качества, требуемой глубины очистки и условий процесса может изменяться в очень широких пределах - от 0,5 до 10 ч-1. Для тяжелого сырья и сырья вторичного происхождения объемная скорость наименьшая.
О влиянии объемной скорости подачи сырья на процесс гидроочистки смеси дистиллятов прямой перегонки и каталитического крекинга можно судить по данным рисунков 5 и 6 .
Рисунок 5 - Влияние объемной скорости подачи сырья на глубину гидрирования непредельных.
Как видно из рисунков 5 и 6, изменение степени гидрирования непредельных углеводородов в интервале объемных скоростей подачи сырья от 1,0 до 15,0 ч-1 при общем давлении 4 МПа и подаче газа, содержащего 65 %(об.) водорода, 500м3/м3 сырья происходит по сравнению с гидрированием сернистых соединений более плавно. При температуре около 300С скорости гидрирования непредельных углеводородов и сернистых соединений примерно одинаковы, при более высоких температурах скорость гидрирования сернистых соединений выше.
Рисунок 6 - Влияние объемной скорости подачи сырья на глубину обессеривания
Характеристика сырья и продуктов гидроочистки
Глубина гидроочистки дистиллятов от серы и других соединений зависит от типа углеводородного сырья, температуры процесса, парциального давления водорода и его кратности циркуляции, объемной скорости подачи сырья и других факторов.
Гидроочистке подвергают как прямогонные фракции (бензин, реактивное и дизельное топливо, вакуумные газойли), так и дистилляты вторичного происхождения (легкая фракция пиролизной смолы, бензины, легкие газойли коксования и каталитического крекинга).
С утяжелением сырья степень его очистки в заданных условиях процесса снижается. Происходит это по следующим причинам. С повышением средней молярной массы доля серы, содержащейся в устойчивых относительно гидрирования структурах, увеличивается. По мере утяжеления сырья все большая его часть находится в условиях гидроочистки в жидкой фазе, что затрудняет транспортирование водорода к поверхности катализатора. При жидкофазной гидроочистке с утяжелением сырья скорость диффузии водорода через пленку жидкости на катализаторе снижается, так как повышается вязкость и снижается растворимость водорода при данных условиях. Увеличение в сырье количества полициклических ароматических углеводородов, смол и асфальтенов, прочно адсорбирующихся на катализаторе и обладающих высокой устойчивостью относительно гидрирования, также снижает глубину очистки.
При одинаковом фракционном составе очистка от серы продуктов вторичного происхождения (коксования, каталитического крекинга) проходит значительно труднее. Это связано с тем, что подвергшиеся крекингу продукты содержат гетероатомы в структуре наиболее термически стабильных, трудно гидрирующихся соединений. Кроме того, продукты вторичного происхождения содержат большое количество ароматических и непредельных углеводородов, обладающих высокой адсорбируемостью на катализаторе и тормозящих в результате гидрирование гетероорганических соединений.
Качество получаемой продукции, то есть дизельного топлива, должно соответствовать показателям, приведенным ниже.
Фракция дизельного топлива гидроочищенная
|
Показатели качества продукта: | |
|
Содержание воды и механических примесей |
Отсутствие |
|
Фракционный состав
|
|
|
Сероводородная коррозия |
Отсутствие |
|
Испытание на медной пластинке |
Выдерживает |
|
Температура вспышки, Определяемая в закрытом тигле, С Не ниже |
62 |
|
Массовая доля общей серы, ppm масс. Не более |
10 |
|
Азот, ppm масс. Не более |
20 |
|
Йодное число, гр/100гр. |
0,5 |
|
Плотность, кг/м3 Не более |
834 |
|
Применяется как компонент дизельного топлива. |
Бензин-отгон.
|
Показатели качества продукта: | |
|
Содержание воды и механических примесей |
Отсутствие |
|
Испытание на медную пластинку |
Выдерживает |
|
Температура начала кипения, С Не ниже |
40 |
|
Температура конца кипения, С Не выше |
180 |
|
Применяется как компонент автомобильных бензинов. |
Сероводород.
|
Показатели качества продукта: | |
|
Содержание сероводорода, % объемных Не менее |
98,0 |
|
Применяется в качестве сырья для производства серной кислоты. |
Углеводородный газ (после очистки).
|
Показатели качества продукта: | |
|
Содержание сероводорода, % объемных |
Не более 0,20 |
|
Применяется в качестве печного топлива на установке. |
Катализаторы гидроочистки
Ужесточающиеся требования к качеству нефтепродуктов, в первую очередь по снижению содержания в среднедистиллятных фракциях серы и ароматических углеводородов, заставляют искать более эффективные катализаторы гидроочистки. Катализаторы гидроочистки представляют собой сочетание окислов активных компонентов (никель, кобальт, молибден и др.) с носителем, в качестве которого чаще всего используют активную окись алюминия. Носитель в составе катализатора гидроочистки играет роль не только инертного разбавителя, но и участвует в формировании активных фаз, а также служит в качестве структурного промотора, создающего специфическую пористую структуру, оптимальную для переработки конкретного сырья.
Для гидроочистки применяют катализаторы на основе оксидов металлов VII и VIII групп (никель, кобальт, молибден, вольфрам). В промышленности используют алюмокобальтмолибденовый (АКМ) и алюмоникельмолибденовый (АНМ) катализаторы. В алюмоникельмолибденовый катализатор на силикатной основе для увеличения прочности вводят диоксид кремния (АНМС).
Носителем служит оксид алюминия. Катализаторы выпускают в виде частиц неправильной цилиндрической формы. В настоящее время применяются катализаторы на цеолитной основе. Катализатор АКМ имеет высокую активность и селективность по целевой реакции обессеривания, достаточно активен в гидрировании непредельных соединений. Катализатор АНМ проявляет большую активность при гидрировании ароматических и азотистых соединений.
Наиболее распространенные для гидроочистки в отечественной и зарубежной практике катализаторы приведены в таблице 6 .
Таблица 6 - Катализаторы гидроочистки нефтяных фракций
|
Марка катали-затора |
Характеристика |
Сырье |
Форма |
Тип носи-теля |
Актив-ные компо-ненты |
|
AKZO Nobel | |||||
|
KF-845 |
Высокая обессериваю-щая и деазотирующая активность |
От бензина до вакуумного газойля |
Четырех-листник |
Al2O3 |
NiMo |
|
KF-752 |
Высокая обессеривающая активность |
От дизельного топлива до ваку-умного газойля |
Четырех-листник |
Al2O3 |
CoMo |
|
KF-747 |
Глубокое гидрообессеривание |
От дизельного топлива до ваку-умного газойля |
Четырех-листник |
Al2O3 |
CoMo |
|
KF-645 |
Глубокое гидрообессеривание, деметализация, легкий гидрокрекинг |
От бензина до вакуумного газойля |
Цилиндр |
Al2O3 |
NiCoMo |
|
"Элетрогорский институт нефтепереработки" | |||||
|
ГО-70 |
Высокая обессеривающая и деазотирующая активность |
От бензина до вакуумного газойля |
Цилиндр, трилистник |
Al2O3 |
CoMo |
|
ГО-86 |
Высокая обессеривающая активность |
Среднедистил-лятные фракции |
Цилиндр |
Al2O3 |
CoMo |
|
ГО-30-7 |
Высокая обессеривающая и деазотирующая активность |
Бензины |
Цилиндр |
Al2O3 |
NiMo |
|
ГО-38а |
Обессеривание и насы-щение ароматических углеводородов |
Масляные дистилляты |
Цилиндр |
Al2O3 |
NiMo |
|
КПС-16Н |
Высокая обессеривающая активность |
Дизельные фракции |
Цилиндр |
Al2O3 |
NiMo |
|
ДТ-005К, ДТ-005Н |
Глубокое гидрообессеривание |
Дизельные фракции |
Цилиндр |
Al2O3 |
CoMo, NiMo |
|
Criterion Catalyst | |||||
|
С-448 |
Для получения низкосернистого дизельного топлива |
Средние дистил-ляты, вакуумный газойль |
Сформо-ванные экструдаты |
Al2O3 |
CoMo |
|
С-447 |
Глубокое гидрообессеривание |
Легкий и тяже-лый вакуумный газойль, остатки |
Сформо-ванные экструдаты |
Al2O3 |
CoMo |
|
HDS-3 |
Насыщение ароматических углеводородов |
От бензина до вакуумного газойля |
Сформо-ванные экструдаты |
Al2O3 |
NiMo |
|
HDS-22 |
Насыщение ароматических углеводородов |
Бензин, сырье каталитического крекинга |
Сформо-ванные экструдаты |
Al2O3 |
CoMo |
|
C-424 |
Высокая гидрообессеривающая и гидродеазотирующая активность, насыщение ароматических углеводородов |
Предваритель-ная гидроочистка сырья каталитического крекинга |
Сформо-ванные экструдаты |
Al2O3 |
NiMo |
|
"Всероссийский институт по переработке нефти" | |||||
|
ГS-168 |
Обессеривающая активность |
Бензин, дизельная фракция |
Цилиндр |
Al2O3+ SiO2 |
NiMo |
|
ГДК-202 |
Высокая обессеривающая активность |
Среднедистил-лятные фракции |
Цилиндр |
Al2O3+ цеолит |
NiMo |
|
ГДК-205 |
Высокая обессеривающая активность |
Среднедистил-лятные фракции |
Цилиндр |
Al2O3+ цеолит |
NiMo |
|
ГДК-202П |
Высокая обессеривающая активность |
Среднедистил-лятные фракции |
Цилиндр |
Al2O3+ цеолит |
CoMo |
|
ГП-534 |
Высокая обессеривающая активность |
От бензина до вакуумного газойля |
Цилиндр |
Al2O3 |
NiMo |
|
Procatalyse | |||||
|
HPC-60 |
Высокая обессеривающая активность |
От бензина до вакуумного газойля |
Лист клевера |
Al2O3 |
- |
|
HR-306C |
Гидрообессери-вание, гидро-деазотирование |
От бензина до вакуумного газойля |
Экструдаты |
Al2O3 |
- |
|
Haldor Topsoe | |||||
|
TK - 524 |
Глубокое гидрообессеривание |
Легкий и тяже-лый вакуумные газойли |
Трехлист-ник |
Al2O3 |
CoMo |
|
TK-907, TK - 908 |
Снижение ароматических углеводородов, низкая сероустойчивость |
Легкий и тяже-лый вакуумные газойли |
Трехлист-ник |
Патент |
Патент |
|
Orient catalysts Co. Ltd | |||||
|
HOP-412 |
Высокое гидродеазотирование и гидрообессеривание |
От бензина до вакуумного газойля |
Сформован-ные экструдаты |
Al2O3 |
NiMo |
|
HOP-463 |
Высокое гидродеазотирование и гидрообессеривание |
От бензина до котельного топлива |
Сформован-ные экструдаты |
Al2O3 |
CoMo |
Особый интерес представляют катализаторы фирм Criterion Catalyst (C-448), Haldor Topsoe (TK-554, TK-907, TK-908), AKZO Nobel (KF-752), а также отечественные катализаторы Элетрогорского института нефтепереработки серии "ГО".
Испытания катализаторов вышеперечисленных компаний на ОАО "Славнефть-Ярославнефтеоргсинтез" показали их различную гидрообессеривающую активность (рисунок 7) .
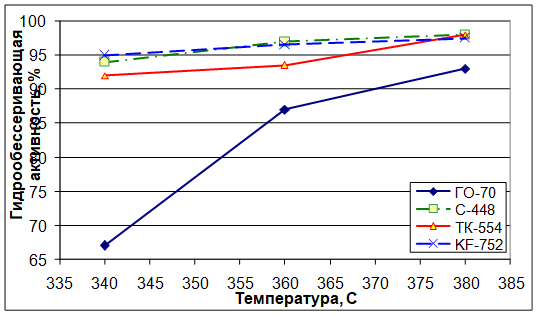
Рисунок 7 - Гидрообессеривающая активность катализаторов ГО-70, С-448, KF-752 и ТК-554 (давление 3 МПа, объемная скорость 4 ч-1, содержание серы в сырье 1,3% масс.).
Результаты испытаний фиксировались при температурах 340, 360 и 380С, а также объемной скорости 3 и 4 ч-1. Было отмечено, что при температурах 360 и 380С и объемной скорости 3 ч-1 все катализаторы позволяли получить дизельное топливо с содержанием серы менее 0,05% масс., однако при увеличении объемной скорости до 4 ч-1 и снижении температуры до 340С наблюдалась заметная разница в активности испытанных катализаторов.
В процессе деароматизации наиболее эффективными являются катализаторы, в состав которых входят промотирующие компоненты для усиления крекирующей активности, а также оксиды гидрирующих металлов в повышенных концентрациях.
Катализаторы деароматизации дизельного топлива были испытаны в лабораторных и полупромышленных условиях. Испытания проводили с использованием в качестве сырья прямогонное дизельное топливо с содержанием 1,7% масс. серы и 36% масс. ароматических углеводородов. Результаты испытаний представлены в таблице 7 .
Таблица 7 - Результаты исследования каталитических систем деароматизации
|
Каталитическая система |
Режим деароматизации |
Глубина деароматизации, % | ||
|
Давление, МПа |
Температура |
Объемная скорость подачи сырья, ч-1 | ||
|
NiMo |
8-12 |
Умеренная |
0,5-1,5 |
30-50 |
|
NiMo+NiW |
8-12 |
Умеренная |
1-2 |
30-50 |
|
NiW +NiW |
4-6 |
Умеренная |
0,25-0,5 |
30-50 |
|
NiW+Pt/Al2O3 |
4-6 |
Низкая |
0,1 |
65-80 |
|
NiMo+ССК |
4-6 |
Умеренная |
0,5-1,5 |
65-80 |
Как видно, с практической точки зрения наиболее приемлема каталитическая система NiW+Pt/Al2O3. При умеренном давлении и низкой температуре она обеспечивает высокую степень деароматизации. Недостаток этой системы - очень высокая чувствительность к присутствию серы в сырье. Ее содержание не должно превышать 1-3 ppm. Кроме того, для достижения необходимой конверсии ароматических углеводородов объемная скорость подачи сырья должна быть менее 0,1 ч-1, что на практике трудно осуществимо. Фирмой Haldor Topsoe был разработан серостойкий катализатор (ССК) на основе благородного металла способный работать на сырье, содержащем до 500 ppm. серы. Он обеспечивает высокую конверсию ароматических соединений при умеренном давлении и объемной скорости.
На базе катализаторной системы ССК разработаны два катализатора деароматизации: ТК-907 на аморфном носителе, и ТК-908 на цеолите. Первый рекомендуется применять при содержании серы в сырье менее 10ppm., второй - до 500ppm. Эти катализаторы были испытаны на пилотной установке в течение 1300 и 5500 ч соответственно. Процесс протекал при умеренной температуре и давлении около 4,6 МПа на катализаторе ТК-907 и около 5 МПа на катализаторе ТК-908. Дезактивации катализаторов за время испытаний не наблюдалось. Содержание ароматических углеводородов в обоих случаях не превышало 5% при содержании их в сырье 20-22% .
Окислительный метод обессеривания
Основными классами сернистых соединений, содержащихся в нефтяных фракциях, являются тиолы, диалкил - и циклоалкилсульфиды, алкиларилсульфиды, а также гетероароматические соединения -- производные тиофена. Сернистые соединения, которые необходимо удалить из фракций дизельного топлива, чтобы снизить содержание серы в них с 300--500 ррm до требуемого уровня в 10--50 ррm, представлены в основном бензотиофеном, дибензотиофеном и их алкильными производными.

R = Н, алкил
Наиболее распространенным окислителем для превращения сернистых соединений нефтяных фракций в настоящее время является пероксид водорода в сочетании с различными катализаторами. Этот окислитель в виде 30%-го водного раствора использовали для окисления дизельной фракции арланской нефти с содержанием серы 2,2% (масс.) с целью получения концентратов сульфоксидов. Для окисления алкилароматических сульфидов до соответствующих сульфоксидов и сульфонов может использоваться пероксид водорода, образующий с солями переходных металлов пероксокомплексы, например, ванадия или ниобия. Реакция идет в двухфазной системе с высокими выходами, окислитель находится в водной фазе, а субстрат -- в органической. Другой вариант окисления сернистых соединений дизельного топлива был предложен в работе, когда окисление пероксидом водорода проводилось в пенно-эмульсионном режиме в присутствии соединений металлов (Мо, V, W) с последующим каталитическим разложением сульфонов на диоксид серы и углеводород. Детальное исследование механизма окисления модельных нефтяных сернистых соединений (бутантиол, тиофенол, дифенилсульфид, бензотиофен, дибензотиофен) системой из пероксида водорода и муравьиной кислоты в различных растворителях показало, что ароматичность органической матрицы влияет на кинетику реакции окисления. Скорость окисления хорошо описывается уравнением первого порядка и возрастает с ростом соотношения С/Н в молекуле растворителя. Авторы полагают, что окисление тиолов и сульфидов представляет более сложный процесс, чем окисление бензо - и дибензотиофенов. Для окисления дибензотиофена и его моно - и диалкильных производных были предложены различные окислительные системы, причем положение алкильных групп в диалкилбензотиофенах играет важную роль в их реакционной способности. Для диалкильных производных бензотиофенов обессеривание наиболее легко протекает на катализаторе СоМо/А12О3 . При окислении бензотиофена, дибензотиофена, 4-метилдибензотиофена и 4,6-диметилдибензотиофена действием трет-бутилгидропероксида на Мо/А12Оз, максимальную активность в окислении дибензотиофена проявил катализатор, содержащий 16% молибдена, дальнейшее увеличение содержания металла в катализаторе уменьшало его каталитическую активность. По реакционной способности при окислении на катализаторе 16% Мо/А12Оз изученные сернистые соединения располагаются в ряд:
Дибензотиофен > 4-метилдибензотиофен > 4,6-диметилдибензотиофен > бензотиофен
Интересным примером окисления бензотиофена и дибензотиофена до сульфонов в мягких условиях является реакция с пероксидом водорода в присутствии краун-эфиров без добавления каких-либо соединений металлов:

Энзиматическое окисление дибензотиофена, катализируемое ланказой в присутствии 2,2'-бис - (З-этилбензтиазолин-6-сульфоновой кислоты), сравнивали с окислением пероксидом водорода в присутствии фосфоромолибденовой кислоты. Константа скорости окисления дибензотиофена в присутствии энзима в 70 раз больше при 40 °С в системе гексан/этанол, чем в присутствии фосфорномолибденовой кислоты, что свидетельствует об определенных преимуществах ферментативного способа окисления. С другой стороны, использование избытка пероксида водорода в присутствии фосфоромолибденовой кислоты для обессеривания дизельного топлива с содержанием серы 342 ррm позволило за 3 ч при 60 °С получить образец топлива, практически не содержащий серы. Из других биологических методов обессеривания топлив, содержащих производные бензотиофена, можно отметить способ, основанный на использовании термофильных бактерий Mycobacterium после предварительного гидрообессеривания топлива. В этом случае сочетание этих двух методов позволяет понизить содержание серы в топливе на 86%.
Распространенными окислителями сернистых соединений нефти являются различные алкилгидропероксиды. Так, окисление сульфидов масляных фракций гидропероксидами трет-амила, трет-бутила и кумила в присутствии низших карбоновых кислот показало, что они могут быть использованы для получения концентратов сульфоксидов с выходами до 94%. Для каталитического окислительного обессеривания смеси бензотиофена и дибензотиофена в декалине использовали растворимый в нефти окислитель -- циклогексанонпероксид в сочетании с оксидом молибдена МоО3, нанесенным на макропористую катионообменную смолу со слабокислыми свойствами.
Авторам этой работы удалось достигнуть 100%-й конверсии дибензотиофена в дибензотиофенсульфон при 100 °С за 40 минут. Использование других растворимых в нефти алкилпероксидов позволило оценить их активность в окислительном обессеривании, которая падала в ряду:циклогексанонпероксид > трет-амилгидропероксид > трет-бутилгидропероксид
Авторы предложили механизм окисления, включающий в качестве первой стадии координацию алкилгидропероксида с МоО3 на поверхности катионообменной смолы, в результате чего повышается электрофильность пероксидного кислорода :

Совсем недавно в качестве окислителя для глубокого обессеривания дизельного топлива был предложен феррат калия в соотношении с содержащейся в топливе серой К2FeO4/S = 7,0. При начальной концентрации серы 457 ррm использование этого окислителя позволило авторам работы при оптимальных условиях обессеривания довести степень удаления серы до 97% и снизить содержание серы с 457 до 15,1 ррm.
Адсорбционный метод обессеривания
Адсорбция (от лат. ad - на, при и sorbeo - поглощаю) - преимущественное концентрирование молекул газа или растворенного в жидкости вещества (адсорбата) на поверхности жидкости или твердого тела (адсорбента), а также растворенного в жидкости вещества на границе ее раздела с газовой фазой. Является частным случаем сорбции и одним из важнейших типов поверхностных явлений.
Явление адсорбции связано с тем, что силы межмолекулярного взаимодействия на границе раздела фаз не скомпенсированы, и, следовательно, пограничный слой обладает избытком энергии - свободной поверхностной энергией. В результате притяжения поверхностью раздела фаз находящихся вблизи нее молекул адсорбата свободная поверхностная энергия уменьшается, т. е. процессы адсорбции энергетически выгодны.
В зависимости от характера взаимодействия молекул адсорбата и адсорбента различают физическую адсорбцию и хемосорбцию. Физическая адсорбция обусловлена силами межмолекулярного взаимодействия и не сопровождается существенным изменением электронной структуры молекул адсорбата. Физическая адсорбция может быть как монослойной (с образованием мономолекулярного слоя), так и полимолекулярной (многослойной). При А. электролитов из их растворов обычно возникает двойной электрический слой. Если жидкий адсорбат смачивает пористый адсорбент, то в порах последнего может происходить капиллярная конденсация. При физической адсорбции адсорбирующие молекулы обычно обладают поверхностной подвижностью.
При хемосорбции между атомами (молекулами) адсорбента и адсорбата образуется хим. Связь, таким образом, хемосорбцию можно рассматривать как химическую реакцию, область протекания которой ограничена поверхностным слоем. В некоторых случаях на одной поверхности могут протекать оба типа адсорбции одновременно. В случае не слишком пористых адсорбентов физическая адсорбция имеет место, как правило, при температуpax ниже критической температуры конденсации адсорбата, хемосорбция же чаще всего протекает при гораздо более высоких температурах. Однако в некоторых системах физическая адсорбция может протекать при температуpax, значительно превышающих критич. температуру конденсации адсорбата. Как и любые химические реакции, процессы хемосорбции носят специфичный характер (т. е. адсорбент хемосорбирует не любые молекулы, а лишь те, которые вступают в реакцию с атомами поверхности); в некоторых случаях специфичность может проявляться и при физической адсорбции.
Количественной характеристикой адсорбции является величина Г, представляющая собой избыток адсорбата, приходящийся на единицу площади поверхностного слоя, по сравнению с количеством адсорбата в единицу объема фазы адсорбента. Отношение называется степенью (или долей) покрытия поверхности (-предельно возможная величина монослойной адсорбции для данной системы).
Процессы адсорбции почти всегда сопровождаются выделением теплоты, называемой теплотой адсорбции, которая возрастает с увеличением прочности связи адсорбат - адсорбент и составляет обычно 8-25 кДж/моль (иногда до 80 кДж/моль) для физической и, как правило, превышает 80 кДж/моль при хемосорбции. Если хемосорбция сопровождается диссоциацией адсорбированных молекул, может наблюдаться поглощение тепла. По мере заполнения поверхности теплота адсорбции обычно уменьшается в результате неоднородного распределения свободной энергии на поверхности или латерального взаимодействия молекул в адсорбированном слое. Для адсорбентов, обладающих несколькими типами адсорбирующих центров, теплота адсорбции может быть различной для разных типов центров, и распределение свободной энергии на поверхности является дискретно-неоднородным. При переходе к полимолекулярной адсорбции теплота адсорбции понижается до величины, близкой к теплоте конденсации адсорбата. Если теплота адсорбции сравнима с поверхностной энергией адсорбента, то в процессе адсорбции может существенно меняться кристаллическая структура поверхности твердого тела, причем при физической адсорбции перестройке подвергаются в основном поверхности молекулярных кристаллов, а в случае хемосорбции изменение поверхностной структуры наблюдается даже для металлов и ионных кристаллов.
Абсорбционные методы очистки - заключаются в избирательном (селективном) растворении вредных компонентов нефтепродукта. В качестве избирательных растворителей используются нитробензол, фурфурол, жидкая двуокись серы, дихлорэтиловый эфир и др. К недостаткам метода можно отнести потери растворителей, вследствие невозможности их восстановления. Этот метод использует редко для очистки дизельного топлива, в основном для масел /9/.
Мембранный метод очистки, позволяет выделять серные соединения (меркаптаны, сульфиды, дисульфиды, тиофены и др.) из дизельного топлива. Она обладает целым рядом преимуществ по сравнению с гидроочисткой:
- 1. Отсутствие химических превращений; 2. Отсутствие дорогостоящих катализаторов; 3. Малые количества используемых реагентов (0,26 кг на 1 кг дизельного топлива) и их полное восстановление в процессе очистки; 4. Низкие энергетические затраты (0,017 кВт-час на 1 кг дизельного топлива);
Похожие статьи
-
Способы улучшения качества дизельного топлива - Сравнительный анализ методов обессеривания
Специальные присадки Понижение содержания серы в дизельном топливе, как правило, приводит к уменьшению его смазывающих свойств, поэтому для дизельных...
-
Сера в дизельном топливе - Сравнительный анализ методов обессеривания
Сера и ее соединения в качестве естественной составляющей входят в состав сырой нефти в виде элементарной серы, сероводорода и различных органических...
-
Введение - Сравнительный анализ методов обессеривания
С развитием техники повышаются требования к ассортименту и качеству нефти и нефтепродуктов, что, в свою очередь, требует совершенствования процессов их...
-
Макрокинетика процесса - Каталитический риформинг
Характерной особенностью всех модификаций риформинга является то, что одна из его основных стадий - ароматизация - эндотермична, а другая - гидрокрекинг...
-
Получение синтезированного газа - Анализ и технологическая оценка химического производства
Химические методы переработки нефти проводят при высоких температурах без катализатора (термический крекинг), при высоких температурах в присутствии...
-
Закономерность управления процессом для реакции - Каталитический риформинг
Управлять ХТП - это означает, меняя технологические параметры процесса (температуру, давление, состав сырья, катализатор, скорость перемешивания,...
-
Количественный анализ - это совокупность, химических, физико-химических и физических методов определения количественного соотношения компонентов,...
-
Описание технологического процесса Процесс каталитического риформинга осуществляют при сравнительно высокой температуре и среднем давлении, в среде...
-
Один из способов повысить селективность - это правильно подобрать катализатор. Рассмотрим этот метод, на примере получения анизола и крезола. Анизол и...
-
Численный сравнительный анализ - Ранговый метод оценивания параметров регрессионной модели
Итак, в рамках данной работы рассматриваются такие распределения случайных величин, как распределения Гаусса и Лапласа, треугольное распределение...
-
Это метод который нашел мировое применение для анализа лекарствнных средств. Он основан на свойстве галогенидов количественно осаждаться нитратом серебра...
-
МЕТОДЫ СРАВНИТЕЛЬНОГО ШКАЛИРОВАНИЯ - Многомерный статистический анализ
Шкалирование методом попарного сравнения - Это метод сравнительного шкалирования, при котором респонденту дается два объекта для выбора по определенному...
-
В настоящее время производственные методы получения формальдегида большим разнообразием не отличаются. Так, в реакциях восстановления СО и СО2 Водой...
-
НЕМНОГО О ПРОМЫШЛЕННОМ КАТАЛИЗЕ - Процесс катализа
На всю жизнь запомнилась мне проводившаяся по Энглеру разгонка полученного конденсата, в котором уже в начале опыта бензиновая фракция составляла 67%. Мы...
-
Цель работы: освоение методик подготовки проб почвы и растительности, подготовка проб почвы и растительности для инструментального...
-
Азотный кислота утилизация оксид Методы получения азотной кислоты Первый завод по производству HNO3 из аммиака коксохимического производства был пущен в...
-
В настоящей работе растворы готовились весовым методом: путем растворения точно взвешенных навесок в мерной посуде. Концентрации тестируемых соединений в...
-
Радиоактивность природных вод В питьевом водоснабжении преимущественно используются поверхностные воды из рек, озер, водохранилищ, а также грунтовые воды...
-
Выбор метода производства (или выделение) готового продукта Современные методы производства азотной кислоты основаны на применении синтетического аммиака...
-
Адсорбционные методы исследования свойств поверхности позволяют количественно охарактеризовать происходящие при адсорбции межмолекулярные взаимодействия,...
-
Производство полимеров - Анализ и технологическая оценка химического производства
Высокомолекулярные соединения получают из мономеров полимеризацией, сополимеризацией, поликонденсацией и методами привитой полимеризации и...
-
Полимеризация двуокиси азота. Переработка нитрозных газов в азотную кислоту обычно происходит при температурах от О до 50 °С. В этих условиях двуокись...
-
Подготовка прибора к эксплуатации 1. Внешний осмотр: Проверка: Отсутствия механических повреждений, Отсутствия коррозии, Надежности крепления,...
-
Качественные методы анализа - Разработка технологической схемы получения анизола и крезола
Рециркуляционных реакционно-ректификационных процессов. При анализе сложных ХТС, характеризующихся большим числом параметров и переменных необходимо...
-
Методы анализа - Свойства флавоноидов
Качественное определение. Для обнаружения флавоноидов в ЛРС используют химические реакции и хроматографию. Химические реакции подразделяются на цветные и...
-
Преимущества комплексного применения методов анализа силикатных материалов
Химический состав силикатов можно представить как сочетание различных оксидов металлов и неметаллов с SiO2. Например, силикат натрия - натриевая соль...
-
Вещество [Co] Лиганды и Комплексообразователь Координационное число 6 Для комплексов с координационным числом 6 характерно октаэдрическое расположение...
-
Метод наименьших квадратов - Анализ методов прогнозирования
Расчет параметров af b для конкретной функциональной зависимости осуществляется с помощью метода наименьших квадратов (МНК) и его модификаций. Суть МНК...
-
Также сравнила методики анализа и выявила, что наиболее применяемым методом осаждения является аргентометрия вариантом Фаянса. Это наиболее доступный,...
-
Что является сырьем, реагентом, полупродуктов, продуктом - Каталитический риформинг
В настоящее время каталитический риформинг стал одним из ведущих процессов нефтеперерабатывающей и нефтехимической промышленности. С его помощью удается...
-
Методы неорганического синтеза - Синтез ацетата натрия ("Горячий лед")
НЕОРГАНИЧЕСКИЙ СИНТЕЗ, получение неорганических соединений. Как правило, состоит из нескольких последовательных или параллельных процессов -...
-
Сравнение методов получения хлорида калия - Производство хлорида калия галургическим способом
Флотационный метод обогащения по сравнению с галургическим (растворение и кристаллизация) имеет следующие преимущества: - флотация проходит при...
-
РОЛЬ КАТАЛИЗА В ЭКОЛОГИИ - Процесс катализа
Огромную роль призван сыграть катализ в решении актуальнейшей проблемы - охраны окружающей среды. По словам Кусто, земной шар напоминает "одиноко...
-
Термоконтактные процессы пиролиза - Пиролиз углеводородного сырья
Разработка процессов пиролиза, основанных на передаче тепла пиролизуемому сырью при его контакте с нагретыми теплоносителями, относилась к 50-60-м годам...
-
Химическое равновесие - Скорость химических процессов. Химическое равновесие, принцип Ле-Шателье
Химическое равновесие и его признаки. Равновесие истинное и заторможенное (ложное). Принцип Ле-Шателье. Константа равновесия и ее связь с...
-
Общие понятия и определения. Термодинамический и кинетический критерий реакционной способности химической системы. Скорость химической реакции. Факторы,...
-
Процесс варки стекла - Производство стекла
Стекловарение ведется при температурах порядка 1400°--1600°. В нем различают три стадии. Первая стадия -- провар, или варка в собственном смысле слова,...
-
Теоретические основы процесса выпаривания Для осуществления процесса выпаривания необходимо теплоту от теплоносителя передать кипящему раствору, что...
-
Производство азотной кислоты - Анализ и технологическая оценка химического производства
Безводная азотная кислота HNO3--тяжелая бесцветная жидкость плотностью 1520 Кг/м 3 (при 15° С). Она замерзает при температуре --47° С и кипит при 85°С,...
-
Методы, применяющиеся для синтеза мультиферроиков - Мультиферроики
Для синтеза мультиферроиков используются различные методы синтеза. К ним относятся: спекание, гидротермальный синтез, соосаждение, золь-гель метод,...
Химизм процесса гидроочистки - Сравнительный анализ методов обессеривания