Кондуктометрическое титрование - Электрохимические методы исследования
Несомненно, большими аналитическими возможностями обладает кондуктометрическое титрование. Титрование позволяет восполнить недостаток селективности определения применением селективного к анализируемому иону титранта. Известны примеры кислотно-основного, осадительного, комплексонометрического титрований. Точность кондуктометрического титрования составляет 1%, но если принять меры по термостатированию анализируемого раствора, то точность определения можно в несколько раз увеличить. Типичный вид кривой кондуктометрического титрования представлен на рисунке 1.
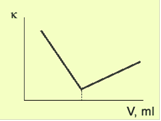
Рис. 1
Точка эквивалентности на графике находится пересечением двух прямых. Одна прямая (до точки эквивалентности) отражает изменение концентрации анализируемого иона и ионов титранта, а другая (после точки эквивалентности) является следствием увеличения концентрации ионов титранта. Однако не всегда кривая титрования имеет такой вид. На рис. 2 приведены в качестве примера кривые титрования, полученные в результате различных аналитических определений.
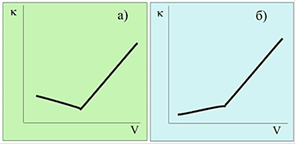
Рис. 2
Вид кривых очевидно различен. В связи с этим возникает закономерный вопрос о причинах различий и возможности прогнозирования вида кривой на основании данных о свойствах анализируемого иона и вещества титранта. В большинстве случаев прогноз возможен, поскольку вид кривой титрования определяется разностью эквивалентных электропроводностей анализируемого иона и ионов, составляющих вещество титранта. Рассмотрим несложный расчет, позволяющий прогнозировать вид кривой титрования. Прежде всего, нужно ясно представить себе перечень ионов, принимающих участие в процессе титрования. Пусть нам предстоит определить хлорид с помощью осадительной реакции с нитратом серебра:
Cl - + Ag+ + NO3- = AgCl + NO3
Не вызывает сомнения, что в процессе титрования до точки эквивалентности происходит уменьшение ионов Cl - и NO3- Увеличение концентрации ионов Ag+ практически не происходит, так как серебро осаждается ионом Cl - В связи с этим можно утверждать, что динамика электропроводности происходит со скоростью, пропорциональной сумме:
L 0Cl + l 0NO3 =-0,00655 + 0,00617 = -0,00038 Ом-1 мІ г-экв-1.
Знак '-' перед электропроводностью l 0Cl говорит о том, что концентрация Cl в результате титрования уменьшается. Знак '+' перед l 0NO3 свидетельствует об увеличении концентраци NO3. Полученное в итоге отрицательное число -0,00038 Ом-1 мІ г-экв-1 указывает на то, что при титрованиии до точки эквивалентности электропроводность раствора уменьшается. После точки эквивалентности электропроводность будет повышатьcя, так как эту ветвь титрования полностью определяет титрант, т. е. ионы Ag и NO3:
0Ag + l 0NO3 = 0,005436 + 0,00617 = 0,011606 Ом-1 мІ г-экв-1.
Прошу обратить внимание на то, что полученное число положительно, что говорит об увеличении электропроводности раствора с каждой порцией титранта. Кривой титрования (рис. 2б) на рисунке может соответствовать титрование ацетата натрия соляной кислотой. Почему? Потому, что до точки эквивалентности электропроводность раствора будет возрастать, а не убывать как в предыдущем случае:
L 0 ацетат + l 0Cl = -0,0034 + 0,00655 = 0,00315 Ом-1 мІ г-экв-1.
В заключении хочу предупредить о том, что любое отклонение кривой титрования от описанных выше видов, должно настораживать, так как при этом увеличивается вероятность появления больших систематических ошибок.
Похожие статьи
-
Теоретические основы кондуктометрического метода анализа - Электрохимические методы исследования
Кондуктометрические методы анализа основаны на измерении электропроводности исследуемых растворов. Существует несколько методов кондуктометрического...
-
Кривые титрования - Методы осаждения
Кривые титрования в аргентометрии обычно строят в координатах pAg -- V, Где pAg -- взятый с обратным знаком лога-рифм концентрации ионов Ag+, V -- Объем...
-
Введение - Электрохимические методы исследования
Кондуктометрия (от англ. conductivity - электропроводность и метрия) - совокупность электрохимических методов анализа, основанных на измерении...
-
Электрическое сопротивление - Электрохимические методы исследования
Основной константой, характеризующей электрические свойства вещества, является удельное электрическое сопротивление, зависящее от природы вещества и от...
-
В пробирку переносят 2 см3 фильтрата водной вытяжки и по каплям добавляют раствор дифениламина в серной кислоте. При наличии нитратов раствор...
-
Методика отбора и хранения проб Отбор и хранение проб производилось согласно ГОСТ Р 51592-2000 "Общие требования к отбору проб".[35,36] Пробы воды в...
-
Подсчет колоний микроорганизмов производился с помощью счетчика колоний Flash&;Go. Изначально с помощью сопутствующей программы производилась калибровка,...
-
В аргентометрии применяют различные способы установления точки эквивалентности как с помощью индикаторов, так и без них. Метод равного помутнения. Идея...
-
Основные понятия теории экономико-математического моделирования Кибернетический подход к исследованию экономико-математических систем Обычно...
-
Это раздел математического программирования, изучающий методы решения таких экстремальных задач, в которых результаты (эффективность) возрастают или...
-
В основе метода лежит закон адитивности оптической плотности при соблюдении основного закона светопоглощения. Ход работы 1. Выбор оптимальных...
-
Из перечисленного обзора типов ММ, составляющих предмет ИСО, можно выделить следующие особенности ММ ИСО [3]. - Системный подход, заставляющий...
-
Общая схема исследования: 1. Составление среднего образца. 2. Извлечение пестицидов из пробы. 3. Очистка экстракта. 4. Анализ экстракта. Прием образцов в...
-
Одним из наиболее важных аспектов построения систем моделирования является проблема цели. Любую модель строят в зависимости от цели, которую ставит перед...
-
1. Ознакомиться с методами регрессионного анализа и планирования эксперимента; 2. Определить коэффициенты статистической характеристики объекта...
-
При управлении подвижными объектами (такими, например, как мобильные роботы, подводные аппараты и т. п.) часто имеет место неопределенность цели, когда...
-
Легирование В настоящее время создано большое число нержавеющих сталей путем присадок к железу никеля, хрома, кобальта и др. Оказалось, что при...
-
С развитием системных исследований, с расширением экспериментальных методов изучения реальных явлений все большее значение приобретают абстрактные...
-
Вычисления для следующих входных данных F=1000H m=200 кг m'=1 кг/сек k=2 t0=0 сек V0=0 м/сек B=50 n=50 V1 (t) - результаты, полученные с помощью...
-
Адсорбционные методы исследования свойств поверхности позволяют количественно охарактеризовать происходящие при адсорбции межмолекулярные взаимодействия,...
-
Метод наименьших квадратов - Основы научных исследований
Пусть проведен однофакторный эксперимент, в котором исследована зависимость У от Х . Установлено, что основные предпосылки регрессионного анализа...
-
Метод максимального правдоподобия - Основы научных исследований
Разработан Р. Фишером. Пусть Х 1 ,х 2 ...х N - выборка из генеральной совокупности случайной величины Х с функцией плотности вероятности Р(х, и),...
-
Системы массового обслуживания -- это такие системы, в которые в случайные моменты времени поступают заявки на обслуживание, при этом поступившие заявки...
-
Динамическое программирование Динамическое программирование -- один из разделов оптимального программирования, в котором процесс принятия решения и...
-
Методы отбора выборок - Основы научных исследований
Известны три метода отборок выборок: случайный, систематический и комбинированный. В результате случайного отбора получается случайная выборка. Выборка...
-
В начале пятилетнего периода работы предприятию выделена сумма в C руб. для приобретения нового оборудования. Стоимость одного комплекта оборудования...
-
Статистический характер экспериментальных исследований Любое экспериментальное исследование, в конечном итоге, сводится к изучению причинно-следственных...
-
При решении экономических задач часто анализировать ситуации, в которых сталкиваются интересы двух или более конкурирующих сторон, преследующих различные...
-
Задание для исследования - Численное нахождение корня уравнения методом Рунге-Кутта
Исследовать решение обыкновенных дифференциальных уравнений методом Рунге-Кутты. Подробное описание Метод этот пригоден для решения как одиночных...
-
Определение температуры плавления Температуру плавления определяем с помощью малогабаритного нагревательного стола типа "Boetinus" с наблюдательным...
-
Заключение - Основные методы и принципы моделирования в исследовании систем управления
В заключение данной курсовой работы хочу сделать несколько выводов из вышеизложенного материала о моделировании в исследовании систем управления. Итак,...
-
В большинстве случаев структурная неопределенность вызвана неполнотой знания аналитической структуры уравнений модели объекта управления. При не...
-
В практике управления системами различного назначения (экономическими, финансовыми, техническими и др.) неизбежно приходится сталкиваться с различными...
-
Методы исследования математических моделей - Математическое моделирование в менеджменте и маркетинге
Все методы математического моделирования можно разделить на четыре класса: -аналитические (априорные); -имитационные (априорно-апостериорные) модели;...
-
Методы исследования, Методика оживления и очистки культуры - Этапы получения лизина
В основу эксперимента положена методика культивирования бактерии продуцента лизина штамма B-11167 Corynebacterium glutamicum на основе сред, предложенных...
-
Объект и методы исследования, Объект исследования - Этапы получения лизина
Объект исследования Штамм Corynebacterium glutamicum B-11167 депонирован во Всероссийской коллекции промышленных микроорганизмов (ВКПМ) и имеет...
-
В основе моделирования лежит теория подобия, которая утверждает, что абсолютное подобие может иметь место лишь при замене одного объекта другим точно...
-
Метод дихотомии требует менее всего итераций цикла для получения корней уравнения с заданной точностью. Если расчет ведется без помощи ЭВМ, то это...
-
Важным для системного подхода является определение структуры системы -- совокупности связей между элементами системы, отражающих их взаимодействие....
-
Моделирование начинается с формирования предмета исследований -- системы понятий, отражающей существенные для моделирования характеристики объекта. Эта...
Кондуктометрическое титрование - Электрохимические методы исследования