Изоэлектрическая точка полиамфолита
Одной из отличительных особенностей высокомолекулярных соединении является гибкость их молекул. Длинные цепи макромолекул способны в растворах принимать различную форму в пределах от свернутого клубка до вытянутой палочки. Причиной гибкости макромолекул является относительная свобода вращения вокруг связи С-С в макроцепи.
Полиэлектролитами называются такие высокомолекулярные соединения, макромолекулы которых содержат ионогенные группы, способные к диссоциации на ионы. Полиамфолиты - это полиэлектролиты, которые содержат как основные, так и кислотные группы. Среди природных полиамфолитов наибольшее значение имеет белок.
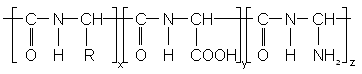
Рисунок 1. Строение белка
С увеличением концентрации раствора полиэлектролита вокруг зарядов на макромолекулах начинает формироваться диффузная оболочка противоионов, которая уменьшает электростатическое взаимодействие между зарядами, в результате чеки цепь приобретает конформацию клубка.
Наиболее ярко влияние зарядов проявляется при изучении вязкостных свойств полимеров. Рассмотрим зависимость вязкости раствора желатины от рН среды. Минимальной вязкостью обладают растворы в изоэлектрической точке - когда число диссоциированных кислотных групп равно числу диссоциированных основных, и при том минимально, вследствие чего заряд макромолекулы равен нулю.
При изменении рН относительно изоэлектрической точки, степень диссоциации ионогенных групп белка увеличивается. Увеличение рН приводит к диссоциации кислотных групп, а уменьшение рН ведет к диссоциации основных групп.
В обоих случаях цепь разворачивается в результате возникновения и отталкивания одноименных зарядов на ней. Это приводит к значительному возрастанию вязкости раствора. При достижении некоторых критических значений степени диссоциации, вязкость начинает уменьшаться. Это происходит из-за уменьшения электростатического отталкивания зарядов цепи вследствие их экранирования противоионами добавляемого электролита. изоэлектрический желатин полиамфолит водородный
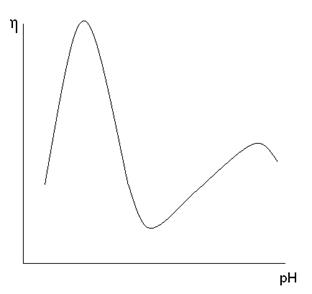
Рисунок 2. Вид зависимости вязкости раствора амфотерного полиэлектролита от рН среды
Практическая часть:
В данной работе мы определяли изоэлектрическую точку желатины путем измерения % светопропускания растворов желатины с различными значениями рН на фотоэлектрическом колориметре.
Был приготовлен 1% раствор желатины в количестве 220 г и в горяем виде отфильтрован через складчатый фильтр. После охлаждения до комнатной температуры в 8 пронумерованных колбочек отобрали по 25 мл раствора желатины, и растворы были доведены до нужных значений рН. После этого каждый из полученных растворов был исследован на фотоэлектрическом колориметре, и результаты были занесены в Таблицу 1.
Таблица 1. Результаты измерения % светопропускания раствора желатины при различных рН
|
№ |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
РН |
2,0 |
3,0 |
3,5 |
4,0 |
4,5 |
5,0 |
7,0 |
9,0 |
|
% светопропускания |
66,5 |
61 |
57 |
56,5 |
58 |
59 |
62 |
63 |
На основе полученных данных был построен график (Рис. 3)
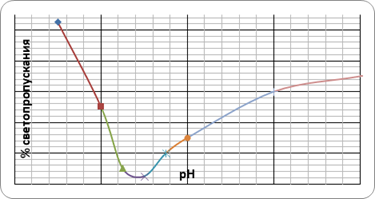
Рисунок 3. Зависимость % светопропускания раствора желатины от рН среды
Как видно из графика (Рис.3), изоэлектрическая точка желатины соответствует рН=3,9.
Вывод:
Значение рН, соответствующее изоэлектрической точке белка желатины, составляет 3,9.
Список литературы
- 1. Ю. Д. Семчиков, С. Д. Зайцев. Введение в химию и физику полимеров. - Изд-во ННГУ, Нижний Новгород, 2007. 2. А. М. Шур. Высокомолекулярные соединения. - Химия, М., 1971. 3. А. А. Тагер. Физико-химия полимеров. - Химия, М., 1978. 4. С. С. Воюцкий. Курс коллоидной химии. - Химия, М., 1976.
Похожие статьи
-
Принципы получения гибридных соединений на основе квантовых точек и органических хромофоров В литературе для получения соединений, обладающих...
-
Сложение, вычитание, умножение комплексных чисел в алгебраической форме производят по правилам соответствующих действий над многочленами. Четность и...
-
На рис. 20 представлены спектры поглощения растворов КТ и лиганда в хлороформе в присутствии HCl. Оптическая плотность КТ максимальна на длине волны 363...
-
Гибридные системы на основе квантовых точек (КТ) и органических лигандов могут быть использованы в качестве хемо-, био - и фотосенсоров, а также...
-
С кислородом большинство металлов образует оксиды - амфотерные и основные: 4Li + O2 = 2Li2O, 4Al + 3O2 = 2Al2O3. Щелочные металлы, за исключением лития,...
-
Геометрический объект любой сложности можно рассматривать как геометрическое место точек, по взаимному расположению, которых можно составить...
-
Непрерывность композиции, Точки разрыва - Свойства функций
Пусть задана функция, со значениями в, и на множестве определена функция со значениями в. Тогда для любого можно вычислить, на можно определить функцию...
-
Спектральные и фотохимические характеристики исходных веществ Спектральные свойства 2-(4-[9-меркаптононокси] стирил) хинолина и квантовой точки CdS На...
-
Изменение люминесценции гибридных систем, состоящих из квантовой точки и фотохромного лиганда, возможно не только за счет химического воздействия, но и...
-
Бериллий с точки зрения металлурга - Бериллий
Свойства бериллия чаще всего именуются "удивительными", "чудесными" и т. п. Отчасти это справедливо, причем главная "удивительность" заключается в...
-
Бериллий с точки зрения биолога и медика - Бериллий
Бериллий обнаружен в растениях, произрастающих на бериллийсодержащих почвах, а также в тканях и костях животных. Но если для растения бериллий безвреден,...
-
УРАВНЕНИЕ ПРЯМОЙ НА ПЛОСКОСТИ На плоскости, заметим, могут быть заданы только двухмерные, или плоские преобразования. Уравнение, связывающее две...
-
ВЗАИМНОЕ РАСПОЛОЖЕНИЕ ТОЧКИ И ПЛОСКОСТИ - Основы моделирования геометрических объектов
Возможны два варианта взаимного расположения точки и плоскости: либо точка принадлежит плоскости, либо нет. Если точка принадлежит плоскости то из трех...
-
ВЗАИМНОЕ РАСПОЛОЖЕНИЕ ТОЧКИ И ПРЯМОЙ - Основы моделирования геометрических объектов
Если точка принадлежит прямой, то ее проекции должны принадлежать одноименным проекциям этой прямой (аксиома принадлежности точки прямой). Из четырех...
-
ВЗАИМНОЕ РАСПОЛОЖЕНИЕ ТОЧЕК - Основы моделирования геометрических объектов
Можно выделить три основных варианта взаимного расположения точек: 1. Пусть точки А и В (рис.2.5) расположены в первой четверти так, что: - YА>YВ. Тогда...
-
В практике изображения различных геометрических объектов, чтобы сделать проекционный чертеж более ясным, возникает необходимость использовать третью -...
-
Точки розриву і їхня класифікація. Теореми про безперервні функції - Основи вищої математики
Якщо функція F така, що для неї існують межі F ( А +0) і F ( А --0), однак F ( А ) F ( А +0) F ( А --0), то, мабуть, вона нерозривна (не безперервна) у...
-
Классификация с различных точек зрения, Классификация по целевому назначению. - Виды моделей
Классификация моделей может быть проведена с различных точек зрения. Рассмотрим некоторые из них. Классификация по целевому назначению. Модели структуры...
-
Определим сначала максимальные (оптимальные) нормализованное значения по каждому из трех нормализованных критериев: F(ХI=1) = 1; f(ХI=2) = 1; f(ХI=3) =...
-
Модель с определением точки заказа - Экономико-математические модели управления запасами
В реальных ситуациях следует учитывать время выполнения заказа Q. Для обеспечения бесперебойного снабжения заказ должен подаваться в момент, когда...
-
Теория Периодической Системы была преимущественно создана Н. Бором (1913-21) на базе предложенной им квантовой модели атома. Учитывая специфику изменения...
-
Бериллий с точки зрения химика - Бериллий
Типично амфотерен, т. е. обладает свойствами и металла, и неметалла. Однако металлические свойства все же преобладают. С водородом бериллий не реагирует...
-
Бериллий с точки зрения физика - Бериллий
В истории многих элементов есть особые вехи - открытия, после которых значение этих элементов неизмеримо возрастает. В истории бериллия таким событием...
-
Бериллий с точки зрения геолога - Бериллий
Типично редкий элемент. На тонну земного вещества в среднем приходится лишь 4,2 г бериллия. Это, конечно, очень немного, но и не так уж мало, если...
-
ГИДРОЛИЗ СОЛЕЙ - Характеристика основных видов растворов
Гидролизом называется обменная реакция между веществом и водой. При гидролизе обычно происходит изменение реакции среды. Если гидролиз не сопровождается...
-
Характеристика ионов хрома - Оценка показателей количественного содержания хрома в реке Москва
Соединения хрома являются тяжелыми металлами, в поверхностные воды попадают при выщелачивании из пород, некоторые количества поступают из почв в процессе...
-
Свойства и важнейшие характеристики - Полимеры
Линейные полимеры обладают специфическим комплексом физико-химических и механических свойств. Важнейшие из этих свойств: способность образовывать...
-
Круговорот углерода связан с использованием СО при фотосинтезе; в процессе дыхания растение возвращает СО в атмосферу. Животные, поедая растения,...
-
Строение и свойства простагландинов - Простагландины. Строение. Биороль
ПРОСТАГЛАНДИНЫ (PG), биологически активные липиды, представляющие собой производные гипотетич. про-становой к-ты (ф-ла I) и различающиеся положением...
-
Свойства и важнейшие характеристики. - Полимерные соединения
Линейные полимеры обладают специфическим комплексом физико-химических и механических свойств. Важнейшие из этих свойств: способность образовывать...
-
Физические свойства - Свойства аминокислот
Аминокислоты -- бесцветные кристаллические вещества, хорошо растворимые в воде. Многие из них обладают сладким вкусом. Химические свойства: Все...
-
Одноатомные насыщенные спирты, Изомерия - Спирты и фенолы
Спирты классифицируют на первичные, вторичные и третичные в зависимости оттого, с каким атомом углерода (связана гидроксильная группа). Атом углерода...
-
Реакции ионного обмена - это реакции между ионами, образовавшимися в результате диссоциации электролитов. Правила составления ионных уравнений реакций 1....
-
Спектральные свойства нейтральной формы гибридного соединения QD-L На рис. 28 представлены спектры поглощения растворов исходных квантовых точек CdS...
-
В 1974г. группа аргентинских ученых во главе с профессором А. Эррерой получила предварительные результаты работы над латиноамериканской моделью...
-
Рассмотрим простейший гальванический элемент Даниэля-Якоби, состоящий из двух полуэлементов - цинковой и медной пластин, помещенных в растворы сульфатов...
-
Практическое применение - Методы осаждения
Наиболее широкое применение в практике имеет метод Фоль-гарда (тиоцианатометрия), с помощью которого находят содержа-ние галогенидов в кислой среде....
-
ПРЕВРАЩЕНИЯ ВЕЩЕСТВ. - Строение и превращение веществ
Для получения разнообразных веществ применяются как физические, так и химические методы. К первым относятся, например, растворение в воде, фильтрование и...
-
Если брать за основу качественный состав молекул, то все рассматриваемые вещества можно определить в три группы. - Органические - это те, в состав...
-
Применение, Биологическая роль - Сера и ее роль в жизни
Около половины производимой серы используется на производство серной кислоты, около 25% расходуется для получения сульфитов, 10-15% -- для борьбы с...
Изоэлектрическая точка полиамфолита