АКТИВНЫЙ ЦЕНТР ФЕРМЕНТОВ - Аминокислоты и ферменты
При изучении механизма химической реакции, катализируемой ферментами, исследователя всегда интересует не только определение промежуточных и конечных продуктов и выяснение отдельных стадий реакции, но и природа техфункциональных групп в молекуле фермента, которые обеспечивают специфичность действия фермента на данныйсубстрат (субстраты) и высокую каталитическую активность. Речь идет, следовательно, о точном знании геометрии и третичной структуры фермента, а также химической природы того участка (участков) молекулы фермента, который обеспечивает высокую скорость каталитической реакции. Участвующие в ферментативных реакциях молекулысубстратов часто имеют небольшие размеры по сравнению с молекулами ферментов, поэтому было высказано предположение, что при образовании фермент-субстратных комплексов в непосредственный контакт с молекулойсубстрата, очевидно, вступает ограниченная часть аминокислот пептидной цепи. Отсюда возникло представление обактивном центре фермента. Под активным центром подразумевают уникальную комбинацию аминокислотных остатков в молекуле фермента, обеспечивающую непосредственное связывание ее с молекулой субстрата и прямое участие в акте катализа (рис. 4.2). Установлено, что у сложных ферментов в состав активного центра входят также просте-тические группы.
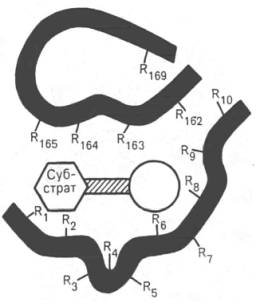
Активный центр фермента (схема) (по Малеру и Кордесу).
Темные полосы - участки полипептидной цепи фермента; R - аминокислотные остатки и их порядковые номера (с N-конца).
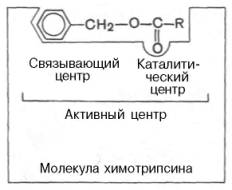
В активном центре условно различают так называемый каталитический центр, непосредственно вступающий в химическое взаимодействие с субстратом, и связывающий центр, или контактную ("якорную") площадку, которая обеспечивает специфическое сродство к субстрату и формирование его комплекса с ферментом. В свою очередьмолекула субстрата также содержит функционально различные участки: например, субстраты эстераз или протеиназ - одну специфическую связь (или группу атомов), подвергающуюся атаке со стороны фермента, и один или несколько участков, избирательно связываемых ферментом.
Получены экспериментальные доказательства наличия в активном центре химотрипсина двух остатков гистидина и остатка серина, схематически представленных в трехмерной структурной модели предшественника этого фермента(рис. 4.3). Выявление химической природы и вероятной топографии групп активного центра - проблема первостепенной важности. Она сводится к определению природы аминокислот, их последовательности и взаиморасположения в активном центре. Для идентификации так называемых существенных аминокислотных остатков используют специфические ингибиторы ферментов (часто это субстратподобные вещества или аналогикоферментов), методы "мягкого" (ограниченного) гидролиза в сочетании с химической модификацией, включающей избирательное окисление, связывание, замещение остатков аминокислот и др.
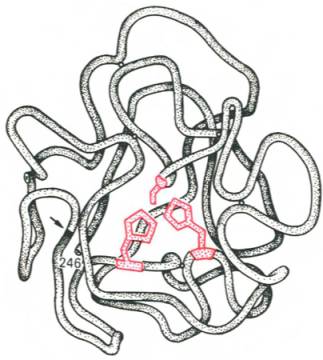
Гипотетическая модель третичной структуры молекулы предшественника химотрипсина (по Ней-рату). Цветом выделены остатки серина и гисти-дина; стрелкой обозначено место отщепления N-концевого участка полипептидной цепи.
При помощи методов ингибиторного анализа были предприняты попытки установить закономерности состава и структуры активных центров у ферментов, относящихся к разным группам. В частности, при использованиидиизопропилфторфосфата (ДФФ), принадлежащего к так называемым нервным ядам, наблюдается полное выключение активного центра холинэстеразы - фермента, катализирующего гидролиз ацетилхолина на холин иуксусную кислоту. Оказалось, что этот ингибитор имеет близкое структурное сходство с ацетилхолином и подобно ему взаимодействует с ОН-группой остатка серина в активном центре. Вызывая фосфорилирование серина в активном центре ряда других ферментов, ДФФ также инактивирует их действие:
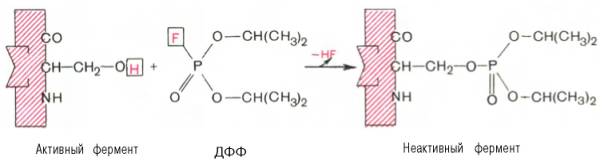
Показано, что ДФФ избирательно фосфорилирует в каждом чувствительном к нему ферменте только один остатоксерина, наделенный функциональной активностью. Учитывая этот механизм действия ДФФ, сделаны попытки определения природы аминокислот в окружении "каталитического" остатка серина у ряда ферментов (табл. 4.2).
Из данных табл. 4.2 видно, что ферменты, сходные по типу действия, хотя и различаются специфичностью, могут иметь почти одинаковую последовательность аминокислотных остатков в тех участках, которые примыкают к остаткусерина, несущему функционально активную гидро-ксильную группу. Существенное значение ОН-группы серина дляакта катализа было доказано, кроме того, химическим ее блокированием или удалением, когда эстеразы полностью лишались ферментативной активности.
Предполагают, что формирование активного центра фермента начинается уже на ранних этапах синтеза белка-фермента (см. главу 14) на рибосоме, когда линейная одномерная структура пептидной цепи превращается в трехмерное тело строго определенной конфигурации. Образовавшийся белок приобретает информацию совершенно нового типа, а именно функциональную (в частности, каталитическую). Любые воздействия, приводящие кденатурации, т. е. нарушению третичной структуры, приводят к искажению или разрушению структуры активного центра и соответственно потере ферментом каталитических свойств. Если при подходящих внешних условиях удается восстановить нативную трехмерную структуру белка-фермента (ренатурировать его), то восстанавливается и его каталитическая активность. Это было показано впервые на примере рибо-нуклеазы поджелудочной железы (см. рис. 1.13).

Помимо активного центра, в молекуле фермента может присутствовать также аллостерический центр (или центры) (от греч. allos - другой, иной и steros - пространственный, структурный), представляющий собой участок молекулыфермента, с которым связываются определенные, обычно низкомолекулярные, вещества (эффекторы, или модификаторы), молекулы которых отличаются по структуре от субстратов. Присоединение эффектора к аллостерическому центру изменяет третичную и часто также четвертичную структуру молекулы фермента и соответственно конфигурацию активного центра, вызывая снижение или повышение энзимати-ческой активности. Ферменты, активность каталитического центра которых подвергается изменению под влиянием аллостерических эффекторов, связывающихся с аллостерическим центром, получили название аллосте-рических ферментов.
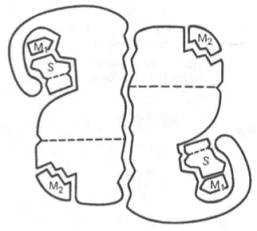
Схематическое изображение аллостерического фермента, состоящего из двух протомеров, соединенных по типу гетерологи-ческой ("голова"-"хвост") ассоциации (по Кошленду). S - субстрат; М1 - модификатор, связывающийся в активном центре; М2 - модификатор, связывающийся в аллосте-рическом центре (эффектор).
Отличительной особенностью ряда аллостерических ферментов является наличие в молекуле олигомерногофермента нескольких активных центров и нескольких аллостерических регуляторных центров, пространственно удаленных друг от друга. В аллостерическом ферменте каждый из двух симметрично построенных протомеров содержит один активный центр, связывающий субстрат S, и один аллостерический центр, связывающий эффектор М2, т. е. 2 центра в одной молекуле фермента (рис. 4.4). Получены доказательства, что для субстратааллостерические ферменты, помимо активного центра, содержат и так называемые эффекторные центры; при связывании с эффекторным центром субстрат не подвергается каталитическому превращению, однако он влияет на каталитическую эффективность активного центра. Подобные взаимодействия между центрами, связывающимилиганды одного типа, принято называть гомотропными взаимодействиями, а взаимодействия между центрами, связывающими лиганды разных типов, - гетеротропными взаимодействиями.
Таким образом, приведенные сведения о химической природе активного центра и аллостерических участках свидетельствуют о том, что в энзима-тическом катализе, как и в реакции связывания субстрата, участвует не ограниченная и небольшая часть фермента, как предполагалось ранее, а значительно большая часть молекулыбелка-фермента. Этими обстоятельствами, вероятнее всего, можно объяснить большие размеры и объемность трехмерной структуры молекулы фермента; эти же обстоятельства следует учитывать в программах создания искусственных низкомолекулярных аналогов ферментов (синзимов), обладающих свойствами на-тивных ферментов(см. ранее).
Похожие статьи
-
СТРОЕНИЕ ФЕРМЕНТОВ - Аминокислоты и ферменты
В природе существуют как простые, так и сложные ферменты. Первые целиком представлены полипептидными цепями и при гидролизе распадаются исключительно на...
-
ХИМИЧЕСКАЯ ПРИРОДА ФЕРМЕНТОВ - Аминокислоты и ферменты
В настоящее время получены неопровержимые экспериментальные доказательства белковой природы ферментов. Трудно сейчас представить, что не только Р....
-
Высокая каталитическая эффективность. Отличительной особенностью любого фермента является его чрезвычайно высокая каталитическая эффективность. Так,...
-
КРАТКАЯ ИСТОРИЯ РАЗВИТИЯ УЧЕНИЯ О ФЕРМЕНТАХ - Аминокислоты и ферменты
Явления брожения и переваривания известны с незапамятных времен, однако зарождение учения о ферментах(энзимология) относится к первой половине XIX в....
-
Использование предшественников при производстве аминокислот позволяет успешно обходить метаболический контроль, осуществляющийся по механизму обратной...
-
ПОНЯТИЕ О ФЕРМЕНТАХ - Аминокислоты и ферменты
Аминокислота фермент реакция Ферменты, или энзимы, представляют собой высокоспециализированный класс веществ белковой природы, используемый живыми...
-
Літературний огляд, Властивості ферментів - Вплив температури на амілолітичну активність
Властивості ферментів Ферменти - термолабільні сполуки. Це означає, що під дією високих температур вони денатурують. Спочатку при підвищенні температури...
-
Энергетический профиль каталитической реакции - Гомогенный и гетерогенный катализ
Энергетический профиль реакции - это кривая, которая показывает зависимость координаты реакции (насколько прошла реакция) от времени (при постоянном...
-
Реакции аминокислот - Способы получения аминокислот
Большинство реакций, в которые аминокислоты вступают в лабораторных условиях (in vitro), свойственны всем аминам или карбоновым кислотам. 1. образование...
-
КАТАЛИЗ В БИОХИМИИ - Процесс катализа
Ферментативный катализ неразрывно связан с жизнедеятельностью организмов растительного и животного мира. Многие жизненно важные химические реакции,...
-
Физические свойства - Свойства аминокислот
Аминокислоты -- бесцветные кристаллические вещества, хорошо растворимые в воде. Многие из них обладают сладким вкусом. Химические свойства: Все...
-
Оптически активные соединения с одним асимметрическим атомом Рис.1. Энантиомерыбутанола-2 При рассмотрении пространственной модели бутанола-2 (рис.1.)...
-
В 2005 году В. Б. Спиричевым предложена новая классификация витаминов, основанная на характере их специфических функций (функциональная классификация) В...
-
1). Изменения жира молока при тепловой обработке. 2). Изменение лактозы при тепловой работке. 3). Влияние нагревания на солевой состав, витаминный и...
-
Химические свойства аминокислот - Способы получения аминокислот
Все - аминокислоты, кроме глицина, содержат хиральный - углеродный атом и могут встречаться в виде энантиомеров: Было доказано, что почти все природные -...
-
Способы получения аминокислот - Способы получения аминокислот
1. Гидролизом белков можно получить около 25 аминокислот, но полученную смесь трудно разделить. Обычно одна или две кислоты получаются в значительно...
-
Аминокислоты - Способы получения аминокислот
Любое соединение, которое содержит одновременно карбоксильную и аминогруппу, является аминокислотой. Однако, чаще этот термин применяется для обозначения...
-
Электролиз - физико-химический процесс, состоящий в выделении на Электродах составных частей растворенных веществ или других веществ, который возникает...
-
Вода реагирует с некоторыми кислотными и основными оксидами, давая гидроксид - соответственно кислоту или основание: Н2О + CaO = Ca(OH)2 основание H2O +...
-
Исследования, направленные на выяснение как материального состава растительных и животных тканей, так и химических процессов, происходящих в организме,...
-
Все аминокислоты, из которых состоят белки, являются" L-а-амино - (или имино-) кислотами. Они находят применение как пищевые добавки, приправы, усилители...
-
Введение - Свойства аминокислот
Аминокисломты (аминокарбомновые кисломты) -- органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные группы....
-
Імітаційне комп'ютерне моделювання процесу організації підприємницького інноваційного центру за допомогою програмного пакету "Ithink" В статті робиться...
-
В количественном отношении белки занимают первое место среди всех содержащихся в живой клетке макромолекул; на их долю приходится не менее половины...
-
Кислотно-основные свойства аминокислот - Способы получения аминокислот
Аминокислоты - амфотерные вещества, которые могут существовать в виде катионов или анионов. Это свойство объясняется наличием как кислотной (-СООН), так...
-
Строение аминокислот - Оптические изомеры и их влияние на организм человека
Принцип построения б - аминокислот, т. е. нахождение у одного и того же атома углерода двух различных функциональных групп, радикала и атома водорода,...
-
Опис впливу температури на активність ферменту - Вплив температури на амілолітичну активність
Однією з характерних властивостей ферментів є їх термолабільність, тобто чутливість до змін температури. У відповідності до закону Вант-Гофа, швидкість...
-
Температура, при якій фермент має максимальну активність, називається оптимальною температурою ферменту. Інтерес представляють дані про вплив на...
-
СИНТЕЗ ВЫСОКОМОЛЕКУЛЯРНЫХ СОЕДИНЕНИЙ - Пластические массы и изделия на их основе
Природные (естественные) органические высокомолекулярные соединения образуются в процессе биосинтеза в клетках растений и живых организмов и для...
-
При приготуванні дріжджового тіста дріжджі розкладають крохмаль з допомогою амілази до ди - і трисахаридів, які потім використовуються у життєвій...
-
Общее понятие о цепных реакциях и автокатализе - Принципы горения и взрыва
К цепным реакциям относят реакции, протекающие с образованием свободных радикалов, способных превращать реагенты в конечные продукты, поддерживая...
-
Целью данного раздела является уточнение баланса активной и реактивной мощностей в сети с учетом уточненных значений потерь активной и реактивной...
-
КАТАЛИЗ - процесс, заключающийся в изменении скорости химических реакций в присутствии веществ, называемых катализаторами. Катализаторы - вещества,...
-
Баланс активной и реактивной мощностей - Расчет электрической сети микрорайона в г. Иркутск
Нагрузка электроснабжение потребитель трансформатор Определить нагрузки подстанций при следующих исходных данных: Таблица 1.3 - Исходные расчетные данные...
-
ВИДНЫЕ ДЕЯТЕЛИ ХИМИИ О КАТАЛИЗЕ - Процесс катализа
И. Берцелиус (1837): "Известные вещества оказывают при соприкосновении с другими веществами такое влияние на последние, что возникает химическое...
-
Гомогенный и гетерогенный катализ - Систематика химических элементов
Вещества, увеличивающие скорость химической реакции, называются Катализаторами. Явление возрастания скорости реакции под действием таких веществ,...
-
Рис.2. Стереоизомеры хлоряблочной кислоты Если в молекуле имеется несколько (n) асимметрических центров, то в общем случае число оптических изомеров...
-
Площа плоскої області обчислюється за формулою (6) У полярній системі координат формула (6) має вигляд (7) Об'єм циліндричного тіла, обмеженою зверху...
-
Превращение аренов - Каталитический риформинг
Каталитический риформинг алкан газ Незамещенные соединения в условиях процесса риформинга устойчивы. Метилзамещенные арены (толуол, ксилолы) подвергаются...
-
Обеспечение потребителей активной и реактивной мощности Наибольшая суммарная активная мощность, потребляемая в проектируемой сети, составляет: Где -...
АКТИВНЫЙ ЦЕНТР ФЕРМЕНТОВ - Аминокислоты и ферменты