Властивості нітратної і фосфатної кислоти
Властивості Нітратної і Фосфатної кислоти
Нітратна кислота. Чиста Нітратна кислота HNO - безбарвна рідина густиною 1,51 р/см при - 42 °С застигаюча в прозору кристалічну масу. На повітрі вона, подібно концентрованій соляній кислоті, "димить", тому що пари її утворять із вологою повітря дрібні крапельки туману.
Нітратна кислота не відрізняється тривкістю, Вже під впливом світла вона поступово розпадається:
Чим вище температура і чим концентрованіше кислота, тим швидше йде розпад. Диоксид азоту, що виділяється, розчиняється в кислоті і надає їй буре фарбування.
Нітратна кислота належить до числа найбільше сильних кислот; у розведених розчинах вона цілком розпадається на іони Н та - NO.
Окисні властивості нітратної кислоти. Характерною властивістю нітратної кислоти є її яскраво виражена окисна здібність. Нітратна кислота--один з енергійніших окислювачів. Багато які неметали легко окисляються нею, перетворюючись у відповідні кислоти. Так, сірка при кип'ятінні з нітратною кислотою поступово окисляється в сульфатну кислоту, фосфор - у фосфатну. Тліюче вугіллячко, занурено у концентровану HNO, яскраво розпалюється.
Нітратна кислота діє майже на всі метали (за винятком золота, платини, тантала, родія, ірідія), перетворюючи їх у нітрати, а деякі метали--в оксиди.
Концентрована HNO пасивує деякі метали. Ще Ломоносов відкрив, що залізо, що легко розчиняється в розведеній нітратній кислоті, не розчиняється в холодний концентрованій HNO. Пізніше було встановлено, що аналогічна дія Нітратна кислота робить на хром і алюміній. Ці метали переходять під дією концентрованої нітратної кислоти в пасивний стан.
Ступінь окисленості азоту в нітратній кислоті дорівнює 4-5. Виступаючи в якості окислювача, НNО може відновлятися до різноманітних продуктів:

Яке з цих речовин утвориться, тобто наскільки глибоко відновляється Нітратна кислота в тому або іншому випадку, залежить від природи відновлювача і від умов реакції, насамперед від концентрації кислоти. Чим вище концентрації HNO, тим менше глибоко вона відновляється. При реакціях із концентрованою кислотою частіше усього виділяється. При взаємодії розведеної нітратної кислоти з малоактивними металами, наприклад, із міддю, виділяється NO. У випадку більш активних металів - залоза, цинку, - утвориться. Сильно розведена Нітратна кислота взаємодіє з активними металами-- цинком, магнием, алюмінієм -- з утворенням іона амонію, що дає з кислотою нітрат амонію. Звичайно одночасно утворяться декілька продуктів.
Для ілюстрації призведемо схеми реакцій окислювання деяких металів нітратною кислотою;
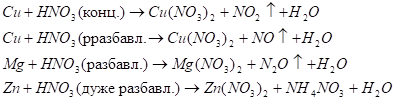
При дії нітратної кислоти на метали водень, як правило, не виділяється.
При окислюванні неметалів концентрована Нітратна кислота, як і у випадку металів, відновляється до, наприклад
Більш розведена кислота звичайно відновляється до NO, наприклад:
Приведені схеми ілюструють найбільше типові випадки взаємодії нітратної кислоти з металами і неметалами. Взагалі ж, окисно-відбудовні реакції, що йдуть за участю, протікають складно.
Суміш, що складається з 1 обсягу нітратної і 3-4 обсягів концентрованої соляної кислоти, називається Царською горілкою. Царська горілка розчиняє деякі метали, що не взаємодіють з нітратною кислотою, у тому числі і "царя металів"-золото. Дія її пояснюється тим, що Нітратна кислота окисляє соляну з виділенням вільного хлору й утворенням Хлороксида азоту(III), або Хлорида нитрозила, :
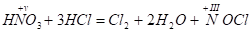
Хлорид нитрозила є проміжним продуктом реакції і розлигається:
Хлор у момент виділення складається з атомів, що й обумовлює високу окисну спроможність царської горілки. Реакції окислювання золота і платини протікають в основному відповідно до таких рівнянь.
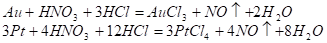
З надлишком соляної кислоти хлорид золота(III) і хлорид платини (IV) утворять комплексні сполуки
На багато органічних речовин Нітратна кислота діє так, що один або декілька атомів водню в молекулі органічної сполуки заміщаються нитрогрупами. Цей процес називається нитрованням і має велике значення в органічній хімії.
Нітратна кислота - одна з найважливіших сполук азоту: у великих кількостях вона витрачається у виробництві, азотних добрив, вибухових речовин і органічних барвників, служить окислювачем у багатьох хімічних процесах, використовується у виробництві сірчаної кислоти по нитрозному засобі, застосовується для виготовлення целюлозних лаків, кіноплівки.
3. Нітрати. Солі нітратної кислоти називаються нітратами. Всі вони добре розчиняються у воді, а при нагріванні розлигаються з виділенням кисню. При цьому нітрати найбільше активних металів переходять у нітрити:
Нітрати більшості інших металів при нагріванні розпадаються на оксид металу, кисень і диоксид азоту. Наприклад:
Нарешті, нітрати найменш активних металів (наприклад, срібла, золота) разлагаются при нагріванні до вільного металу:
Легко відчіплюючи кисень, нітрати при високій температурі є енергійними окислювачами. Їхні водяні розчини, навпроти, майже не виявляють окисних властивостей.
Найбільше важливе значення мають нітрати натрію, калію, амонію і кальцію, що на практику називаються селітрами.
Нітрат натрію або Натрієвої селітри, Іноді називана також Чилійською селітрою, зустрічається у великій кількості в природі тільки в Чилі.
Нітрат калію , або Калійна селітра, у невеличких кількостях також зустрічається в природі, але головним чином утворюється штучно при взаємодії нітрату натрію з хлоридом калію.
Обидві цієї солі використовуються в якості добрив, причому нітрат калію містить дві необхідних рослини елемента: азот і калій. Нітрати натрію і калію застосовуються також при скловарінні й у харчовій промисловості для консервування продуктів.
Нітрат кальцію або Кальцієвої селітри, утворюється у великих кількостях нейтралізацією нітратної кислоти вапном; застосовується як добриво.
4. Промислове отримання нітратної кислоти. Сучасні промислові засоби одержання нітратної кислоти засновані на каталітичному окислюванні аміаку киснем повітря. При" описі властивостей аміаку було зазначено, що він горить у кисні, причому продуктами реакції є вода і вільний азот. Але при каталізаторів - окислювання аміаку киснем може протікати інакше. Якщо пропускати суміш аміаку з повітрям над каталізатором, то при 750 °С і визначеному складі суміші відбувається майже повне перетворення
, що отримався легко переходить у, що із водою при кисню повітря дає нітратну кислоту.
У якості каталізаторів при окислюванні аміаку використовують сплави на основі платини.
Одержувана окислюванням аміаку Нітратнакислота має концентрацію, що не перевищує 60%. При необхідності її концентрують,
Промисловістю випускається розведена Нітратнакислота концентрацією 55, 47 і 45%, а концентрована-98 і 97%, Концентровану кислоту перевозять в алюмінієвих цистернах, розведену - у цистернах із кислотоупорній сталі.
5. Кругооберт азоту в природі. При гнитті органічних речовин значна частина азоту, що утримується в них, перетворюється в аміак, що під впливом живучих у грунті бактерій, що нітрифицируюють, окисляється потім в нітратну кислоту. Остання, вступаючи в реакцію з карбонатами, що находялись у грунті, наприклад із карбонатом кальцію, утворює нітрати
Деяка ж частина азоту завжди виділяється при гнитті у вільному виді в атмосферу. Вільний азот виділяється також при горінні органічних речовин, при запалюванні дров, кам'яного вугілля, торфу. Крім того, існують бактерії, що при недостатньому доступі повітря можуть віднімати кисень від нітратів, руйнуючи їх із виділенням вільного азоту. Діяльність цих бактерій, що денітрифицируюють, призводить до того, що частина азоту з доступної для зелених рослин форми (нітрати) переходить у недоступну (вільний азот). Таким чином, далеко не весь азот, що входив до складу загиблих рослин, повертається обернено в грунт; частина його поступово виділяється у вільному виді.
Безупинний збиток мінеральних азотних сполук давно повинен був би призвести до повного припинення життя на Землі, якби в природі не існували процеси, що відшкодовують втрати азоту. До таких процесів належать електричні розряди, що відбуваються насамперед в атмосфері, при яких завжди утвориться деяка кількість оксидів азоту; останні з водою дають нітратну кислоту, що перетворюється в грунті в нітрати. Другим джерелом поповнення азотних сполук грунту є життєдіяльність так званих азотобактерій, спроможних засвоювати атмосферний азот. Деякі з цих бактерій поселяються на коренях рослин із сімейства бобових, викликаючи утворення характерних вздуть - "клубеньків", чому вони й одержали назву клубенькових бактерій. Засвоюючи атмосферний азот, клубенькові бактерії переробляють його в азотні сполуки, а рослини, у свою чергу, перетворюють останні у білки й інші складні речовини.
Таким чином, у природі відбувається безупинний кругооберт азоту. Проте щорічно з врожаєм з полів убираються найбільше багаті білками частини рослин, наприклад зерно. Тому в грунт необхідно вносити добрива, що відшкодовують збиток у ній найважливіших елементів харчування рослин.
Вивчення питань харчування рослин і підвищення врожайності останніх шляхом застосування добрив є предметом спеціальної галузі хімії, що одержала назву агрохімії.
Оксид фосфору (V) P4O10, взаємодіючи з водою, утворює триметафосфатну кислоту H3(PO3)3 (спрощено її формулу часто пишуть HPO3); остання при кип'ятінні з надлишком води утворює фосфатну кислоту H3PO4; при нагріванні H3PO4 утворюється дифосфатна кислота H4P2O7:
3P4O10 + 6H2O = 4H3(PO3) 3
H3(PO3) 3 + 3H20 = 3H3PO4
2H3PO4 = H4P2O7 + H2O
Найбільше практичне значення має фосфатна кислота, тому що її солі - фосфати - використовуються в якості добрив.

Фосфатна кислота - Біла кристалічна речовина. З водою мішається в будь-яких співвідношеннях. На відміну від азотної кислоти не є окислювачем і не розпадається при нагріванні, що пояснюється найбільшою стійкістю ступеня окислювання +5 із усіх можливих для фосфору. До складу фосфатної кислоти входять три атоми гідрогену, чотири атоми оксигену й одного фосфору - H3PO4.
Форма молекули фосфатної кислоти
У промисловості фосфатна кислота утворюється двома способами: екстракційним і термічним.
У першому способі здрібнений фосфат кальцію опрацьовують сульфатною кислотою:
Ca3(PO4)2 + 3H2SO4 = 2H3PO4 + 3CaSO4"
CaSO4 випадає у виді осаду, а кислота залишається в розчині. Разом із кислотою в розчин переходять багато домішків - сульфати заліза, алюмінію й ін. Така кислота йде на виробництво добрив.
У другому способі спочатку одержують фосфор (відновленням природного фосфору в електропічі). Потім його окисляють до оксиду P4O10, а останній сполучають з водою й одержують чисту кислоту (масова частка 80%).
Хімічні властивості фосфатної кислоти. Фосфатна кислота активна речовина. Реагує з багатьма речовинами.
Тому що фосфатна кислота багатооосновна, її дисоціація протікає ступінчато. Головним чином по першій ступені, в меншім по другий і лише в незначній мірі - по третій. Тому у водяному розчині фосфатної кислоти поряд із молекулами H3PO4 є іони (у кількостях, що послідовно зменшуються,) H2PO4Й, HPO4ІЙ и PO4іЙ:
H3PO4 Ф Н+ + H2PO4ї (перша ступінь)
H2PO4Й Ф Н+ + HPO4ІЙ (друга ступінь)
HPO4ІЙ Ф Н+ + PO4іЙ (третя ступінь)
Взаємодія з металами:
6Na + 2H3PO4 = 2Na3PO4 + 3H2 m
Взаємодія з оксидами:
3CaO + 2H3PO4 = Ca3(PO4)2 " + 3H2O
Взаємодія з основами:
H3PO4 + 3KOH = K3PO4 + 3H2O
- 3Н+ + PO4іЙ+ 3K++3OHЙ = 3K+ + PO4іЙ + 3H2O 3Н++3OHЙ = 3H2O
Взаємодія із солями:
2H3PO4 + 3Na2CO3 = 2Na3PO4 + 3CO2' + 3H2O
Фосфатна кислота витискує більш сильну кислоту з розчину:
3Ca(NO3)2 + 2H3PO4 = Ca3(PO4)2" + 6HNO3
CaІ+ + 6NO3Й + 2H3PO4 = Ca3(PO4)2" + 6Н+ + 6NO3Й
CaІ+ + 2H3PO4 = Ca3(PO4)2"+ 6Н+
7. Специфічна властивість:
H3PO4 + 3AgNO3 = Ag3PO4" + 3HNO3
3Н++ PO4іЙ+ 3Ag++ 3NO3Й = Ag3PO4" + 3Н++ 3NO3Й
PO4іЙ+ 3Ag+ = Ag3PO4"
Солі фосфатної кислоти. У молекулі фосфатної кислоти атоми гідрогену сполучені з атомами оксигену: H
Похожие статьи
-
ЗВ'ЯЗКИ - Амінокислоти: одержання, властивості, роль у біології
Амінокислоти здатні утворювати ряд хімічних зв'язків з різними реакційноздатними групами. Пептидний зв'язок . Цей зв'язок утворюється в результаті...
-
Фізичні властивості, ХІМІЧНІ ВЛАСТИВОСТІ - Амінокислоти: одержання, властивості, роль у біології
Амінокислоти-безбарвні кристалічні речовини з високими температурами плавлення, які мало відрізняються для цих кислот і тому не характерні. Плавлення...
-
АМІНОКИСЛОТИ, ІЗОМЕРІЯ. НОМЕНКЛАТУРА - Амінокислоти: одержання, властивості, роль у біології
Органічні сполуки, що містять в молекулі карбоксильну та аміно групи, називають - амінокислотами. Амінокислоти мають надзвичайно велике значення в...
-
Хімічні сполуки титану - Титан та його властивості
З одновалентними галогенами (фтором, бромом, хлором і йодом) він може утворювати ди - три - і, тетраз'єднання, із сіркою й елементами її групи (селеном,...
-
ШЛЯХИ ОТРИМАННЯ АМІНОКИСЛОТ - Амінокислоти: одержання, властивості, роль у біології
Розроблено багато шляхів отримання - амінокислот. Найважливіші з них три: 1. Дія аміаку на солі хлорзамісних кислот:...
-
ЙОД Сировиною для промислового одержання йоду служать нафтові бурові води, морські водорості, а також маткові розчини чилійської (натрієвої) селітри, що...
-
Готуємо розчин НСІ з С = 0,1 моль/дм3 об'ємом 1 дм3 з фіксаналу, у відповідності з правилами, наведеними вище. Стандартизація приготовленого розчину...
-
ЙОД ЙОД - І хімічний елемент VII групи періодичної системи Менделєєва, належить до галогенів (у літературі зустрічається також символ J); атомний номер...
-
Висновок - Типові неметали - галогени, їх характеристика, властивості і сполуки
Всі галогени дуже отруйні. Вдихання їхньої пари викликає подразнення органів дихання, а у великих кількостях вони викликають задуху. Особливо отруйним є...
-
КАУЧУК І ГУМА, ДЖЕРЕЛА НАТУРАЛЬНОГО КАУЧУКУ, ВЛАСТИВОСТІ КАУЧУКУ - Каучук і гума
Каучук - речовина, що одержується з каучуконосних рослин, що ростуть у тропіках і утримуючих молочну рідину (латекс) у коренях, стовбурі, гілках, чи...
-
Отримання титану - Титан та його властивості
Ціна - от що ще гальмує виробництво і споживання, титану. Власне, висока вартість - не уроджений порок титану. У земній корі його багато - 0,63%....
-
Температурні, електричні і магнітні властивості титану - Титан та його властивості
Титан має порівняно низьку теплопровідність, всього 22,07 Ут/(мк), що приблизно в 3 рази нижче теплопровідності заліза, у 7 разу-магнію, у 17-20...
-
Фізичні і механічні властивості титану - Титан та його властивості
Титан дуже тугоплавкий метал. Довгий час вважався, що він плавиться при 1800° С, однак у середині 50-х рр. англійські вчені Діардорф і Хейс установили...
-
Фізичні та хімічні властивості - Натрій: історія, властивості
Фізичні властивості. Оскільки в атомах лужних металів один зовнішній електрон доводиться на 4 і більше вільні орбіталі, а енергія іонізації атомів...
-
Горіння простих і складних речовин: А) С + О2 СО2 2Сu + O2 = 2CuO (окислення, крім благородних металів) Б) СН4 + 2О2 СО2 + 2Н2О 2. Розклад під час...
-
Фізичні властивості. - Виробництво і застосування платини
Платина дуже тугоплавкий метал, кристалізується в гранецентровані кубічні (р. ц. до.) грати. При дії на розчини солей відновниками метал може бути...
-
ВИРОБНИЦТВО СУЛЬФАТНОЇ КИСЛОТИ - Загальні відомості про елементи
Найбільш сучасний спосіб добування сульфатної кислоти у промисловості - це кнтактний. Як сировина використовується пірит FeS2 (залізий, сірчаний,...
-
Вступ - Типові неметали - галогени, їх характеристика, властивості і сполуки
До головної підгрупи VII групи періодичної системи елементів Д. І. Менделєєва входять: Фтор F, Хлор Cl, Бром Br, Йод J та Астат At. Загальна назва цієї...
-
ВУГЛЕКИСЛИЙ ГАЗ ТА ЙОГО ВЛАСТИВОСТІ - Склад повітря
Вивчаючи "Склад повітря" ми проводили дослід, зображений на малюнку 41. Через те, що вапняна вада помутніла ми зробили висновок, що у повітрі є...
-
Властивості природного газу - Зріджений природний газ: його характеристика
У природному стані газ представлений у вигляді окремих скупчень. Їх прийнято називати газовими покладами, які накопичуються в земних надрах, як газові...
-
Визначення : Скалярний добуток двох векторів і дорівнює добутку модулів цих векторів на косинус кута між ними . (6.1) Таким чином, скалярний добуток двох...
-
Властивості титану - Титан та його властивості
У періодичній системі елементів Менделєєва титан має порядковий номер 22. Атомна маса природного титану, обчислена за результатами досліджень його...
-
З історії відкриття титану - Титан та його властивості
Навряд чи можна знайти ще один такий метал, історія відкриття і вивчення якого були б так повны драматичних подій, помилок і оман, як історія титану....
-
Цей параграф носить допоміжний характер. Тут встановлюється декілька простих властивостей модуля нерперывности вищих порядків. Всі функції F1 , що...
-
Загальні властивості функцій - Функції та способи їх задання
Означення : Множина всіх значень аргумента, для яких можна обчислити значення функції, називається природною областю визначення функції. Область...
-
Їдкі луги - Натрій: історія, властивості
Їдкими лугами називаються добре розчинні у воді гідроксиди. Найважливіші з них NaOH і KOH. Гідроксид натрію - білий, непрозорий, тверда кристалічна...
-
КИСЕНЬ ТА ЙОГО ВЛАСТИВОСТІ - Склад повітря
Кисень -- найпоширеніший хімічний елемент на Землі. У вільному стані кисень є у повітрі і в природних водах. У зв'язаному стані кисень входить до складу...
-
Натрій в природі, Отримання, застосування натрію - Натрій: історія, властивості
У природі лужні елементи трапляються лише у вигляді солей. Найважливішими мінералами Натрію є кам'яна сіль або галіт NaCl, чилійська селітра NaNO3,...
-
Виробництво сульфатної кислоти - Неметали та їхні сполуки
Найбільш сучасний спосіб добування сульфатної кислоти у промисловості - це кнтактний. Як сировина використовується пірит FeS2 (залізий, сірчаний,...
-
Нехай функція F (х) задана на відрізку [a, b] . Розіб'ємо цей відрізок на N частин точками ділення А = х0 < x1 < x2 < ... < хn = b У кожному...
-
ХІМІЧНІ ВЛАСТИВОСТІ КИСНЮ І СІРКИ - Неметали та їхні сполуки
Ви вже знаєте, що кисень - дуже реакційноздатна речовина. Він реагує з багатьма металами, неметалами багатьма складними речовинами, виявляючи властивості...
-
Історія натрію - Натрій: історія, властивості
Назва "натрій" походить від стародавнього слова, яке порівняно широко поширене в Єгипті, а так само у древніх греків і римлян. Це слово можна було...
-
Альдегіди Ми знаємо, що спирти легко окиснюються. При їх повному окисненні (горінні) утворюються оксид вуглецю (IV) і вода. Під впливом різних окисників...
-
ХІМІЧНІ ВЛАСТИВОСТІ КИСНЮ І СІРКИ - Загальні відомості про елементи
Ви вже знаєте, що кисень -- дуже реакційноздатна речовина. Він реагує з багатьма металами, неметалами багатьма складними речовинами, виявляючи...
-
Визначення : Алгебраїчні лінійні рівняння називаються однорідними, якщо в них вільний член дорівнює нулю. Розглянемо таку систему, що має вигляд: (10.1)...
-
Система диференціальних рівнянь, що записана у вигляді Чи у векторно-матричному вигляді Називається системою лінійних неоднорідних диференціальних...
-
Властивості розчинників електролітів - властивості іонів. - Дисоціація
Хлор отруйний, а в міру посолена їжа, крім користі, нашому організму не приносить. Але проста речовина Na складається з атомів натрію, а проста речовина...
-
Задачі, що привели до поняття визначеного інтеграла Розглянемо дві задачі -- геометричну та фізичну. 1. Обчислення площі криволінійної трапеції . Нехай...
-
Визначники та їх властивості - Основи вищої математики
До поняття визначника приходимо, розглядаючи системи алгебраїчних рівнянь першого степеня. Розглянемо систему рівнянь: (2.1) X та y -- невідомі,...
-
З математичної точки зору розв'язки (1) і (2) мають однаковий зміст. О-1 Подвійним інтегралом від функції по області називається границя (3) За умови, що...
Властивості нітратної і фосфатної кислоти