Производство формальдегида на серебряном катализаторе - Разработка технологической схемы парофазного окисления этиленгликоля в глиоксаль с использованием серебряных катализаторов
Основной производственный метод получения формальдегида во всем мире уже много лет - каталитическое взаимодействие метанола с кислородом воздуха.
В 20-х годах многими исследователями было показано, что серебро и его сплавы более эффективны в качестве катализаторов, чем медь.
Как известно, смеси метанола с кислородом или воздухом взрывоопасны. При атмосферном давлении область распространения пламени в смесях метанол - воздух находится в диапазоне объемного содержания метанола от 6,7 до 36,4 %. При добавлении инертного газа (азот) пределы взрывных концентраций сужаются, также аналогичный эффект оказывает добавление паров воды (рисунок 1.1). С повышением температуры указанные пределы несколько расширяются.
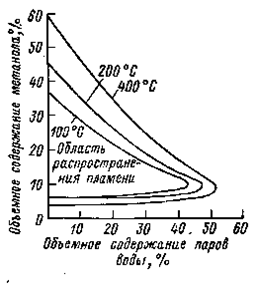
Рисунок 1.1 - Влияние воды на размеры области распространения пламени в смесях метанола с воздухом
Окислительная конверсия метанола на серебре (рисунок 1.2) проводится при соотношении метанол : воздух выше верхнего предела взрывной концентрации, то есть при большом избытке метанола по отношению к кислороду.
Образование формальдегида осуществляется в результате протекания параллельных реакций простого и окислительного дегидрирования метанола (тепловые эффекты найдены на основе данных [17, стр. 33], ?Q298 = - ?Н298):
СН3ОН + 0,5О2 > СН2О + Н2О + 147,4 кДж/моль, (1.4.1)
СН3ОН > СН2О + Н2 - 93,4 кДж/моль. (1.4.2)
Наряду с этими реакциями в системе протекает ряд побочных превращений:
СН3ОН+3/2О2 > СО2 + 2Н2О + 575,1 кДж/моль, (1.4.3)
СН2О + 0,5О2 > НСООН + 270,4 кДж/мол, (1.4.4)
НСООН + 0,5О2 > СО2 + Н2О + 14,5 кДж/моль, (1.4.5)
СН2О>СО+Н2+1,9 кДж/моль. (1.4.6)

1 - испаритель; 2 ,7- теплообменник; 3 - реактор; 4 - катализатор; 5 - подконтактный холодильник; 6 - абсорбер; 8 - сборник формалина; а - воздух, б - метанол, в - вода, г - метанольный формалин.
Рисунок 1.2 - Технологическая схема производства формальдегида на серебряном катализаторе
Технологическая схема рассматриваемого процесса приведена на рисунке 1.2. Она состоит из следующих узлов: Испарителя 1; четырех теплообменников 2 и 7; реактора 3, в который входят катализатор 4 и подконтактный холодильник 5; абсорбера 6; сборника формалина 8.
На схеме производства формальдегида на катализаторе серебро на носителе метанол, содержащий 20 - 25 % воды, поступает в испаритель 1, где испаряется в токе воздуха. Паровоздушная смесь перегревается до 110 °С в теплообменнике 2 и подается в верхнюю часть реактора 3. При пуске системы слой катализатора 4 в реакторе разогревается до 250 - 300 °С с помощью специального электроподогревателя, а после "зажигания" слоя температура катализатора поддерживается на заданном уровне за счет тепла реакции. Пройдя с высокой скоростью через слой катализатора, реакционная смесь охлаждается в подконтактном холодильнике 5. Далее газообразные продукты реакции поступают в абсорбер 6, где из них извлекаются формальдегид и не прореагировавший метанол. Абсорбер, представляющий собой тарельчатую колонну, разделен на три секции. Нижняя секция орошается формалином, средняя - раствором, содержащий 15 - 20 % формальдегида, а верхняя - чистой водой. Из низа абсорбера выходит товарный формалин.
Превращение метанола в формальдегид происходит в результате контакта молекул спирта с кислородом, хемосорбированных на атомах серебра, то есть активными центрами катализатора являются поверхностные окислы серебра.
В условиях технического процесса значение ?Q составляет 90 - 100 кДж. Исходная смесь, попадая в реактор, нагревается более, чем на 500 оС, процесс осуществляется без отвода тепла - адиабатический режим. С учетом большого разбавления азотом, система в целом малочувствительна к изменению давления. Изменение общего давления от 0,01 до 1 МПа практически не влияет на состав продуктов.
При температуре около 300 оС происходит "зажигание" катализатора, то есть переход от изотермического к адиабатическому режиму. Этот момент характеризуется быстрым и самопроизвольным повышением температуры "горячей точки" катализатора до 600 - 700 оС, соответствующей заданному мольному отношению кислород : метанол.
Разбавление спиртовоздушной смеси инертными газами - один из способов повышения общей конверсии метанола [18]. Оптимальным разбавлением является отношение инерт : метанол = 1,5 : 1 ч 2 : 1. В этих пределах разбавления лежат рекомендации патентов [20]. В качестве разбавителя рекомендуется применять абгазы, азот, аргон, гелий [18, 19], диоксид углерода [20].
В таблице 1.8 приведены показатели процесса получения формальдегида с рециркуляцией отходящего газа по данным фирмы BASF [17, стр. 44].
Добавление к исходному метанолу воды, помимо уменьшения взрывоопасности процесса, благоприятно сказывается на таких показателях, как селективность, стабильность работы катализатора.
Таблица 1.8 - Показатели процесса получения формальдегида
|
Мольная селективность образования формальдегида, % |
89,3 |
|
Конверсия метанола, % |
97- 98 |
|
Температура в реакторе, оС |
680 - 720 |
|
Выход абгазов (на 1т формалина), м3 |
1984 |
|
Массовое содержания формальдегида в формалине, % |
50 - 55 |
|
Содержание (на 100 % формальдегида) Метанола, % Муравьиной кислоты, ‰ |
|
|
Содержание воды в продуктах реакции (в расчете на 1т формалина), м3 |
0,54 |
Похожие статьи
-
Первое пробное исследование по получению формальдегида из метанола в присутствии смеси оксидов железа и молибдена проведено в начале 30-х годов [17, стр....
-
Основной производственный метод получения формальдегида во всем мире уже много лет - каталитическое взаимодействие метанола с кислородом воздуха. В 20-х...
-
Моделирование ХТС производства формальдегида на пакете HYSYS Процесс парофазного окисления этиленгликоля в глиоксаль на серебряных катализаторах является...
-
В промышленности синтез глиоксаля окислением этиленгликоля протекает в адиабатических условиях, оптимальный температурный режим процесса зависит от...
-
В России процесс окисления этиленгликоля с получением глиоксаля в промышленных масштабах не реализован, что обусловлено отсутствием соответствующих...
-
Запатентован способ получения глиоксаля окислением этиленгликоля в жидкой фазе при обработке кислородом или кислородсодержащим газом. Окисление проводят...
-
Анализ моделирования ХТС Высокая реакционная способность этиленгликоля и, особенно, продуктов его превращения, многообразие влияющих на процесс внешних...
-
В промышленности синтез глиоксаля окислением этиленгликоля протекает в адиабатических условиях, оптимальный температурный режим процесса зависит от...
-
Элементы технологических схем производства формальдегида на оксидном катализаторе (рисунок 1.3 и 2.2) не совпадают, поскольку программная система Hysys...
-
Метод жидкофазного окисления ацетальдегида азотной кислотой является одним из промышленных способов получения глиоксаля. Суммарное уравнение реакции...
-
Общие сведения о глиоксале Глиоксаль (этандиал, диформиль, щавелевый альдегид) -- простейший диальдегид. Несмотря на простое строение и химический состав...
-
Запатентован способ получения глиоксаля окислением этиленгликоля в жидкой фазе при обработке кислородом или кислородсодержащим газом. Окисление проводят...
-
Смоделированная технологическая схема производства глиоксаля парофазным окислением этиленгликоля (рисунок 2.4) предназначена для создания установки на...
-
Существуют разработки метода синтеза глиоксаля озонированием бензола эквивалентным количеством озона с дальнейшим гидрированием получаемых продуктов для...
-
Синтез альдегидов и кетонов парофазным каталитическим окислением спиртов осуществляется во всех промышленно-развитых странах. Таким путем получают...
-
Глиоксаль формальдегид катализатор окисление В процессе выполнения дипломного проекта проведен анализ способов получения глиоксаля, а также...
-
Термодинамика процесса В процессах парофазного каталитического окисления моноатомных спиртов и этиленгликоля возможна реализация следующих превращений...
-
Таблица 2 - Структура сырья в производстве метанола, %. Сырье В мире Беларусь и Россия Природный газ 73,8 70,7 Нефть и нефтепродукты 24,4 4,0 Отходы...
-
Другим способом получения формальдегида является окислительное дегидрирование метилового спирта в присутствии катализаторов. Последние можно разделить на...
-
Возникновение горения чаще всего связано с нагреванием горючей системы тем или иным источником воспламенения. При этом энергия молекул горючего и...
-
Каталитическое окисление органических соединений является ведущим методом получения ценных продуктов химической и нефтехимической промышленности. Этим...
-
В России процесс окисления этиленгликоля с получением глиоксаля в промышленных масштабах не реализован, что обусловлено отсутствием соответствующих...
-
При использовании разомкнутых химико-технологических систем в большинстве случаев принципиально невозможно проведение процессов при практически полной...
-
Метиловый спирт [30] - Разработка технологической схемы получения анизола и крезола
Молекулярная формула CH3OH Молярная масса 32,04 г/моль Внешний вид бесцветная жидкость Свойства Плотность и агрегатное состояние 791,8 кг/м?,...
-
Качественные методы анализа - Разработка технологической схемы получения анизола и крезола
Рециркуляционных реакционно-ректификационных процессов. При анализе сложных ХТС, характеризующихся большим числом параметров и переменных необходимо...
-
В настоящее время производственные методы получения формальдегида большим разнообразием не отличаются. Так, в реакциях восстановления СО и СО2 Водой...
-
Этот способ концентрирования обеспечивает получение чистой концентрированной азотной кислоты без вредных выбросов в атмосферу. Однако у него есть ряд...
-
Свойства, получение и применение компонентов разделяемой смеси Анизол C7H8O / С6Н5ОСН3 Молекулярная масса: 108.1 Температура кипения: 155°C Температура...
-
Один из способов повысить селективность - это правильно подобрать катализатор. Рассмотрим этот метод, на примере получения анизола и крезола. Анизол и...
-
Термодинамика процесса В процессах парофазного каталитического окисления моноатомных спиртов и этиленгликоля возможна реализация следующих превращений...
-
Производство полимеров - Анализ и технологическая оценка химического производства
Высокомолекулярные соединения получают из мономеров полимеризацией, сополимеризацией, поликонденсацией и методами привитой полимеризации и...
-
Получение синтезированного газа - Анализ и технологическая оценка химического производства
Химические методы переработки нефти проводят при высоких температурах без катализатора (термический крекинг), при высоких температурах в присутствии...
-
Полимеризация двуокиси азота. Переработка нитрозных газов в азотную кислоту обычно происходит при температурах от О до 50 °С. В этих условиях двуокись...
-
Метод жидкофазного окисления ацетальдегида азотной кислотой является одним из промышленных способов получения глиоксаля. Суммарное уравнение реакции...
-
Можно выделить и сопоставить преимущества и недостатки обоих методов (таблица 1.10) [17, стр. 65 - 66] . Применение технологии с оксидным катализатором...
-
Условия, при которых протекает процесс получения глиоксаля на серебряном катализаторе, сведены в таблице 2.2. Таблица 2.2 содержит следующие данные: -...
-
Выводы - Анализ способов получения глиоксаля и технологических схем окисления одноатомных спиртов
В ходе изучения процессов окисления спиртов были смоделированы в программной системе Hysys две технологические схемы производства формальдегида: - на...
-
Общие сведения о глиоксале Глиоксаль (этандиал, диформиль, щавелевый альдегид) -- простейший диальдегид. Несмотря на простое строение и химический состав...
-
О-КРЕЗОЛ - Разработка технологической схемы получения анизола и крезола
C7H8O/CH3C6H4OH Молекулярная масса: 108.2 Температура кипения: 191°C Температура плавления: 31°C Относительная плотность (вода = 1): 1.05 Растворимость в...
-
Введение - Разработка технологической схемы получения анизола и крезола
Известно в некоторых случаях невозможно достичь высокой селективности химико-технологических процессов. Это происходит вследствие наличия побочных...
Производство формальдегида на серебряном катализаторе - Разработка технологической схемы парофазного окисления этиленгликоля в глиоксаль с использованием серебряных катализаторов