Экспериментальная часть - Определение теплоты и энтропии адсорбции или растворения на основе хроматографических данных
Определение теплоты и энтропии адсорбции или растворения на основе хроматографических измерений
Коэффициент адсорбции Г и коэффициент распределения К - термодинамические константы фазового равновесия. Поэтому для них справедливы уравнения:
(1)
(1, а)
(2)
(2, а)
В этих условиях Ga и Gs - свободные энергии адсорбции и растворения, соответственно, т. е. свободные энергии перехода вещества из одной фазы (подвижной) в другую фазу (неподвижную) и наоборот; R и Т - газовая постоянная и абсолютная температура хроматографической колонки, при которой измерены Г или К; На и Нs - энтальпии адсорбции и растворения, соответственно, численно равные теплотам адсорбции и растворения, но с обратным знаком, т. е. - Qа и - Qs; Sa и Ss - энтропии адсорбции и растворения, соответственно. Приравняем правые части уравнения (1) и (2), а также (1, а) и (2, а). После простых преобразований:
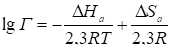
, (3)
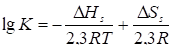
. (3, а)
При этом - На = Qa и - Нs=Qs.
Так как Н и S мало зависят от температуры, то уравнения (3) и (3, а) можно рассматривать как уравнения прямой
У = Ах + В
со следующими параметрами:
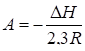
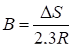
(или lgK), , ; (4)
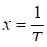
Очевидно, если нанести на график величины lgГ или lgK относительно обратных температур 1/Т хроматографической колонки, при которых измерялись Г и К, то экспериментальные точки должны лечь на прямую. Из углового его коэффициента прямой можно вычислить теплоту адсорбции Qa или теплоту растворения Qs, а по отрезку В и его численному значению - соответствующую энтропию адсорбции или энтропии растворения, т. е. Sa или Ss.
Угловой коэффициент прямой, построенной в координатах lgГ или lgK относительно 1/Т, очевидно, равен:
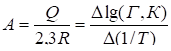
. (5)
Следовательно,
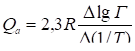
(для ГАХ) (6)
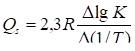
(для ГЖХ) (6, а)
Величины lgГ и lgK представляют собой соответственно разности логарифмов коэффициентов адсорбции и коэффициентов распределения, измеренных при двух температурах хроматографической колонки: Т1 и Т2. Величина (1/Т) есть разность обратных температур Т1 и Т2.
Таким образом, теплота адсорбции и теплота растворения определяется довольно просто из ряда хроматографических опытов, проведенных при различных температурах колонки в изотермическом режиме.
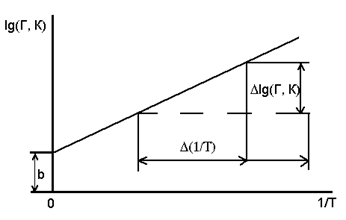
Рис. 33 Определение теплот адсорбции из хроматографических данных
Удельный удерживаемый объем связан с константой адсорбционного равновесия следующим образом:
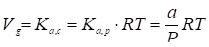
, (7),
Где Vg - удельный удерживаемый объем, приведенный к температуре колонки; а - величина адсорбции в молях на г вещества, Р - равновесное давление вещества в газовой фазе.
Пользуясь уравнением Клаузиуса-Клайперона, можно вычислить изотермическую теплоту адсорбции (при а=соnst):
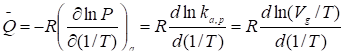
. (8)
Интегрируя (2) при допущении независимости Qa от Т, получаем:
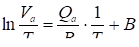
(9)
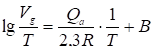
(9, а)
Где В - константа интегрирования.
Для измерения теплоты адсорбции нужно измерить удерживаемые объемы при нескольких температурах и построить график значений lg(Vg/T) от функции 1/Т. Из тангенса угла наклона полученной прямой по формуле (3, а) вычисляют величину теплоты адсорбции.
Если при всех температурах объемная скорость газа-носителя сохраняется постоянной, можно для расчетов вместо lg(Vg/T) брать lgtR.
Следует отметить, что деление Vg на Т производится для того, чтобы избавиться от переменной Т, вводимой в Vg приведением объемной скорости к температуре колонки. Если теплоту адсорбции вычислить из графика зависимости lgVg от 1/Т, то полученная величина будет меньше истинной на величину RT, где Т - средняя температура интервала.
Следовательно, для расчетов нужно брать либо Vg/T, либо удерживаемый объем, приведенный к постоянной температуре (обычно 273 К):
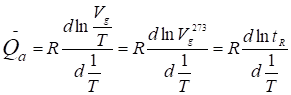
. (10)
При линейной изотерме адсорбции пики симметричны и удерживаемы объем не зависит от величины пробы, т. е. теплота адсорбции не зависит от величины а и от степени заполнения поверхности
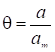
.
В этом случае расчет производится по удерживаемым объемам, соответствующим максимам пиков. При нелинейной изотерме и несимметричных пиков расчет по (7) осложнен тем, что даже при одинаковых вводимых пробах величины заполнений при разных температурах могут быть разными, т. е. нарушится основное условие а = const.
Для точных расчетов при нессиметричных пиках рекомендуется вычислять из пиков изотермы адсорбции в координатоах из зависимости lgP от 1/Т.
Для расчета теплоты адсорбции какого-либо вещества по удерживаемым объемам или временам удерживания нужно произвести следующие измерения.
При нескольких температурах (не мене трех, через интервалы 10-200С) в колонку вводятся одинаковые количества исследуемого вещества и измеряются времена выхода максимумов пиков. Для каждой температуры определяется также время выхода газа-носителя, для этого в колонку вводится проба несорбирующегося газа (если в качестве газа-носителя используется азот, можно вводить гелий, водород или воздух).
Пример расчета теплоты адсорбции пара гексана на силикагеле дан в таблице 2 и на рис. 13.
Таблица 2
|
Вещество |
Т, К |
1/Т103 |
Время удерживания вещества t, с |
Время удерживания газа-носителя, t0, с |
TR=t-t0 |
LgtR |
, кал/моль |
|
373 |
2,68 |
135 |
28 |
107 |
2,029 |
810 | |
|
398 |
2,51 |
78 |
26 |
52 |
1,716 | ||
|
423 |
2,36 |
54 |
25 |
29 |
1,426 |
На оси абсцисс откладываются значения 1/Т по оси ординат соответствующие им значения lg tR.
Через точки проводится прямая, из тангенса угла наклона которой к оси абсцисс вычисляется теплота адсорбции:
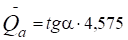
(11)
Для гомологических рядов веществ наблюдается линейная зависимость как lgtR, так и Qa от числа углеродных атомов в молекуле адсорбента.
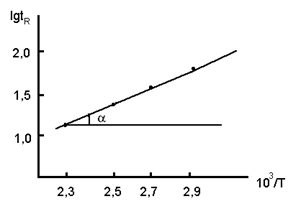
Рис. 34 Зависимость lgtR от 1/Т для н-гексана на силикагеле.
Порядок работы на хроматографе ЛХМ - 72
- 1. Подать газ-носитель гелий (Не), 4-5 атм. (на контроле 10 и 10 в обеих колонках). 2. Регуляторы "колонки I, II" не трогать! 3. Включите тумблер Сеть на блоке анализатора. В верхней части передней панели блока анализатора должна загореться сигнальная лампочка и включиться вентилятор циркуляции воздуха, работа которого определяется характерным шумом.
Если крыльчатка вентилятора не вращается по каким-либо причинам, включите тумблер Сеть во избежание перегорания обогревателя.
Внимание! Работа прибора с неработающим вентилятором недопустима.
4. Включите тумблер Сеть на регистраторе КСП-4 блока управления, а также тумблер Диаграмма регистратора.
Предварительно на регистраторе должна быть установлена скорость протяжки диаграммной ленты в соответствии с указаниями инструкции на регистраторе.
- 5. Включите тумблер Сеть на блоке программирования. 6. Вывернув ручку Ток детектора блок управления до отказа против часовой стрелки, включите тумблер Сеть и Ток детектора, а затем установите необходимый ток детектора, учитывая род газа-носителя и температуру в термостате колонок согласно таблице 3.
Таблица 3 Ток детектора, мА
|
Температура термостата детектора, С |
Газ - носитель | ||
|
Гелий |
Азот |
Аргон | |
|
20 |
150 - 160 |
100 - 110 |
70 - 80 |
|
100 |
120 - 130 |
85 - 95 |
60 - 65 |
|
200 |
110 - 115 |
70 - 80 |
50 - 55 |
|
300 |
70 - 95 |
45 - 50 |
35 - 45 |
Включать тумблер Ток детектора без подачи газа-носителя в детектор нельзя во избежание выхода из строя детектора
Ручку переключателя Множитель установите в положение 100. Ручками Установка нуля, Плавно и Грубо выведите перо регистратора на середину шкалы.
- 7. Установить "ток детектора" 60А. 8. Установите требуемую температуру испарителей с помощью переключателя В1 за детекторной крышкой на блоке анализатора. 9. Температура испарителя должна быть на 500С выше температуры в термостате колонок. При установке температуры испарителей более 2000С подключите воздушное или водяное охлаждение мембраны испарителя (через резиновые шланги к крану с водой). (Испаритель ВКЛ-I - установлен на постоянную температуру (не меняется). 10. После 3-5 минут прогрева включить тумблеры: "термостат колонок" - 80, 100 и 120 (С) и "термостат детектора" - 160С (не более 200С, иначе испарится свинцовая пайка катарометра). 11. До тех пор, пока температура детектора по теплопроводности не стабилизируется, возможен большой дрейф нулевой линии регистратора. В это период разогрева (около 1,5 часа) масштаб регистрации следует оставлять равным 100. 12. По мере разогрева прибора переключатель Множитель постепенно переводится в положение минимального значения, а потенциометрами Установка нуля перо регистратора постепенно выводится на нулевую отметку. Прибор можно считать вышедшим на режим, если дрейф и флуктуации нулевой линии на самом чувствительном масштабе не будут соответственно превышать 2% в час и 0,5% от значения шкалы. После выхода прибора на режим можно приступать к проведению анализа.
Для анализа жидкой пробы шприцем (рис. 14), промытым несколько раз анализируемой смесью, вбирается необходимое количество этой смеси, а затем игла шприца через уплотнительную резину испарителя вводится в испаритель на максимально возможную глубину по центру отверстия ввода испарителя, и проба выдавливается.
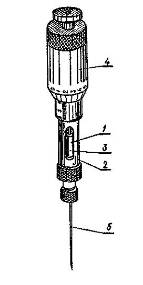
Рис. 35 Микрошприц. 1 - капилляр, 2 - корпус, 3 - поршень, 4 - микрметрический винт, 5 - игла
Следует помнить, что после 10-15 проколов резиновое уплотнение испарителя может потерять герметичность, что приведет к потерям анализируемого вещества и соответствующему уменьшению пиков на хроматограмме, а также к увеличению дрейфа нулевой линии прибора. Поэтому следует менять уплотнение испарителя, сняв гайку испарителя на внешней панели корпуса хроматографа.
13. Аналогично вводу жидкой пробы вводится с помощью шприца и газовая.
В случае, если при подаче анализируемой смеси в прибор происходит движение пера регистратора в левую сторону - отрицательные пики, то необходимо изменить положение тумблера, маркированного "+" и "-" на блоке управления.
Задание к работе
- 1. При работающей диаграмме (60 мм/час) ввести 5 (или 10) мкл пентана (либо гексана). 2. Подсчитать время выхода вещества (число клеток на диаграмме). 3. Опыт проводить еще не менее трех раза - до воспроизводимости результатов. 4. Записать: tколонок (80 С); tдетектора (160С). 5. Другим шприцом (объем V = 1-5 мл) при закрытых отверстиях выхода гелия (вверху слева на приборе) ввести 1 см3 воздуха - для определения емкости колонок. 6. Установить tколонок на 20С больше, т. е. 100С; значение tдетектора не изменяется (160С). Ввести 5-10 мкл пентана (гексана). 7. Опят повторить еще 3 раза, вычислить время выхода.
Отключение прибора
1. Все выключатели перевести в положение "ВЫКЛ", кроме вентилятора; когда температура детектора понизится, закрыть подачу газа из баллона (Не).
Похожие статьи
-
Газовый хроматография энтропия адсорбция Области физико-химических применений газовой хроматографии Газовая хроматография, имеющая главным образом...
-
На рис. 8 изображена схема газового хроматографа ХЛ-4. Выходящий из баллона газ-носитель проходит через осушитель 3, дроссель 4, ротаметр 5 и попадает в...
-
С помощью регистрирующих приборов - самописцев, которые измеряют и автоматически записывают последовательность сигналов детектора, получают кривую...
-
Адсорбенты Применяемые адсорбенты характеризуются адсорбционной активностью, истинной и насыпной плотностью, удельной поверхностью общим объемом пор и их...
-
Теплотой нейтрализации называется количество теплоты, выделенное при взаимодействии 1 моля эквивалента какой-либо кислоты с 1 молем эквивалента...
-
Теплота нейтролизация растворение соль Интегральной теплотой растворения называют теплоту, выделенную или поглощенную при растворении 1 моля вещества в...
-
Программное обеспечение, Первичная обработка экспериментальных данных - Основы качественного анализа
На компьютерах кафедры общей и неорганической химии все необходимое установлено, а если Вы предполагаете выполнять работу на своем компьютере, то...
-
Определение необходимого объема выборки - Основы эконометрики
В практике проектирования выборочного наблюдения возникает вопрос о необходимой численности выборки, которая необходима для обеспечения определенной...
-
ПОНЯТИЕ ОБ АВТОКОРРЕЛЯЦИИ. ОПРЕДЕЛЕНИЕ СИЛЫ АВТОКОРРЕЛЯЦИИ Парные регрессионные модели отражают специфику взаимодействия некоторого функционального...
-
Время удерживания (абсолютное) - это отрезок времени, который проходит с момента ввода вещества в колонку до появления максимума пика вещества на...
-
В термодинамике понятие "энтропия" было введено Р. Клаузиусом (1865), который показал, что процесс превращения теплоты в работу следует общей физической...
-
Исходные данные - Расчет трансформаторов теплоты
Потребность предприятия в захоложенной воде с учетом ее потерь составляет V = 80 м 3/ч. Вода выходит из технологических аппаратов с температурой T1 = 30...
-
Q1-2=CP - (T2-T1)= 1046 - (475,4 - 300)= 183468,4 Дж/кг. Q2-3= ДU = 47359,8 Дж/кг. Q3-4= CP - (T3-T4)= 1046 - (538,8 - 336,6)=211501,2 Дж/кг. Q4-1= Дh...
-
Разработка алгоритма нахождения входного потока заявок в имитационной модели контрольно-пропускной системы на основе статистических данных В наши дни...
-
Пусть необходимо подобрать оптимальные настройки для объекта с передаточной функцией (9). Степень затухания, к примеру, ш= 0.75. Ниже даются рекомендации...
-
Энтропия. Движущее начало химических процессов - Химическая термодинамика. Термохимия. Решение задач
Убедившись в полезности знания тепловых эффектов химических превращений, мы, тем не менее, не смогли ответить на вопрос: "Почему одни химические реакции...
-
Синтез бромэтана проводили в соответствии с методикой, изложенной в источнике [2]. ХОД РАБОТЫ - Приготовление исходных реактивов и собирание прибора Рис....
-
Тепловые эффекты при растворении. Механизмы растворения веществ в воде - Растворы
Растворение веществ сопровождается различными тепловыми эффектами в зависимости от природы вещества. При растворении в воде, например, гидроксида калия...
-
Методы изучения связи качественных признаков - Основы эконометрики
При наличии соотношения между вариацией качественных признаков говорят об их ассоциации, взаимосвязанности. Для оценки связи в этом случае используют ряд...
-
Генеральная совокупность и выборка - Основы научных исследований
Распределение случайной величины содержит всю информацию о ее статистических свойствах. Много ли нужно знать значений случайной величины, чтобы построить...
-
Методика: расворяют 50 мг анализируемого вещества в гексане R, затем разбавляют до 50,0 мл тем же растворителем. Эталонный раствор (А): растворяют 50 мг...
-
Адсорбционные методы исследования свойств поверхности позволяют количественно охарактеризовать происходящие при адсорбции межмолекулярные взаимодействия,...
-
Определение. Примеры - Формационные основы универсальных алгебр
1. Пусть А - непустое множество (АШ), n -- натуральное число, - декартова (прямая) n-ая степень множества А. В частности, если n=0, то под будем понимать...
-
В инвестиционной практике постоянно приходится считаться с корректирующим фактором инфляции, которая с течением времени обесценивает стоимость денежных...
-
Плоскость геометрический точка проецирование Длину отрезка АВ можно определить из прямоугольного треугольника АВС-- AС = A1B1...
-
Статистический характер экспериментальных исследований Любое экспериментальное исследование, в конечном итоге, сводится к изучению причинно-следственных...
-
В основе метода площадей лежит предположение, что объект может быть описан линейным дифференциальным уравнением с постоянными коэффициентами, а его...
-
Экспериментальная часть - Синтез пара-нитродифенила. Теоретические основы нитрования
A. Реагенты и оборудование Для проведения синтеза использовались следующие реагенты: Дифенил C12H10 Молекулярная масса: 154.2 Температура кипения: 256°C...
-
Скорость реакции определяется изменением молярной концентрации одного из реагирующих веществ: V=dC/dtV. Факторы, влияющие на скорость химических...
-
Воздушная известь - одно из древнейших вяжущих, широко применяемых в строительстве и промышленности. Известь - продукт умеренного обжига кальциевых и...
-
Общая схема исследования: 1. Составление среднего образца. 2. Извлечение пестицидов из пробы. 3. Очистка экстракта. 4. Анализ экстракта. Прием образцов в...
-
Гигиеническая классификация пестицидов - Метод определения хлорсодержащих пестицидов
По токсичности при поступлении в желудок А) сильнодействующие ядовитые вещества ( СДЯВ ) - ЛД до 50мг/кг Б) высокотоксичные - ЛД 50-200мг/кг В)...
-
Определение температуры плавления Температуру плавления определяем с помощью малогабаритного нагревательного стола типа "Boetinus" с наблюдательным...
-
Методы непараметрической статистики - Основы теории систем и системного анализа
Использование классических распределений случайных величин обычно называют "параметрической статистикой" - мы делаем предположение о том, что...
-
Элементы теории процентов - Финансово-математические основы инвестиционного проектирования
В процессе анализа инвестиционных решений принято использовать сложные проценты. Сложным процентом называется сумма дохода, которая образуется в...
-
Окисление фосфора - Основы теории окислительной плавки
Как уже отмечалось, фосфор вредная примесь. Наличие его в стали понижает ее пластические свойства, свариваемость, повышает анизотропию механических...
-
Адсорбция Лэгмюра и Фрейндлиха
Адсорбция. Изотермы адсорбции Лэгмюра, Фрейндлиха. Уравнение БЭТ и его анализ Поверхностная энергия стремится самопроизвольно уменьшиться. Это выражается...
-
Что такое гравиметрический фактор F - Основы аналитической химии
Если мы знаем A - навеску анализируемой пробы, b - массу осадка и его состав, то мы можем вычислить содержание определяемого вещества X . X = a*F*100/b...
-
Целью курсовой работы является эффективная организация работы отдела планирования и экономического анализа Могилевского филиала РУП "Белтелеком"....
-
Смещение химического равновесия. Принцип Ле-Шателье - Основы химии
Положение химического равновесия зависит от следующих параметров реакции: температуры, давления и концентрации. Влияние, которое оказывают эти факторы на...
Экспериментальная часть - Определение теплоты и энтропии адсорбции или растворения на основе хроматографических данных