Заторможенное внутреннее вращение - Внутреннее вращение молекул
Еще А. М. Бутлеров указывал на существование в молекуле взаимного влияния атомов, непосредственно несвязанных друг с другом химическими связями, а изучением этого влияния много занимался В. В. Марковников. Очевидно, что открытое физико-химическими методами торможение внутреннего вращения молекул относительно одинарных связей обусловлено взаимодействием непосредственно химически не связанных между собой атомов. Раз такое взаимодействие существует, то его энергия должна как-то зависеть от расстояния между взаимодействующими несвязанными атомами. Можно предполагать, что экстремумы функции этой зависимости должны находиться при таких относительных расположениях взаимодействующих атомов, когда атомы максимально удалены друг от друга или максимально сближены.
Рассмотрим более подробно характер явления заторможенного внутреннего вращения на примере молекулы этана, СН3-СН3. Эта молекула является простейшей для случая, когда одинарная связь, совпадающая с осью внутреннего вращения, образована двумя атомами углерода в состояниях с тетраэдрической системой валентных связей. Случай этот наиболее изучен и важен, так как предельные углеводороды и их производные являются основой органической химии, а указанный тип одинарной углерод-углеродной связи, т. е, звенья из двух тетраэдрических узлов, встречаются не только в молекулах этих веществ, но и в молекулах многих других классов соединений.
Две предполагаемые конфигурации ядерного скелета молекулы этана, соответствующие максимальному удалению и максимальному сближению не связанных между собой, но попарно взаимодействующих атомов водорода двух тетраэдрических узлов, могут быть представлены в виде пространственных моделей или проекций на плоскость, перпендикулярную оси внутреннего вращения, как это показано на рис. 2.
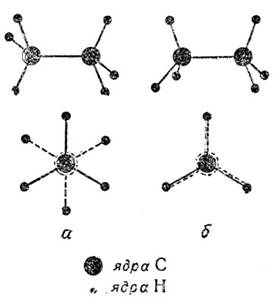
Рис.2. Пространственные модели и проекции Ньюмера на плоскость, перпендикулярную связи С-С, для устойчивой 'шахматной' (а) и неустойчивой 'затененной' (б) форм молекулы этана
Физическими методами исследования равновесных ядерных конфигураций, в частности спектроскопическими, было показано, что в случае молекул типа этана, и вообще звеньев из двух узлов с тетраэдрической направленностью связей, устойчивой, т. е. соответствующей минимуму потенциальной энергии, является форма, представленная на рис. 2, А и названная "шахматной". Эта равновесная ядерная конфигурация молекулы этана имеет зеркально-поворотную ось симметрии шестого порядка, S6, проходящую через ядра атомов углерода. Ядра атомов водорода в группах - СН3 молекулы этана совершают - крутильные колебания относительно положений равновесия, причем может быть несколько состояний такого колебательного движения или энергетических уровней крутильного колебания СН3-групп. При достаточно больших амплитудах кручения, т. е. при достаточном энергетическом возбуждении, в молекуле этана практически может происходит полный поворот одной метальной группы относительно другой на 360°, т. е. крутильное колебание переходит в свободное внутреннее вращение молекулы.
Качественная кривая зависимости потенциальной энергии от угла внутреннего вращения в молекуле этана (и молекулах подобного типа) представлена на рис. 3.
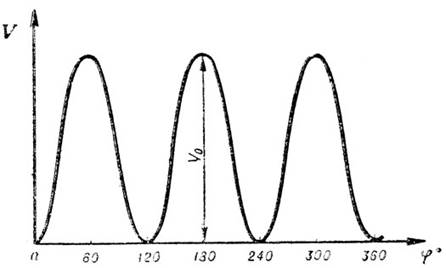
Рис.3. Потенциальная кривая внутреннего вращения молекул типа этана
Минимумы этой кривой соответствуют, "шахматным", а максимумы - неустойчивым "затененным" ядерным конфигурациям молекулы, получающимся при постепенном повороте метильных групп друг относительно друга 360°. Относительное расположение экстремумов на потенциальной кривой описывается также формулой Питцера:

Где ц - угол внутреннего вращения с началом его отсчета от одной из трех возможных "шахматных" ядерных конфигураций, a V0 - так называемый тормозящий потенциал внутреннего вращения или потенциальный барьер (см. рис. 3). Энергия крутильного колебания никогда не равна нулю, как и колебания любой другой формы, о чем говорилось выше. Поэтому, строго говоря, потенциальный барьер равен не разности между максимумом и минимумом на кривой потенциальной энергии, а разности энергий первого энергетического уровня над этой кривой, который отвечает уже свободному внутреннему вращению метильных групп в молекуле этана, и нулевого уровня крутильного колебания этих групп, для которого колебательное квантовое число VКрут=0.
Поскольку атомы водорода в метильных группах ничем неотличимы друг от друга, то и все три "шахматные" конфигурации ядерного скелета молекулы этана, получающиеся при повороте одной метильной группы относительно другой на углы ?, равные 0 (или 360°), 120 и 240°, тождественны друг другу, т. е. не различаются никакими свойствами. Каждая из этих ядерных конфигураций имеет один и тот же набор энергетических колебательных уровней, в том числе и уровней крутильного колебания. Число последних невелико, и они сравнительно низки по энергиям, так что в соответствии с законами статистики все они уже при обычных температурах достаточно, как говорят, заселены молекулами. Иными словами, каждая из молекул легко может возбудиться до любого, из этих уровней энергии, включая и уровень, соответствующий свободному внутреннему вращению метильных групп. Поэтому при обычных температурах в газообразном и жидком состояниях этана одна "шахматная" ядерная конфигурация молекулы может быстро переходить в другую, тождественную ей. Это явление возбуждения одной из устойчивых ядерных конфигураций молекулы от одного из энергетических состояний крутильного колебания до энергетического уровня свободного внутреннего вращения с последующим переходом на один из низких уровней крутильного колебания другой устойчивой ядерной конфигурации и может быть названо Заторможенным внутренним вращением молекулы с преодолением потенциального барьера V0.
Устойчивость "шахматных" конформаций вообще характерна для молекул и звеньев, подобных молекуле этана, т. е. образованных двумя тетраэдрическими узлами, когда все химические связи в них являются одинарными (предельные углеводороды и их производные, силаны и т. п.). Отсюда следует, что главными силами, определяющими возникновение потенциального барьера внутреннего вращения, являются пространственные силы отталкивания между непосредственно не связанными между собою атомами, так как в "шахматных" конформациях эти атомы наиболее удалены друг от друга.
Для нахождения наиболее выгодных относительных расположений в пространстве непосредственно не связанных атомов или атомных групп в молекулах стали даже пользоваться следующим критерием: расстояние между двумя несвязанными атомами не должно быть меньше суммы их вандерваальсовых (или межмолекулярных) радиусов.
Во многих случаях молекул предельных соединений такое представление действительно могло удовлетворительно объяснить геометрию устойчивых конформаций. Однако это все же грубое приближение. Взаимодействие непосредственно не связанных атомов носит весьма сложный характер, и в других случаях, устойчивыми могут оказаться "затененные" (рис.2б) положения атомов вращающихся групп.
При отсутствии осевой симметрии волчков, напр. в молекулах 1,2-дизамещенных этана, заторможенное внутреннее вращение приводит к явлению поворотной изомерии, представляющей собой частный случай конформационной изомерии, когда устойчивым конформациям соответствуют разные по глубине минимумы потенциальной энергии, т. е. возникают различающиеся по форме и свойствам поворотные изомеры (конформеры). В частности, у молекул типа 1,2-дизамещенных этана имеются три стабильных конформации - одна транс - (или Анти - )и две Гош-Конформации (см. рис. 4). Относительная стабильность поворотных изомеров определяется разностью их энергий
, т. е. разностью значений энергии в минимумах потенциальной кривой. Напр., транс-изомер 1,2-дихлорэтана более устойчив, чем гош-изомер, т. к. его энергия (в газовой фазе) ниже на ~ 5,6 кДж/моль. При достаточно низких потенциальных барьерах (несколько десятков кДж/моль) поворотные изомеры находятся в термодинамическом равновесии, положение которого зависит от температуры, давления и природы среды. Для барьеров порядка 3 кДж/моль время жизни конформеров составляет ~10-10С. При высоких значениях V0 (выше ~ 100 кДж/моль), когда В. в. отсутствует, конформеры даже при малой разности их энергий могут существовать как индивидуальные в-ва. В. в. молекул возможно в газовой и жидкой фазах, параметры
зависят от характера среды и электронного состояния молекулы. В кристаллах внутреннее вращение, как правило, отсутствует и стабилен лишь один конформер; иногда существуют твердые фазы (напр., у некоторых фреонов), в которых стабильны разные конформеры и между ними осуществляются переходы.
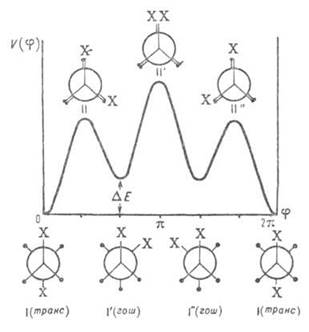
Рис. 4. Потенциальная функция внутреннего вращения молекул типа 1,2-дизамешенного этана. I-I''-поворотные изомеры (конформеры), или стабильные заторможенные конформации, II-II"-нестабильные заслоненные конформации.
Явления заторможенного внутреннего вращения и поворотной изомерии молекул оказывают влияние на термодинамические, электрические, оптические и другие свойства веществ. Внутреннее вращение необходимо учитывать при расчете термодинамических функций методами статистической термодинамики.
В случае поворотной изомерии свойства вещества определяются как свойства равновесной смеси изомеров и зависят от внешних условий, влияющих на положение равновесия. Например, эффективный дипольный момент µ зависит от температуры. Если µ поворотных изомеров различны, как, например, у Транс - (µ = 0) и Гош - (µ?0) конформеров 1,2-дихлорэтана, то при изменении температуры значение измеряемого µ будет приближаться к значению, характерному для изомера, концентрация которого будет при этом возрастать. В жидкой фазе и в среде полярных растворителей повышается устойчивость более полярного гош - изомера в результате взаимодействия молекул растворителя и растворенного вещества. Поворотные изомеры, имея различные равновесные конфигурации, различаются своими колебательными и вращательными спектрами. При увеличении числа осей внутреннего вращения в молекуле возрастает и число ее возможных конформаций.
Похожие статьи
-
Общие представления о внутреннем вращении молекул - Внутреннее вращение молекул
Физические и химические свойства веществ во многом зависят от строения образующих их молекул. Немаловажную роль играет не только их состав, но и...
-
Хиральность молекул - Оптические изомеры и их влияние на организм человека
Хиральность (молекулярная хиральность) -- свойство молекулы быть несовместимой со своим зеркальным отражением любой комбинацией вращений и перемещений в...
-
Ван-дер-Ваальсовы силы: ориентационная, индукционная и дисперсионная составляющие. Полная энергия межмолекулярного взаимодействия Молекула - Химически...
-
В зависимости от направления перекрывания атомных орбиталей различают два вида ковалентной связи: -связь возникает при перекрывании атомных орбиталей...
-
Термодинамика. Химическая термодинамика. Термодинамические системы. Энергия. Внутренняя энергия Термодинамика изучает взаимное превращение теплоты,...
-
Молекулы, радикалы и ионы - Введение в химию
Молекула - наименьшая частица вещества, определяющая его свойства, способная к самостоятельному существованию. Состоит из одинаковых или разных атомов....
-
С помощью программы Hyper Chem Professional 8.0 были рассчитаны характеристики электронной структуры молекулярной системы метилэтилового эфира. Рисунок...
-
Целью данной работы стало построение пространственного изображения молекулы метилэтилового эфира, проведение оптимизации ее геометрических параметров...
-
Химическая связь и строение молекул вещества. - Роль химии в повседневной жизни
Атомистические воззрения возникли первоначально на Древнем Востоке, в античных Греции и Риме. Первоначально атомное учение предполагало существование...
-
Н 2О = О 2- + 2Н+. В Щелочной среде атомы кислорода можно взять из гидроксид-ионов, при этом образуются молекулы воды: 2ОНЇ = О 2- + Н 2О. Пример 1....
-
План-конспект теоретической самоподготовки Поверхностное натяжение Состояние молекул вещества, находящегося в поверхностном слое твердого тела или...
-
Дипольный момент молекулы и связи
Представим себе, что можно найти "центры тяжести" отрицательных и положительных частей молекулы. Тогда условно все вещества можно разбить на две группы....
-
Предметом статьи является обоснование необходимости использования математических методов в процессе внутреннего мониторинга операций организациями с...
-
ВВЕДЕНИЕ, СТРОЕНИЕ МОЛЕКУЛ И СВОЙСТВА ВОДЫ - Химические свойства и строение воды
Вода - ценнейший природный ресурс. Вода играет исключительную роль в процессах обмена веществ, составляющих основу жизни. Огромное значение вода имеет в...
-
Ступенчатое регулирование скорости можно осуществить, используя специальные многоскоростные асинхронные двигатели с короткозамкнутым ротором. Из...
-
Внутренняя энергия термодинамическая функцция состояния системы, ее энергия, определяемая внутренним состоянием. Внутренняя энергия складывается в...
-
1. В результате линейной комбинации две атомные орбитали (АО) формируют две молекулярные орбитали (МО) - связывающую, энергия которой ниже, чем энергия...
-
История открытия тиосульфата натрия, Строение молекулы и ее влияние на свойства - Тиосульфат натрия
Имя и время открытия тиосульфата натрия нам не известны. Во всяком случае в истории химии об этом не упоминается. Но в конце XVII и в начале XVIII века,...
-
Вращение рамки в магнитном поле, Токи Фуко - Характеристика электромагнитной индукции
Явление электромагнитной индукции используется для преобразования механической энергии и энергии электрического тока в генераторах. Рамка площадью S...
-
Так как частота вращения магнитного поля статора nо = 60f/р, то регулирование частоты вращения асинхронного двигателя можно производить изменением...
-
Введение резисторов в цепь ротора приводит к увеличению потерь мощности и снижению частоты вращения ротора двигателя за счет увеличения скольжения,...
-
Поляриметр. Удельное вращение - Оптические изомеры и их влияние на организм человека
Различить оптические изомеры можно с помощью поляриметра - прибора, измеряющего угол поворота плоскости поляризации. Величину оптической активности...
-
Внутренние связи на предприятии - это и есть та основополагающая, без которой предприятие вообще не может существовать. Также внутренние связи можно...
-
Влияние внешних и внутренних факторов на скорость химической коррозии - Химическая коррозия
Внешними называют факторы, связанные с составом коррозионной среды и условиями протекания коррозии (температура, давление, скорость движения среды и...
-
Строение белков - Строение белков, качественные реакции на белки
Среди органических веществ Белки , или Протеины , -- самые многочисленные, наиболее разнообразные и имеющие первостепенное значение биополимеры. На их...
-
Плоскости носитель траекторий перемещения точек параллельны плоскости проекций. Траектория - дуга окружности, центр которой находится на оси...
-
Анализ внутренней среды организации Для проведения SNW-анализа: - Выберем основные показатели, характеризующие каждый из срезов внутренней среды...
-
ВРАЩЕНИЕ И ИНТЕРПРЕТАЦИЯ ФАКТОРОВ - Многомерный статистический анализ
Вращение факторов. Матрицу факторных нагрузок называют также матрицей факторного отображения. Она содержит коэффициенты, используемые для выражения...
-
С помощью программы Hyper Chem Professional 8.0 была проведена оптимизация геометрических параметров молекулы метил этилового эфира методом молекулярной...
-
Круговорот углерода связан с использованием СО при фотосинтезе; в процессе дыхания растение возвращает СО в атмосферу. Животные, поедая растения,...
-
Валовой внутренний продукт (ВВП) - общий показатель экономической деятельности страны, центральный макроэкономический показатель системы национальных...
-
Активация молекул в катализе - Промотирование катализаторов
Активация молекул происходит в результате взаимодействия молекул с катализатором: с поверхностью - в гетерогенном, с молекулами, ионами, комплексами - в...
-
Площадь поверхности вращения - Определенный интеграл
Пусть кривая АВ Является графиком функции У = f(х) ? 0, где Х [а;b], А функция У = F(х) И ее производная У' = f'(х) Непрерывны на этом отрезке....
-
Q(x) - соответствует площади боковой поверхности данного тела от точки А до точки х. Q(x)>х€[a, x]. Q (x+?x)>х€[a, x+?x], тогда ?Q=Q...
-
Пусть в пространстве дано тело, ограниченное некоторой замкнутой поверхностью и пусть известна площадь любого его сечения, полученного плоскость,...
-
Введение, Классификация Фенолов, Физические свойства фенола, Химические свойства - Синтез фенола
Фенол химический синтез Целью данной курсовой работы является изучение способов синтеза фенолов, в частности фенола. Свойства фенолов специфичны, поэтому...
-
ЭНЕРГЕТИЧЕСКИЙ БАРЬЕР - Процесс катализа
Все каталитические реакции - самопроизвольный процесс, т. е. протекают в направлении убыли энергии Гиббса - убыли энергии системы. Давно уже было...
-
Строение углеводов Рассмотрим стереоизомерию углеводов на примере моносахаридов. Молекулы моносахаридов содержат несколько центров хиральности, что...
-
Химические свойства кремнийорганических полимеров - Кремнийорганические полимеры
Силоксаны содержат два или более атомов кремния, связанных посредством одного или нескольких атомов кислорода: Два атома кремния, связанные таким...
-
Ионизация газов - Электрический ток в газах
Вышеописанный опыт показывает, что в газах под влиянием высокой температуры появляются заряженные частицы. Они возникают вследствие отщепления от атомов...
Заторможенное внутреннее вращение - Внутреннее вращение молекул