Дипольный момент молекулы и связи
Представим себе, что можно найти "центры тяжести" отрицательных и положительных частей молекулы. Тогда условно все вещества можно разбить на две группы. Одну группу составляют те, в молекулах которых оба "центра тяжести" совпадают. Такие молекулы называются неполярными. К ним относятся все ковалентные двухатомные молекулы вида А2, а также молекулы, состоящие из трех и более атомов, имеющие высокосимметричное строение, например СО2, СS2 , СCl4 , С6 H6. Во вторую группу входят все вещества, у которых "центры тяжести" зарядов в молекуле не совпадают, молекулы которых характеризуются электрической асимметрией. Эти молекулы называют полярными. К ним относятся молекулы вида АВ, в которых элементы А и В имеют различную электроотрицательность, и многие более сложные молекулы. Систему из двух разноименных электрических зарядов, равных по абсолютной величине, называют диполем.
Полярность молекулы (и полярность связи) характеризуется дипольным моментом молекулы (или связи)
Величина дипольного момента сильно влияет на свойства полярных молекул и веществ, построенных из таких молекул. Полярные молекулы поляризуются в электрическом поле, устанавливаясь по силовым линиям поля, ориентируются в электрических полях, создаваемых ионами в растворах, взаимодействуют между собой, замыкая свои электрические поля. Дипольный момент образуется за счет смещения центров положительного и отрицательного зарядов на некоторую величину l, называемую длиной диполя.
Чем более полярны молекулы, чем значительнее смещены валентные электронные пары к одному из атомов, тем больше. И наоборот, если электрическая ассиметрия молекул незначительна, то величина невлика ?.
Для системы из двух частиц дипольный момент ? равен: = el.
Где e - величина заряда;l - расстояние между центрами. Однако, определяя сразу величину дипольного момента, мы не знаем ни величины заряда e, локализованного в полярной молекуле, ни расстояния между центрами l.
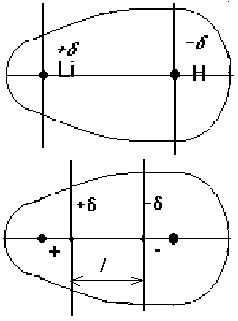
Принимаем e равным заряду электрона(1,6021*10-19Кл) и тогда получаем приведенную длину диполя l, которая является условной величиной. В качестве единицы измерения дипольных моментов принят дебай(названный в честь голландского физика П. Дебая, разработавшего теорию полярных молекул).в системе СИ 1D=0,33*10-29Кл*м.
Дипольные моменты обычно определяют экспериментально, измеряя относительную диэлектрическую проницаемость ?? веществ при различных температурах. Если вещество поместить в электрическое поле, создаваемое конденсатором, то емкость последнего возрастет в ?? раз, т. е. ?=c/c0 (где c0 И с - емкость конденсатора в вакууме и в среде вещества).
Энергия электрического поля в конденсаторе U выражается соотношением:
U=1/2cV2,
Где V - напряжение на обкладках конденсатора.
Из приведенного уравнения видно, что конденсатор в среде вещества имеет больший запас энергии, чем в вакууме (с>1). Это обусловлено тем, что под действием электрического поля происходит поляризация среды - ориентация диполей и деформация молекул. Первый эффект зависит от температуры, второй - не зависит.
Температурную зависимость относительно диэлектической проницаемости вещества ???выражает уравнение Ланжевена-Дебая:
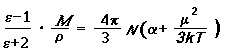
'
Где М - относительная молекулярная масса вещества; ??плотность вещества, NA- постоянная Авогадро; k - постоянная Больцмана, равная R/ NA (R - универсальная газовая постоянная); деформационная поляризуемость молекул.
Измерив ?при двух температурах, с помощью уравнения Ланжевена-Дебая можно определить ?и ??Есть и другие методы экспериментального определения ?
Значения дипольных моментов для некоторых связей между разнородными атомами приведены в таблице:

Не следует путать дипольный момент связи и дипольный момент молекулы, так как в молекуле могут существовать несколько связей, дипольные моменты которых суммируются как векторы. Кроме того, на величину дипольного момента молекулы могут влиять магнитные поля орбиталей, содержащих электронную пару,- "неподеленные" электроны. Большое влияние на полярность молекулы оказывает ее симметрия.
Например, молекула метана CH4 обладает высокой степенью симметрии (центрированный тетраэдр), и поэтому векторная сумма дипольных моментов связей (?=0,4D) равна нулю:
?Св=0
Если заменить водородные атомы на атомы хлора и получить молекулу CCl4, у которой дипольный момент связи ?=2,05D, те в пять раз больший, чем для C-H, то результат останется прежним, так как молекула CCl4 обладает таким же строением.
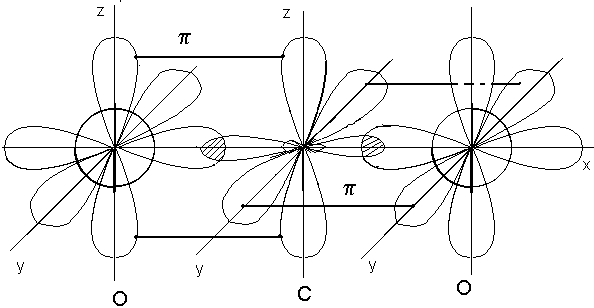
Рис.2. Схема строения молекулы СО2
Связь С=О обладает дипольным моментом 2,7D, однако линейная молекула СО2
Является неполярной до тех пор, пока ее структура не исказится под действием других молекул(напр, Н2О).Структура линейной молекулы СО2, в которой атом углерода гибридизирован частично: 2s22p2 2s12p3 2q22p2 ,представлена на рис.2. Дипольные моменты связей, обладая различными знаками, дают общий депольный момент, равный нулю:
?Св=0.
Таким образом, полярность молекул определяется довольно сложно, так как она учитывает все взаимодействия, которые могут возникнуть в такой сложной структуре, как молекула. Кроме того, "полярность" молекулы не определяется лишь величиной дипольного момента, а зависит также от размеров и конфигурации молекул. Например, молекула воды более резко проявляет свои полярные свойства (образование гидратов, растворимость и т. д.), чем молекула этилового спирта, хотя дипольные моменты у них почти одинаковые (?н2О=1,84D; ?с2Н5Он=1,70D).
Значения дипольных моментов для некоторых полярных молекул:
|
Молекула |
? |
Молекула |
? |
Молекула |
? |
Молекула |
? |
Молекула |
? |
|
Н2 |
0 |
HF |
1,82 |
Н2О |
1,84 |
CO2 |
0 |
CH4;CCl4 |
0 |
|
О2 |
0 |
HCl |
1,07 |
Н2S |
0,93 |
SO2 |
1,61 |
CH3Cl |
1,86 |
|
N2 |
0 |
HBr |
0,79 |
NН3 |
1,46 |
SO3 |
0 |
CH2Cl2 |
1,57 |
|
Cl2 |
0 |
HI |
0,38 |
PН3 |
0,55 |
SF6 |
0 |
CHCl3 |
1,15 |
Дипольный момент полярной молекулы может изменять свою величину под действием внешних электрических полей, а также под действием электрических полей других полярных молекул, однако при удалении внешних воздействий дипольный момент принимает прежнюю величину. Некоторые молекулы, неполярные в обычных условиях, могут получать так называемый индуцированный или "наведенный" дипольный момент, тоже исчезающий при снятии поля. Величина индуцированного момента в первом приближении пропорциональна напряженности электрического поля E: Инд=0E, где?- коэффициент поляризуемости, []=м3,??0?электрическая постоянная.
Физико-химические особенности полярных молекул определяются их способностью реагировать на внешние электрические поля (электрическая поляризация) и на поля, созданные другими полярными молекулами. В частности, за счет взаимодействия с полярными молекулами воды такие полярные молекулы, как HF, HCl и др.,могут подвергаться электролитической диссоциации.
Дополнительно используемая литература:
- 1. Общая и неорганическая химия. Карапетьян, Дракин 2. Теоретические основы общей химии. Горбунов, Гуров, Филиппов
Похожие статьи
-
Химическая связь и строение молекул вещества. - Роль химии в повседневной жизни
Атомистические воззрения возникли первоначально на Древнем Востоке, в античных Греции и Риме. Первоначально атомное учение предполагало существование...
-
1. В результате линейной комбинации две атомные орбитали (АО) формируют две молекулярные орбитали (МО) - связывающую, энергия которой ниже, чем энергия...
-
Химия и физика - Связь химии с другими науками
К общим вопросам химии и физики относятся строение веществ и движение тех частиц, из которых вещества построены. Показательно, что самые первые шаги в...
-
Молекулы, радикалы и ионы - Введение в химию
Молекула - наименьшая частица вещества, определяющая его свойства, способная к самостоятельному существованию. Состоит из одинаковых или разных атомов....
-
Хиральность молекул - Оптические изомеры и их влияние на организм человека
Хиральность (молекулярная хиральность) -- свойство молекулы быть несовместимой со своим зеркальным отражением любой комбинацией вращений и перемещений в...
-
Химическая связь - Квантовые концепции в химии
Химия изучает процессы превращения молекул при воздействиях и при воздействии на них внешних факторов (теплоты, света, электрического тока, магнитного...
-
Водородные соединения, Водородная связь - Свойства водорода
В этой таблице слева легкой тенью выделены клетки элементов, образующих с водородом ионные соединения - гидриды. Эти вещества имеют в своем составе...
-
Свойства связей и отношений - Системная революция и принцип дуального управления
Отвлекаясь от конкретного содержания реальных связей и отношений, можно выделить три наиболее общих группы синтаксических свойств бинарных связей и...
-
При взаимодействии атомао м/у ними может возникнуть хим. связь, приводящая к образованию устойчивой многоатомной с-мы - молекулы, кристалла. Чем прочнее...
-
ВВЕДЕНИЕ, СТРОЕНИЕ МОЛЕКУЛ И СВОЙСТВА ВОДЫ - Химические свойства и строение воды
Вода - ценнейший природный ресурс. Вода играет исключительную роль в процессах обмена веществ, составляющих основу жизни. Огромное значение вода имеет в...
-
Химическая связь - это взаимное сцепление атомов в молекуле и кристаллической решетке в результате действия между атомами электрических сил притяжения....
-
Химическая связь и валентность, Валентность - Квантовые концепции в химии
Валентность Валентность - это способность атома присоединять или замещать определенное число других атомов или атомных групп с образованием химической...
-
Физика создания момента по картине синусоидальных величин - Электромеханические преобразователи
Создание момента в результате взаимодействия синусоидально распределенных магнитных полей: 1 - сталь ротора; 2 - сталь статора; 3 - N -я гармоника...
-
Существует несколько форм уравнения моментов, две из которых наиболее полезны: . Здесь Н С Т , В Р Т - максимальные величины напряженности и индукции...
-
Способы определения моментов исполнительных двигателей - Электромеханические преобразователи
Момент вращения, действующий в электрической машине в процессе преобразования энергии, может быть определен как отношение электрической мощности к...
-
Главные оси и главные моменты инерции - Геометрические характеристики поперечных сечений
Рис. 3 Посмотрим, как изменяются моменты инерции при повороте осей координат. Положим, даны моменты инерции некоторого сечения относительно осей Х, у (не...
-
Методы изучения связи качественных признаков - Основы эконометрики
При наличии соотношения между вариацией качественных признаков говорят об их ассоциации, взаимосвязанности. Для оценки связи в этом случае используют ряд...
-
Модель парной линейной регрессии - Математическое описание связи: регрессия, корреляция
Предположим, что у нас есть все основания считать, что два экономических показателя взаимосвязаны. Например, уровень инфляции и уровень безработицы в...
-
История открытия тиосульфата натрия, Строение молекулы и ее влияние на свойства - Тиосульфат натрия
Имя и время открытия тиосульфата натрия нам не известны. Во всяком случае в истории химии об этом не упоминается. Но в конце XVII и в начале XVIII века,...
-
Химия и биология - Связь химии с другими науками
На уроках биологии вы уже встречались как с химическими веществами, так и с химическими реакциями. Так, вы узнали, что любая клетка, растительная или...
-
Строение Солнечной системы. Солнечно-Земные связи - Основы естественно-научных знаний
Вселенная -- это весь окружающий нас мир, безграничный во времени и пространстве и бесконечно разнообразный по формам, которые принимает вечно движущаяся...
-
ХИМИЧЕСКАЯ СВЯЗЬ - Неограническая химия
Задание 2.1. Для двух, указанных по варианту (табл. II.2), молекул с позиций метода валентных связей показать образование молекул и ответить на следующие...
-
Взаимодействия, связи и отношения - Системная революция и принцип дуального управления
Понятия связи и отношения не являются тождественными. Отношение выражает либо принадлежность некоторого признака элементу, либо опосредовано (посредством...
-
Рассмотрим теперь, какое влияние на свойства веществ оказывает порядок соединения атомов в молекуле. Обратимся сначала к историческим фактам. Изучая...
-
Основы новой теории сформулировал 1861 г. профессор Казанского университета Александр Бутлеров. В химии к тому времени уже значительное распространение...
-
Площа плоскої області обчислюється за формулою (6) У полярній системі координат формула (6) має вигляд (7) Об'єм циліндричного тіла, обмеженою зверху...
-
Разработав теорию и подтвердив правильность ее синтезом новых соединений, А. М. Вутлеров не считал теорию абсолютной и неизменной. Он утверждено, что она...
-
ТЕСНОТА И ЗНАЧИМОСТЬ СВЯЗИ - Многомерный статистический анализ
Соответствующий статистический вывод включает определение тесноты и значимости связи между Х и Y. Тесноту связи измеряют коэффициентом детерминации R 2 ....
-
Винилхлорид -- достаточно активное химическое соединение, чьи химические свойства определяются как наличием двойной связи, так и атома хлора. Наибольший...
-
Моменты инерции сечения - Геометрические характеристики поперечных сечений
В дополнение к статическим моментам рассмотрим еще три следующих интеграла: Через Х и У обозначены текущие координаты элементарной площадки DF в...
-
Важной задачей статистики является разработка методики статистической оценки социально-экономических явлений, которая осложняется тем, что многие...
-
Теорема 1. Предел постоянной равен самой постоянной. . Доказательство. f(x)=с, докажем, что . Возьмем произвольное e>0. В качестве d можно взять любое...
-
Важнейшей задачей науки является исследование объективно существующих связей между явлениями. Знание их характера и величины может помочь управлять...
-
Химические свойства. Образование ковалентной связи по донорно-акцепторному механизму - Аммиак
1. Аммиак - основание Льюиса. Его раствор в воде (аммиачная вода, нашатырный спирт) имеет щелочную реакцию (лакмус - синий; фенолфталеин - малиновый)...
-
Моменты распределений дискретных случайных величин. - Распределение вероятности случайных величин
Итак, закон распределения вероятностей дискретной СВ несет в себе всю информацию о ней и большего желать не приходится. Не будет лишним помнить, что этот...
-
Предмет органической химии. Изучая неорганическую химию, мы знакомились с веществами самого разнообразного состава и при этом ни разу не встречали, чтобы...
-
Связь phenoxy гербицидов с саркомами мягких тканей и лимфомами типа нон-Ходкина - Токсичные вещества
Саркомы мягких тканей и лимфомы нон-Ходкина связывают с воздействием phenoxy гербицидов с 1970-х гг. после ряда докладов в Швеции. При изучении...
-
В общем случае: , где Для не корреляционных случайных величин: Ответ на билет 15 В широком смысле слова, закон больших чисел характеризует устойчивость...
-
Коэффициент детерминации - Математическое описание связи: регрессия, корреляция
Предположим, что экономические предпосылки и анализ расположения точек на корреляционном поле позволил нам выдвинуть гипотезу о том, что зависимость...
-
Топологический анализ связей и отношений - Системная революция и принцип дуального управления
Среди основных морфологических типов связей и отношений, определяющих внутреннее строение дискретных систем, прежде всего следует выделить...
Дипольный момент молекулы и связи