Оптимальный температурный режим и способы его осуществления в промышленных реакторах - Химические процессы и реакторы
В предыдущих параграфах были рассмотрены варианты тепловых режимов химических реакторов и способы учета теплопереноса в реакторе при разработке математической модели.
Температурный (тепловой) режим проведения химического процесса, обеспечивающий экономически целесообразную максимальную производительность единицы объема реактора (интенсивность) по целевому продукту, называют Оптимальным.
Подход к разработке оптимального температурного режима может быть различным в зависимости от типа химической реакции. Очевидно, что максимальная интенсивность реактора будет достигнута при проведении процесса с максимально возможной скоростью. Рассмотрим поэтому, как влияет тип кинетического уравнения на выбор температурного режима.
Простые необратимые реакции. Уравнение скорости необратимых экзо - и эндотермических реакций можно записать в виде

(6.26)
Например, для реакции первого порядка

(6.27)
Скорость химической реакции является функцией нескольких переменных: температуры и степеней превращения реагентов (или их концентраций). С ростом температуры константа скорости реакции в соответствии с уравнением Аррениуса монотонно возрастает. Из уравнений (6.26) и (6.27) видно, что принципиальных ограничений повышения температуры с целью увеличения скорости необратимых реакций нет. С ростом степени превращения реагентов скорость реакции падает. Для компенсации этого уменьшения целесообразно увеличивать температуру.
Эндотермическая реакция сопровождается поглощением теплоты. Следовательно, такие реакции невыгодно проводить в адиабатических условиях, так как по мере протекания реакции ее скорость будет падать как из-за увеличения степени превращения, так и из-за уменьшения температуры. Более разумно проводить эндотермические процессы в реакторах с подводом теплоты (изотермических или в реакторах с промежуточным тепловым режимом), поддерживая температуру, максимально допустимую по конструкционным соображениям. Необходимо при этом дополнительно провести оптимизацию температурного режима, сопоставив экономические показатели: увеличение прибыли вследствие роста производительности реактора и возрастания расходов на поддержание высокой температуры.
Для необратимых экзотермических реакций рост степени превращения сопровождается выделением теплоты, и, следовательно, в адиабатическом режиме это приведет к возрастанию температуры реакционной смеси. Уменьшение скорости реакции вследствие увеличения степени превращения будет частично компенсироваться ростом константы скорости реакции с возрастанием температуры. Проводя такую реакцию в проточном адиабатическом реакторе, можно обеспечить высокую скорость химической реакции и высокую производительность реактора в автотермическом режиме без использования посторонних источников теплоты. При этом теплота реакционной смеси, выходящей из реактора, служит для нагрева исходных реагентов на входе в реактор.
Обратимые химические реакции. Проанализируем условия обеспечения оптимального температурного режима обратимых реакций на примере обратимой реакции первого порядка АR. Скорость такой реакции

(6.28)
Или [см. уравнение (6.20)]

(6.29)
С одной стороны, как и скорость необратимой реакции [см. выражение (6.27)], она зависит от константы скорости K1 и глубины химического превращения ХА, а с другой - определяется степенью приближения реакционной системы к состоянию химического равновесия и значением предельно достижимой степени превращения в равновесных условиях ХА,Е. Характер изменения скорости с ростом температуры будет разным для эндо - и экзотермических реакций.
Повышение температуры проведения обратимой эндотермической реакции приводит одновременно к росту K1 и увеличению равновесной степени превращения ХА,Е. Следовательно, при фиксированной степени превращения ХА скорость обратимой эндотермической реакции с ростом температуры монотонно увеличивается. Поэтому подход к разработке оптимального температурного режима этих реакций будет таким же, как и для необратимых эндотермических процессов.
Иначе обстоит дело с обратимыми экзотермическими реакциями. Так как скорость реакции - функция нескольких переменных (по меньшей мере, двух - T и ХА), то для анализа этой функции удобно использовать ее сечение при постоянстве всех переменных, кроме одной.
Такой подход облегчает и задачу графического представления функции. Функция П Переменных F (Х1, х2, ..., ХN) графически изображается некоторой поверхностью в (П + 1)-мерном пространстве. Сечения функции можно представить в виде семейства графиков на плоскости в координатах f (Х1, х2, ..., хN)ЧхI при постоянстве переменных Х1, х2, ..., ХI-1, хI+1, ..., ХN.
В частности, рассмотрим два вида сечений функций WRA(XA, T): При постоянных значениях хA и при постоянных значениях Т.
Выберем некоторое значение степени превращения 0 < ХА,1 < 1. Для этой степени превращения концентрация исходного реагента при протекании реакции АR составит СА,1 = сА,0(1 - хА,1), а концентрация продукта реакции CR,1 = сА,0ХА,1. С ростом температуры увеличивается константа скорости прямой реакции [растет сомножитель K1СА,0 в уравнении (6.29)], но одновременно уменьшается равновесная степень превращения ХА,Е и при фиксированном значении ХА,1 система находится ближе к состоянию равновесия [уменьшится второй сомножитель в уравнении (6.29)]. Таким образом, налицо два противоположных влияния. При низких температурах, когда темп изменения отношения ХА,1 /хА,E меньше темпа роста константы скорости K1 с увеличением температуры, преобладает влияние первого (возрастающего) сомножителя. При некоторой температуре T1,E выбранная степень превращения ХА,1 становится равновесной (ХА,Е при температуре T1,Е), тогда скорость прямой реакции равна скорости обратной реакции и суммарная скорость реакции будет формально равна нулю. При приближении к этой температуре (слева) преобладает влияние второго сомножителя, характеризующего степень приближения системы к равновесию. Очевидно, что существует какая-то оптимальная температура Т1,Т, при которой скорость реакции при заданной степени превращения является максимальной. Найдем эту температуру, пользуясь методами математического анализа (определение экстремума функции). Для этого продифференцируем функцию (6.28) по температуре, считая концентрации СА и CR постоянными, и приравняем производную нулю:

Отсюда при Т = ТТ

.
Или

(6.30)
Уравнение (6.30) позволяет определить оптимальную температуру для любой степени превращения кроме ХА = 0 и ХА = 1, когда функция wRA(T, xA) не имеет максимума.
Теперь можем построить сечение функции wRA(T, хА)ХА = xA-1 (рис. 6.9, кривая 1). Для другой степени превращения ХА,2 > хА,1 Функция WRА(T, хА)XА = xA,2 также имеет максимум. Точка Т2,Е пересечения графика с осью абсцисс находится левее T1,Е, так как у обратимых экзотермических реакций большая равновесная степень превращения достигается при меньшей температуре (при меньшей температуре наступает равенство ХА,2 и ХА,Е).
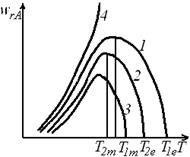
Рис. 6.9. Сечения функции WRA = WRA(XA, T) при постоянных температурах: 1, 2, 3 - Зависимости WRA (T) для степеней превращения XA,1, xА,2, xА,3 (XА,1 < хА,2 < хАу); 4 - зависимость WRA (T) для хА = 0
Из уравнения (6.30) следует, что с ростом степени превращения оптимальная температура Т2Т также уменьшается, потому что функция
У - хА(1 - ХА) в знаменателе уравнения является возрастающей. Таким образом, кривая wRA(T)ХA = хA,2 (кривая 2) будет находиться ниже кривой WRA(T)ХA = хA,1 (кривая 1) и ее максимум будет сдвинут влево.
Соединив точки максимумов (рис. 6.10) на различных сечениях WRA(T), получим линию оптимальных температур.
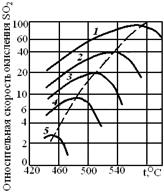
Рис. 6.10. Зависимость скорости окисления диоксида серы на ванадиевом катализаторе от температуры при различных степенях превращения SO2: 1 - XSO2 = 0,7; 2 - XSO2 = 0,8; 3 - xSO2 = 0,85; 4 - XSO2 = 0,9; 5 - xSO2 = 0,95; штриховая линия - линия оптимальных температур
Проведение процесса по линии оптимальных температур предполагает, что по мере увеличения степени превращения температуру в реакторе нужно уменьшать, чтобы скорость реакции всегда оставалась максимально возможной.
Чтобы убедиться в том, что скорость реакции действительно не может быть выше, чем при проведении процесса по линии оптимальных температур, рассмотрим сечения функции WRA(T, xA) при фиксированных температурах, т. е. зависимость скорости реакции от степени превращения.
Если Т - Т1 = Const, величины K1 и ХА,Е, зависящие от температуры и входящие в уравнение (6.29), также являются постоянными. Тогда уравнение (6.29) описывает прямую, пресекающую ось абсцисс в точке ХА = хА,Е и ось ординат в точке WRA = k1(Т1) сА,0 (рис. 6.11, линия 1). Для другой температуры Т2 > T1, точка пересечения прямой с осью абсцисс сдвинется влево, а точка пересечения с осью ординат - вверх.
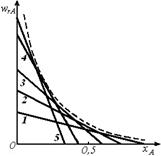
Рис. 6.11. Сечения функции WRA = wRA(XA, T) при постоянных температурах: 1-5 - зависимости WRA(XA) для температур Т1, Т2, T3, Т4, Т5 (T1<Т2<Т3<<Т4<Т5); штриховая линия - линия оптимальных температур
На рис. 6.11 нанесено семейство таких сечений, отвечающее условию T1 < Т2< Т3< T4 < ... < ТN. Линия оптимальных температур будет получена в этом случае как огибающая этого семейства прямых. Из рис. 6.11 видно, что ни при каких температурах скорость реакции не может быть выше скоростей, определяемых линией оптимальных температур.
При решении практических задач линию оптимальных температур часто строят в координатах ХА - Т. Тогда это линия, абсциссы точек которой - температуры, обеспечивающие максимальную скорость реакции для степеней превращения, являющихся ординатами этих точек. Для построения такой кривой можно воспользоваться уравнением типа (6.30). На рис. 6.12 приведена линия оптимальных температур для процесса окисления диоксида серы на ванадиевом (V2O5) катализаторе при составе исходной газовой смеси (в объемных долях, %) 7 % SO2 и 11 % О2. Линии 2 отвечают условию, когда скорость реакции составляет 80 % максимальной.
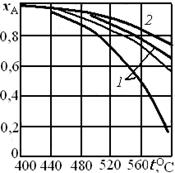
Рис. 6.12. Зависимость степени превращения диоксида серы на ванадиевом катализаторе от температуры: 1 - линии, отвечающие условию wRA = 0,8WRAOpt; 2 - равновесная кривая; штриховая линия - линия оптимальных температур WRA = wRAOpt
Способы осуществления оптимального температурного режима
Решение практической задачи проведения процесса в промышленном реакторе в соответствии с оптимальным температурным режимом зависит от многих факторов и прежде всего от теплового эффекта и кинетики реакции.
Для эндотермических (обратимых и необратимых) реакций целесообразно химический процесс проводить в реакторах с подводом теплоты, причем желательно обеспечить достаточно равномерное распределение температуры по объему реактора. Распространенным типом аппаратов для проведения эндотермических реакций являются трубчатые реакторы, похожие по конструкции на кожухотрубные теплообменники. В этих аппаратах трубное пространство представляет собой собственно реактор, в котором реагенты движутся в режиме вытеснения, а по межтрубному пространству проходит теплоноситель, например топочные газы. Трубчатый реактор для проведения каталитических реакций, обогреваемый топочными газами (рис. 6.13), применяют, в частности, для паровой конверсии природного газа.
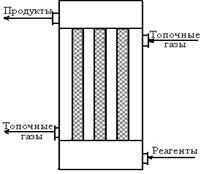
Рис. 6.13. Трубчатый реактор для проведения эндотермической реакции
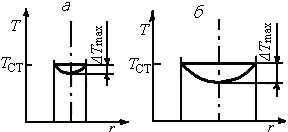
Рис. 6.14. Температурные профили в каналах малого (А) и большого (Б) диаметров при проведении эндотермической реакции
Аналогичную конструкцию имеет ретортная печь для синтеза бутадиена из этилового спирта, в которой катализатор вместо труб располагают в ретортах - узких каналах с прямоугольным сечением. В таких реакторах ширина поперечного сечения каналов, по которым движется реакционная смесь, должна быть невелика, чтобы получить достаточно равномерное распределение температуры по сечению. Так как в реальных реакторах гидродинамический режим отклоняется от режима идеального вытеснения, при котором в любом поперечном сечении условия выровнены, то температура в центре канала отличается от температуры у стенки. Из рис. 6.14 видно, что в трубах большого диаметра температура на оси трубы существенно ниже температуры у стенки. Следовательно, и скорость реакции в той части реакционного потока, которая движется близко к оси трубы, ниже средней скорости в аппарате. При проведении каталитических процессов можно наносить катализатор только на внутреннюю поверхность труб, что обеспечит примерно одинаковую температуру по всему реактору.
Гомогенные эндотермические реакции можно также осуществлять в реакторах с интенсивным перемешиванием и теплообменной поверхностью, так как и в этом случае будет обеспечено равномерное распределение температуры по реактору.
Экзотермические реакции проводят, как правило, либо в адиабатических условиях, либо в аппаратах с отводом теплоты.
При осуществлении необратимых экзотермических реакций рост температуры приводит однозначно лишь к увеличению скорости процесса. Для снижения энергетических затрат такие реакции выгодно проводить в автотермическом режиме, когда требуемая температура обеспечивается исключительно выделяющейся теплотой химической реакции без подвода энергии извне. Существуют две предельные температуры (нижняя и верхняя), между которыми целесообразно проводить процесс.
Нижней предельной является температура, при которой скорость экзотермической реакции (следовательно, и скорость выделения теплоты) достаточна для обеспечения автотермического режима. Ниже этой теплоты скорость тепловыделения меньше скорости отвода теплоты с реакционным потоком, выходящим из реактора, и температура в проточном адиабатическом аппарате будет падать.
Верхнее предельное значение температуры связано с побочными процессами (побочными химическими реакциями или побочными физическими явлениями), а также с жаропрочностью конструкционных материалов. Например, при проведении гетерогенных процессов обжига зернистого твердого материала повышение температуры выше некоторого предельного значения приводит к спеканию твердых частиц, а, следовательно, к увеличению времени их полного превращения и уменьшению производительности реактора (см. гл. 7). Часто рост температуры ограничен прочностью конструкционных материалов и нецелесообразностью применения дорогостоящих жаропрочных материалов.
При проведении экзотермических процессов микробиологического синтеза повышение температуры ограничено жизнестойкостью микроорганизмов. Поэтому такие процессы целесообразно осуществлять в реакторах с отводом теплоты, а во избежание локальных перегревов лучше использовать реакторы, гидродинамический режим в которых приближается к идеальному смешению. Интенсивное перемешивание в таких процессах не только обеспечивает равномерное распределение температуры, но и интенсифицирует стадии массопередачи кислорода из газовой фазы в жидкую фазу.
Обратимые экзотермические реакции нужно проводить в соответствии с линией оптимальных температур, т. е. понижая температуру в аппарате по мере роста степени превращения реагентов. Такой режим неосуществим ни в адиабатических, ни в изотермических реакторах. При адиабатическом режиме рост степени превращения сопровождается выделением теплоты и разогревом, а не охлаждением реакционной смеси; при изотермическом режиме температура остается постоянной и не меняется с ростом степени превращения.
Осуществить процесс строго по линии оптимальных температур чрезвычайно сложно. Это можно было бы сделать в реакторе с теплообменной поверхностью, работающем в режиме вытеснения, при условии, что количество теплоты, отводимое через стенку реактора, будет разным на различных участках аппарата. Реагенты перед началом реакции следовало бы нагреть до высокой температуры, а сразу же после их поступления в аппарат предусмотреть отвод теплоты. Если реактор разбить по длине на несколько участков, то, чтобы обеспечить движение по линии оптимальных температур, на каждом из них количество отводимой теплоты должно быть немного больше количества теплоты, выделяющейся в ходе реакции. Следует иметь в виду, что по мере увеличения степени превращения падает скорость реакции и, следовательно, уменьшается скорость тепловыделения. Поэтому на участках реактора, где реакция завершается, нужно отводить меньше теплоты, чем на начальных участках.
Некоторым приближением к линии оптимальных температур является проведение процесса в реакторе вытеснения, находящемся внутри теплообменной трубки, по которой проходит холодный реагент (см. рис. 6.15). Такая конструкция может быть применена, например, в колоннах синтеза аммиака.
Рабочая линия процесса, характеризующая изменение температуры с ростом степени превращения (кривая 3) на участке BCFD, Близка к линии оптимальных температур (штриховая линия). Однако указанные выше требования по условиям теплообмена в таком реакторе соблюдаются слабо. Действительно, на участке ВС Скорость тепловыделения максимальна, и нужно отводить много теплоты. В то же время скорость теплоотвода здесь мала, так как невелика движущая сила теплопередачи (?T). На участке FD Теплоты выделяется сравнительно немного, но по наружной трубке идет холодный газ, ?Т Велика и скорость теплоотвода выше необходимой. В какой-то степени этот недостаток можно устранить в аналогичных реакторах с двойными теплообменными трубками (см. рис. 6.16).
Вообще же на практике обычно считают, что степень приближения к линии оптимальных температур удовлетворительная, если для реактора выполняется условие
WR ? 0,8 WOpt. (6.31)
На графике ХА(Т) две линии, соответствующие условию WRA=0,8WRAOpt, проходят выше и ниже линии оптимальных температур, образуя область оптимальных температур, удовлетворяющую условию (6.31). При построении области оптимальных температур следует иметь в виду, что верхняя ограничивающая линия находится ниже равновесной кривой ХА,Е(Т). При выборе конструкции реактора и режима его работы стремятся к тому, чтобы большая часть рабочей линии процесса находилась внутри области оптимальных температур. Такому условию отвечают, в частности, рабочие линии на рис. 6.15, В и 6.16, Б.
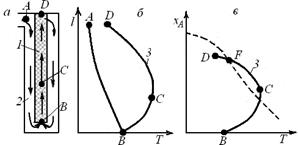
Рис. 6.15. Реактор с теплообменной трубкой (А), температурный профиль по длине реактора (Б) и зависимость степени превращения от температуры (В):
1 - реактор; 2 - теплообменная трубка; 3 - кривая изменения температуры по длине реактора (рабочая линия); штриховая линия - линия оптимальных температур
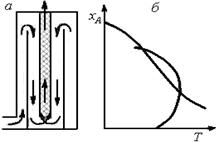
Рис. 6.16. Реактор с двойными теплообменными трубками (А) и профиль температур в нем (Б)
Сравнительно простым способом приближения к оптимальному режиму является проведение процесса в многосекционном реакторе вытеснения, в котором каждая секция работает в адиабатическом режиме, и между секциями имеется промежуточное охлаждение (рис. 6.17, А). На рис. 6.17, Б Показано, как будет проходить рабочая линия процесса в таком реакторе.
В секции 1 Реактора (рис. 6.17, А) процесс протекает адиабатически, причем изменения температуры и степени превращения связаны между собой уравнением (6.23).
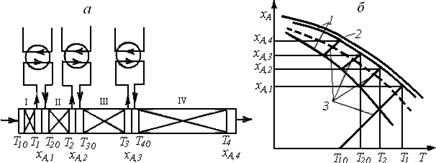
Рис. 6.17. Многосекционный реактор вытеснения с промежуточным отводом теплоты (А) и зависимости ХА(Т), характеризующие процесс в нем (Б):
- 1 - линии, отвечающие условию wRA = 0,8WRAOpt; 2 - Равновесная кривая; 3 - Рабочая линия процесса; штриховая линия - линия оптимальных температур (WRA = WRAOpt)
Объем секции должен быть таким, чтобы на выходе из нее достигалась степень превращения ХА,1, соответствующая пересечению адиабаты с верхней границей области оптимальных температур. Необходимое значение объема (или среднего времени пребывания) можно найти из решения системы уравнений материального и теплового балансов такого реактора.
На выходе из секции I реакционную смесь необходимо охладить от температуры T1 до температуры Т20, соответствующей нижней границе оптимальной области при ХА = хА,1. Затем реакционная смесь попадает в адиабатическую секцию II, второй теплообменник, секцию III и т. д. Так как скорость реакции по мере увеличения степени превращения уменьшается, объем каждой последующей секции возрастает.
Охлаждение реагентов между секциями адиабатического реактора можно вести не только косвенным теплообменом, но и введением свежей холодной реакционной смеси (см. рис. 6.18, А). В общем случае добавление к уже частично прореагировавшей смеси свежих реагентов изменяет их концентрацию и может привести к смещению равновесия. Положение линии оптимальных температур зависит и от положения равновесной кривой, следовательно, изменение равновесного состава несколько сместит и положение линии оптимальных температур (рис. 6.18, Б).
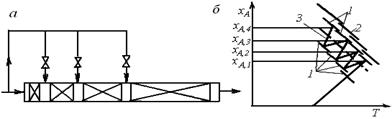

Рис. 6.18. Многосекционный реактор вытеснения с байпасными линиями ввода холодного газа между секциями (А) и зависимости ХА(Т), характеризующие процесс в нем (Б) (обозначения те же, что и на рис. 6.17)
Возможным вариантом осуществления процесса по оптимальному температурному режиму является и применение каскада реакторов смешения, в каждом из которых поддерживается своя температура благодаря введению теплообменных поверхностей (рис. 6.19, А). Задавшись температурой Т1, а следовательно, и степенью превращения в первой секции ХА,1, соответствующей верхней границе области оптимальных температур, можно рассчитать необходимый объем первой секции, рассматривая ее как реактор, работающий при постоянной температуре. Аналогично могут быть рассчитаны вторая и третья секции. Уравнение теплового баланса для таких реакторов позволит определить необходимую поверхность теплообмена и расход хладагента для поддержания в секциях температур, заданных рабочей линией процесса (рис. 6.19, Б).
Для каждого из рассмотренных вариантов возможна дальнейшая оптимизация процесса - расчет оптимальных объемов секций, начальных температур, объемных расходов в байпасных линиях и т. д. При такой оптимизации стремятся получить наиболее целесообразные экономические показатели процесса. Более подробно вопросы оптимизации, ее методы рассмотрены в специальной литературе.
Рис. 6.19. Схема каскада реакторов идеального смешения с отводом теплоты в секциях каскада (А) и зависимости ХА(Т), характеризующие процесс в нем (Б) (обозначения те же, что и на рис. 6.17)
Вопросы и упражнения
Для повторения и самостоятельной работы
В чем состоят принципиальные различия в условиях теплообмена для изотермического и адиабатического режимов работы реактора?
Составьте систему уравнений материального и теплового балансов для изотермического реактора идеального смешения.
Почему нельзя найти аналитическое решение системы уравнений материального и теплового балансов адиабатического реактора идеального смешения, работающего в стационарном режиме, относительно температуры в реакторе и достигаемой в нем степени превращения?
Используя графическое решение системы уравнений материального и теплового балансов адиабатического реактора идеального смешения, проанализируйте возможности увеличения достигаемой в реакторе степени превращения в случае проведения в нем:
- А) необратимой реакции; Б) обратимой эндотермической реакции; В) обратимой экзотермической реакции.
Найдите графическое решение системы уравнений материального и теплового балансов реактора идеального смешения промежуточного типа при проведении в нем обратимой эндотермической реакции.
Составьте алгоритм и схему расчета на ЭВМ изменения во времени температуры в периодическом реакторе идеального смешения с рубашкой обогрева, при проведении в нем необратимой эндотермической реакции первого порядка.
Составьте алгоритм и схему расчета на ЭВМ распределения степени превращения по длине реактора идеального вытеснения с промежуточным тепловым режимом, при проведении в нем необратимой экзотермической реакции первого порядка.
Какая величина выбирается в качестве критерия оптимизации при разработке оптимального температурного режима? Обоснуйте сделанный выбор.
Постройте линию оптимальных температур для проведения реакции АR, характеризующейся следующими кинетическими параметрами:

Как можно построить рабочую линию проведения обратимой экзотермической реакции в последовательно соединенных адиабатических реакторах вытеснения с промежуточным теплоотводом?
Похожие статьи
-
Проточный реактор идеального смешения в неизотермическом режиме - Химические процессы и реакторы
При составлении балансовых уравнений в качестве элементарного объема для реактора идеального смешения принимают полный реакционный объем V. Тепловые...
-
Уравнение теплового баланса. Тепловые режимы химических реакторов - Химические процессы и реакторы
В уравнении теплового баланса учитываются все тепловые потоки, входящие в реактор и выходящие из него. Такими потоками являются: Q Вых - физическая...
-
Химическая термодинамика позволяет решать вопрос о направлении протекания химических реакций и оценить предельно достижимые (равновесные) состояния...
-
Каскад реакторов идеального смешения - Химические процессы и реакторы
Каскад представляет собой несколько последовательно соединенных проточных реакторов (секций) идеального смешения (рис. 5.9). Реакционная смесь проходит...
-
Об эффективности осуществления любого промышленного процесса судят прежде всего по экономическим показателям, таким, как приведенные затраты,...
-
Классификация химических реакторов и режимов их работы - Химические процессы и реакторы
Химические реакторы для проведения различных процессов отличаются друг от друга по конструктивным особенностям, размеру, внешнему виду. Однако, несмотря...
-
Способы изменения скорости простых и сложных реакций - Химические процессы и реакторы
Как указывалось, скорость химической реакции зависит от большого числа различных факторов. Из кинетических уравнений следует, прежде всего, что скорость...
-
Расчет равновесия по термодинамическим данным - Химические процессы и реакторы
Расчет константы равновесия и изменения энергии Гиббса позволяет определить равновесный состав реакционной смеси, а также и максимально возможное...
-
Как видно из примеров 5.1 и 5.2, при одинаковых условиях проведения одной и той же реакции для достижения равной глубины превращения среднее время...
-
Реактор идеального вытеснения - Химические процессы и реакторы
Реактор идеального вытеснения представляет собой длинный канал, через который реакционная смесь движется в поршневом режиме (рис. 5.4). Каждый элемент...
-
Реактор идеального смешения - Химические процессы и реакторы
Для модели идеального смешения принимается ряд допущений. Допускается, что в результате интенсивного перемешивания устанавливаются абсолютно одинаковые...
-
Равновесие химических реакций - Химические процессы и реакторы
Под воздействием подвода или отвода энергии в форме теплоты или работы происходит изменение состояния термодинамической системы (значений...
-
Исходные данные для расчета реакторов - Проектирование химического реактора идеального смешения
При выборе конструкции и определении размеров реактора необходимо принимать во внимание различные факторы и, прежде всего, располагать данными о скорости...
-
Рассмотрение химических реакторов как сложных объектов в рамках иерархического подхода целесообразно провести на основе предварительного построения...
-
Способы смещения равновесия - Химические процессы и реакторы
Положение равновесия всегда зависит от внешних условий, а так как внешние условия не могут сохраняться неизменными, то равновесие рано или поздно...
-
Теоретические основы процесса Реакторы смешения - это емкостные аппараты с мешалкой или циркуляционным насосом. Человечество давно пользуется...
-
Тепловая устойчивость химических реакторов - Химические процессы и реакторы
При анализе совместного решения уравнений материального и теплового балансов адиабатического реактора идеального смешения для экзотермических реакций...
-
Зависимость константы равновесия от температуры - Химические процессы и реакторы
Функциональная зависимость константы равновесия от температуры при постоянном давлении передается Уравнением изобары Вант-Гоффа (2.9) Где ?H° -...
-
В современной химии известно большое число различных химических реакций. Многие из них осуществляются в промышленных химических реакторах и,...
-
ТЕПЛОПЕРЕНОС В ХИМИЧЕСКИХ РЕАКТОРАХ - Химические процессы и реакторы
Характер распределения температуры в химическом реакторе чрезвычайно важен при анализе протекающих в нем процессов, так как температура - один из...
-
Прежде чем рассмотреть отдельные типы химических реакторов в соответствии с приведенной классификацией, составим уравнение материального баланса по...
-
Структура математической модели химического реактора - Химические процессы и реакторы
Математические модели высоких уровней иерархии включают в себя, как правило, несколько уравнений, как конечных, не содержащих операторов...
-
Скорость гомогенных химических реакций - Химические процессы и реакторы
Скорость химической реакции W RJ принято выражать количеством (моль) N J одного из реагентов или продуктов, прореагировавшим (или образовавшимся) в...
-
ХИМИКО-ТЕХНОЛОГИЧЕСКИЙ ПРОЦЕСС И ЕГО СОДЕРЖАНИЕ - Химические процессы и реакторы
Химико-технологический процесс представляет собой совокупность операций, позволяющих получить целевой продукт из исходного сырья. Все эти операции входят...
-
Реакторами идеального (полного) смешения называются реакторы непрерывного действия, в которых осуществляется турбулентный гидродинамический режим. В них...
-
Химическое равновесие - Скорость химических процессов. Химическое равновесие, принцип Ле-Шателье
Химическое равновесие и его признаки. Равновесие истинное и заторможенное (ложное). Принцип Ле-Шателье. Константа равновесия и ее связь с...
-
Общие понятия и определения. Термодинамический и кинетический критерий реакционной способности химической системы. Скорость химической реакции. Факторы,...
-
Термодинамика - наука о взаимопревращениях различных форм энергии и законах этих превращений. Термодинамика базируется только на экспериментально...
-
Энтропия. Движущее начало химических процессов - Химическая термодинамика. Термохимия. Решение задач
Убедившись в полезности знания тепловых эффектов химических превращений, мы, тем не менее, не смогли ответить на вопрос: "Почему одни химические реакции...
-
ТЕРМОДИНАМИЧЕСКИЕ РАСЧЕТЫ ХИМИКО-ТЕХНОЛОГИЧЕСКИХ ПРОЦЕССОВ - Химические процессы и реакторы
При проектировании технологических процессов очень важны термодинамические расчеты химических реакций. Они позволяют сделать заключение о принципиальной...
-
Скорость химического превращения зависит от большого числа переменных. Результаты экспериментальных исследований различных реакций показали, что на...
-
Центральным аппаратом в любой химико-технологической системе, включающей целый ряд машин и аппаратов, соединенных между собой различными связями,...
-
Стехиометрия химических реакций - Химические процессы и реакторы
Для описания химических реакций, лежащих в основе промышленных химико-технологических процессов, используют основные законы химии - законы стехиометрии,...
-
Критерии самопроизвольного протекания процессов - Химическая кинетика, равновесия, термодинамика
А) В изолированной системе самопроизвольно идут только процессы с увеличением энтропии. S > 0 - процесс возможен, S Одновременно действуют обе тенденции...
-
Процесс получения винилхлорида сбалансированным методом из этилена состоит из шести стадий: 1. синтез 1,2-дихлорэтана прямым жидкофазным хлорированием...
-
Таким образом, подбор реактора для конкретного химического процесса, его расчет, оптимизация конструкции и условий проведения -- задача очень сложная,...
-
Описание технологического процесса Процесс каталитического риформинга осуществляют при сравнительно высокой температуре и среднем давлении, в среде...
-
СО2 + С = 2СО Если известно, что для СО2 ДG2980 = - 394572 Дж/моль и для СО ДG2980 = - 137334 Дж/моль. Рассчитаем ДG2980 = 2ДGСО - ДGСО2 = 2*(137,334)...
-
В промышленности синтез глиоксаля окислением этиленгликоля протекает в адиабатических условиях, оптимальный температурный режим процесса зависит от...
-
Введение - Проектирование химического реактора идеального смешения
Промышленный химический процесс - это экономически и экологически целесообразное производство требуемого продукта из исходного сырья....
Оптимальный температурный режим и способы его осуществления в промышленных реакторах - Химические процессы и реакторы