Катализ. Виды к. механизм действия К, Хим. равновесие: понятие, динамич. хар-р, конст. хим. равновесия - Основные понятия неорганической химии
К-изменение скорости хим. р-ции, под действием особых ве-в-катализаторов, кот. участвуют в ходе р-ции, но к концу ее остаются в неизменном кол-ве.
Виды: 1. по влиянию на скорость р-ции: положительный (ускорение хим. р-ции), отрицат (уменьшение).
Ингибитор в-ва уменьшающие скорость хим. р-ции.
2. по агрегатному сост-ю: гомогенный (реаг. ве-ва и кат. нах-ся в одном сост-ии); гетерогенный (реаг. в-ва нах-ся в одном сост-ии, а кат. в другом); ферментативный-протекающий в жив. организмах под действием особых ве-в-ферментов (в-ва белковой природы, их размер позоляет занимать промежуточное положение м/у гомогенным и гетерогенным), явл. очень высокоэффективным.
Механизм: присутствие кат. в реакционной системе снижает Е активации р-ции, анправляя р-цию по другому пути.
- 1. А+В-А...В >АВ 2. А+В+К-А....К+В>АК+В-АК...В>АВ+К.
Хим. равновесие: понятие, динамич. хар-р, конст. хим. равновесия
Больш-во хим. р-ций явл. Обратимыми - протекают в 2х противопол. направлениях.: прямая, обратная.
По мере протекании р-ции концентрация исх. в-в уменьшается, а в следств. с законом действ. масс, будет уменьш. скорость р-ции. Одновременно сэтим кол-во получаемого продукта будет возр-ть, и соотв. будет увелич-ся скорость обратной р-ции. В итоге скорости обеих р-ции выравниваются. Начиная с этого момента концентрации ве-в будут оставаться пост. Это сост-е когда
Vпрям.=Vобратн. - хим. равновесие.
Хим. равновесие - сост-е системы, кот. не изменяется во времени, при чем, эта неизменяемость не обусловлена протеканием к-либо внешнего процесса.
Хим. равн. явл. динамическим по характеру, т. е. сохраняется во времени, не вследствие отсутствия или прекращения процесса, а вследствие протекания его в 2х противопол. направлениях с равными скоростями.
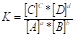
-з-н действ. масс для обратимой хим. р-ции.
Похожие статьи
-
Слабые (L<<1, L<<100%) нек. мин. к-ты HNO2, H3PO4, HJ NH3, все ост. органич. основания (Me(OH)2), больш-во органич. кислот НСООН, СН3СООН,...
-
Соли-сильные электролиты, существующие в водных растворах в виде положительно запряженных ионов металлов и отрицательно заряженных ионов кислотных...
-
Если на равновесную с-му не оказ-ся вноешнего воздействия (не изм. темп, давл.), то равновесие м/существовать неизменным долго. Любое внешнее возд-ие...
-
Гомогенный и гетерогенный катализ. Механизм действия катализатора - Основы химии
При гомогенном катализе катализатор и реагирующие вещества образуют одну фазу (газовая смесь или раствор). При гетерогенном катализе катализатор и...
-
ОВР, протекающие с изменением ст. окисления эл-тов, вхлдящие в состав реакц. ве-в. они сопровожд-ся переход электронов одним за другим. Zn-2e =Zn2+...
-
Р-ры-галог. с-мы, сост. из 2х или более компонентов(расв-ль и растворимые ве-ва). Растворитель-тот компонент, кот. в чистом виде нах-ся в том же...
-
ХИМИЧЕСКАЯ КИНЕТИКА И ХИМИЧЕСКОЕ РАВНОВЕСИЕ - Неограническая химия
Задание 4.1: 4.1.1. Проанализируйте данную Вам реакцию (табл. IV.1) и укажите, какой она является: гомогенной или гетерогенной. 4.1.2. Запишите...
-
Электролиз - р-ция превращения ве-ва под действ. эл. тока. если к р-ру или расплаву эл-та поднести эл. ток, то ионы в нем начнут направленно перемещаться...
-
Опис-ся правиломВант-Гоффа: С увелич-ем темп. на каждые 10 градусов. Скор. больш-ва хим. р-ций увелич-ся в 2-4 раза. Где г-темп. коэф-т скорости хим....
-
При взаимодействии атомао м/у ними может возникнуть хим. связь, приводящая к образованию устойчивой многоатомной с-мы - молекулы, кристалла. Чем прочнее...
-
Гидролиз - р-ция обменного взаимод-я ионов связи, с ионами, входящими в состав Н2О (Н+ и ОН-). Г-з протекает в том случае, если хотя бы один из ионов...
-
Химическим равновесием называется такое состояние химической системы, при котором количества исходных веществ и продуктов не меняются со временем. 1....
-
Св-ва хим. эл-тов, а так же формы и св-ва соединений эл-тов нах-ся в периодической зависимости от заряда ядер их атомов. Возрастание + зарядов атомных...
-
Атом сост. из массивн. "+" заряж. ядра и нах-ся в его поле "-"электронов. В ядрах нах-ся практич. вся масса атома. В состав ядра входят элемент. частицы:...
-
Комплексные соединения - соед-я, обр-ся сочетанием нескольких, способных к существованию ионов, сост. из атома в опр. валентном сост-ии, связ. с одной...
-
Атомно-молекулярное учение. Основные понятия химии - Основные понятия неорганической химии
Все вещества сост. из атомов. В химию понятие атома ввел Ломоносов: ат. разные, ат. каждого вида один. М/у собой, но отлич. от атомов др. вида., ат....
-
Масса всех веществ, вступивших в химическую реакцию, равна массе всех продуктов реакции. Атомно-молекулярное учение этот закон объясняет следующим...
-
Или N экв.1=n экв.2 для газообразных ве-в наряду с понятием молярного V (22,4 моль/л), исп-ся понятие - молярный объем эквивалента-это V одного моль...
-
Катализ - Концепции современного естествознания: химическая составляющая
Наиболее сильное влияние на скорость реакции оказывает присутствие в реагирующей системе Катализатора -- вещества, которое повышает (а иногда и уменьшает...
-
Растворы - термодинамические устойчивые системы переменного состава, состоят не менее чем из двух компонентов и продуктов их взаимодействия. Это...
-
Реакторами идеального (полного) смешения называются реакторы непрерывного действия, в которых осуществляется турбулентный гидродинамический режим. В них...
-
Смещение химического равновесия. Принцип Ле-Шателье - Основы химии
Положение химического равновесия зависит от следующих параметров реакции: температуры, давления и концентрации. Влияние, которое оказывают эти факторы на...
-
Закон постоянства состава - Основные понятия и законы химии
Впервые сформулировал Ж. Пруст (1808 г). Все индивидуальные химические вещества имеют постоянный качественный и количественный состав и определенное...
-
Составление химических уравнений, Расчеты по химическим уравнениям - Основные понятия и законы химии
Включает три этапа: 1. Запись формул веществ, вступивших в реакцию (слева) и продуктов реакции (справа), соединив их по смыслу знаками "+" и "®" : HgO ®...
-
Уравнение Клайперона-Менделеева - Основные понятия и законы химии
Если записать объединенный газовый закон для любой массы любого газа, то получается уравнение Клайперона-Менделеева: PV= (m / M) RT Где m - масса газа; M...
-
Закон Авогадро ди Кваренья (1811 г.) - Основные понятия и законы химии
В равных объемах различных газов при одинаковых условиях (температура, давление и т. д.) содержится одинаковое число молекул. Закон справедлив только для...
-
ОСНОВНЫЕ ПОНЯТИЯ И ЗАКОНЫ ХИМИИ, Атомно-молекулярное учение - Основные понятия и законы химии
Химия - наука о веществах, закономерностях их превращений (физических и химических свойствах) и применении. В настоящее время известно более 100 тыс....
-
Энергия Гельмгольца Изохорно-изотермический потенциал F = U - TS Величина ( V - TS ) является свойством системы; она называется энергией Гельмгольца....
-
В термодинамике понятие "энтропия" было введено Р. Клаузиусом (1865), который показал, что процесс превращения теплоты в работу следует общей физической...
-
Пусть { , , ..., } - множество возможных состояний некоторой физической системы. В любой момент времени система может находиться только в одном...
-
Цель и задачи исследования операций Исследование операций - научная дисциплина, занимающаяся разработкой и практическим применением методов наиболее...
-
Основные понятия и определения проблемы прогнозирования - Прогнозирующие системы
Необходимо отметить, что мы рассматриваем прогнозирование в целях планирования производства или управления запасами. Таким образом, наш интерес лежит в...
-
Первым практическим поводом к осознанию необходимости изучения химической эволюции явились исследования в области моделирования биокатализаторов....
-
Основные понятия теории экономико-математического моделирования Кибернетический подход к исследованию экономико-математических систем Обычно...
-
Основные понятия и обозначения Динамическое программирование как самостоятельная дисциплина сформировалась в пятидесятых годах двадцатого века. Большой...
-
Скорость реакции определяется изменением молярной концентрации одного из реагирующих веществ: V=dC/dtV. Факторы, влияющие на скорость химических...
-
Чтобы осуществлялось химическое взаимодействие веществ А и В, их молекулы (частицы) должны столкнуться. Чем больше столкновений, тем быстрее протекает...
-
Модель в общем смысле (обобщенная модель) есть создаваемый с целью получения и (или) хранения информации специфический объект (в форме мысленного образа,...
-
ВИДНЫЕ ДЕЯТЕЛИ ХИМИИ О КАТАЛИЗЕ - Процесс катализа
И. Берцелиус (1837): "Известные вещества оказывают при соприкосновении с другими веществами такое влияние на последние, что возникает химическое...
-
Химическая связь - это взаимное сцепление атомов в молекуле и кристаллической решетке в результате действия между атомами электрических сил притяжения....
Катализ. Виды к. механизм действия К, Хим. равновесие: понятие, динамич. хар-р, конст. хим. равновесия - Основные понятия неорганической химии