Cлабые электролиты. Равновесие в р-ре слаб. электролита. степень и конст. дисс. з-н разведения Оствальда, Сильные электролиты. Понятие об активности и коэф-те активности. Ионная сила раствора - Основные понятия неорганической химии
Слабые (L<<1, L<<100%) нек. мин. к-ты HNO2, H3PO4, HJ NH3, все ост. органич. основания (Me(OH)2), больш-во органич. кислот НСООН, СН3СООН, С6Н5СООН. Процесс обратимый.
НСООН-Н++НСОО-
СН3СООН-Н++СН3СОО-
H2S-H++HS-
Т. е в р-ре слаб. эл-та уст-ся равновесие м/у ионами и продисс. Молекулами, кот. опис-ся соотв. конст. равновесия:
Для НСООН-Н++НСОО-
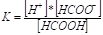
-конст. диссоц. слабого электролита.
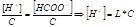
М/у L и К сущ-т связь, выраж-я з-ном разведения Оствальда: обозн. общим НСООН в р-ре С [моль/л], L-ст. дисоц., тогда в соотв. с определением степени диссоц. = равновесн. С ионов составят:[HCOO-]=L*C
А С недессоц. молекул будет = [HCOOH]=Cобщ.-L*Cдиссоц.=С(1-L)
Подставим эти С в выр-я для К:
Сильные электролиты. Понятие об активности и коэф-те активности. Ионная сила раствора
Сильные электролиты - L>1 (L>100%), где L-ст. диссоциации. Это почти все соли, некот. кислоты, некот. основания. HCl, HBr, HJ, H2SO4, НClO4,ROH(Li, Na, K,Cs, Rb); R(OH)2 (Ca, Ba, Ra), соли растворимые.
Процесс дис. запис-ся как необратимый:
HCl>Н++Сl-
H2SO4>2H++SO42-
Активность-та концентрация илнов или ве-ва, кот. проявляется в действии. м/у активностью и концентр. сущ-т взаимосвязь: a=c*f, где f-коэф-т активности, с-молярная концентрация.
Для расчета f теории сильных электролитов исп-ся выражение: , где - ионная сила р-ра, z-заряд иона.
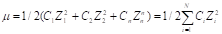
Т. о. коэф-т активности ионов в р-ре не зависит от его природы, а опр-ся только величиной его заряда и общим содержанием ионов в р-ре.
Похожие статьи
-
СИЛЬНЫЕ ЭЛЕКТРОЛИТЫ - Характеристика основных видов растворов
В водных растворах сильные электролиты полностью диссоциированы, поэтому даже при малых концентрациях растворов энергия электростатического...
-
К-изменение скорости хим. р-ции, под действием особых ве-в-катализаторов, кот. участвуют в ходе р-ции, но к концу ее остаются в неизменном кол-ве. Виды:...
-
СЛАБЫЕ ЭЛЕКТРОЛИТЫ - Характеристика основных видов растворов
При растворении в воде слабого электролита устанавливается динамическое равновесие между недиссоциированными молекулами и продуктами их диссоциации -...
-
ГИДРОЛИЗ СОЛЕЙ - Характеристика основных видов растворов
Гидролизом называется обменная реакция между веществом и водой. При гидролизе обычно происходит изменение реакции среды. Если гидролиз не сопровождается...
-
1.1. Освоить методику определения тепловых эффектов процессов. 1.2. Определить тепловой эффект при нейтрализации кислоты щелочью. 1.3. Вычислить тепловой...
-
Соли-сильные электролиты, существующие в водных растворах в виде положительно запряженных ионов металлов и отрицательно заряженных ионов кислотных...
-
При взаимодействии атомао м/у ними может возникнуть хим. связь, приводящая к образованию устойчивой многоатомной с-мы - молекулы, кристалла. Чем прочнее...
-
Комплексные соединения - соед-я, обр-ся сочетанием нескольких, способных к существованию ионов, сост. из атома в опр. валентном сост-ии, связ. с одной...
-
Электролиз - р-ция превращения ве-ва под действ. эл. тока. если к р-ру или расплаву эл-та поднести эл. ток, то ионы в нем начнут направленно перемещаться...
-
ДИСПЕРСНЫЕ СИСТЕМЫ - Неограническая химия
Задание 5.1. В определенном объеме раствора V л содержится m г вещества. Плотность раствора с (табл. V.1). Рассчитайте: 5.1.1. Процентную концентрацию...
-
ОВР, протекающие с изменением ст. окисления эл-тов, вхлдящие в состав реакц. ве-в. они сопровожд-ся переход электронов одним за другим. Zn-2e =Zn2+...
-
Гидролиз - р-ция обменного взаимод-я ионов связи, с ионами, входящими в состав Н2О (Н+ и ОН-). Г-з протекает в том случае, если хотя бы один из ионов...
-
Если на равновесную с-му не оказ-ся вноешнего воздействия (не изм. темп, давл.), то равновесие м/существовать неизменным долго. Любое внешнее возд-ие...
-
Или N экв.1=n экв.2 для газообразных ве-в наряду с понятием молярного V (22,4 моль/л), исп-ся понятие - молярный объем эквивалента-это V одного моль...
-
Опис-ся правиломВант-Гоффа: С увелич-ем темп. на каждые 10 градусов. Скор. больш-ва хим. р-ций увелич-ся в 2-4 раза. Где г-темп. коэф-т скорости хим....
-
ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ - Характеристика основных видов растворов
Все вещества по способности в растворе или в расплавленном состоянии проводить электрический ток можно подразделить на две группы: электролиты и...
-
Атом сост. из массивн. "+" заряж. ядра и нах-ся в его поле "-"электронов. В ядрах нах-ся практич. вся масса атома. В состав ядра входят элемент. частицы:...
-
Обзор литературы - Синтез пара-нитродифенила. Теоретические основы нитрования
Нитрование - введение нитрогруппы - NO2 в молекулы органических соединений. Может проходить по электрофильному, нуклеофильному и радикальному механизмам;...
-
Существует три основных типа окислительно-восстановительных реакций: 1. Если окислитель и восстановитель находятся в молекулах различных веществ, то...
-
Гидролиз солей в водном растворе - Реакция обмена между растворами электролитов
Цель работы. Исследовать характер гидролиза солей. Приборы и реактивы . Штатив с пробирками, растворы карбоната натрия, сульфата меди, хлорида аммония...
-
ХИМИЧЕСКАЯ КИНЕТИКА И ХИМИЧЕСКОЕ РАВНОВЕСИЕ - Неограническая химия
Задание 4.1: 4.1.1. Проанализируйте данную Вам реакцию (табл. IV.1) и укажите, какой она является: гомогенной или гетерогенной. 4.1.2. Запишите...
-
Растворимость солей, кислот и оснований в воде, Ионное произведение воды - Ионные реакции
Таблица. Таблица растворимости солей, кислот и оснований в воде Катион Анион H+ NH4+ K+ Na+ Ag+ Ba2+ Ca2+ Mg2+ Zn2+ Cu2+ Hg2+ Pb2+ Fe2+ Fe3+ Al3+ OH- P P...
-
ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ (рН) - Характеристика основных видов растворов
Вода - очень слабый электролит, поэтому в незначительной степени диссоциирует на ионы: H2O H+ + OH-. Константа диссоциации воды равна: Kд. = [H+][OH-] /...
-
Р-ры-галог. с-мы, сост. из 2х или более компонентов(расв-ль и растворимые ве-ва). Растворитель-тот компонент, кот. в чистом виде нах-ся в том же...
-
ПРОИЗВЕДЕНИЕ РАСТВОРИМОСТИ - Характеристика основных видов растворов
В насыщенном растворе малорастворимого сильного электролита устанав-ливается равновесие между твердой фазой (осадком) и ионами электролита: ВaSO4 (в...
-
Основные положения стереохимии Стереохимия Стереохимия или структурная химия(от греч. уфесеьт -- твердый, пространственный), -- раздел химии о...
-
АБСОРБЦИЯ ТРИОКСИДА СЕРЫ. - Получение серной кислоты
Последней стадией процесса производства серной кислоты контактным способом является абсорбция триоксида серы из газовой смеси и превращение его в серную...
-
Электролиз - физико-химический процесс, состоящий в выделении на Электродах составных частей растворенных веществ или других веществ, который возникает...
-
Диссоциация воды. Водородный показатель. Гидролиз солей - Основы химии
Чистая вода, хоть и плохо (по сравнению с растворами электролитов), но может проводить электрический ток. Это вызвано способностью молекулы воды...
-
Атомно-молекулярное учение. Основные понятия химии - Основные понятия неорганической химии
Все вещества сост. из атомов. В химию понятие атома ввел Ломоносов: ат. разные, ат. каждого вида один. М/у собой, но отлич. от атомов др. вида., ат....
-
Растворы электролитов. Диссоциация кислот, солей и оснований - Основы химии
Электролиты - вещества, которые при растворении подвергаются диссоциации на ионы. В результате раствор приобретает способность проводить электрический...
-
Химическим равновесием называется такое состояние химической системы, при котором количества исходных веществ и продуктов не меняются со временем. 1....
-
Скорость реакции определяется изменением молярной концентрации одного из реагирующих веществ: V=dC/dtV. Факторы, влияющие на скорость химических...
-
Химическая связь - это взаимное сцепление атомов в молекуле и кристаллической решетке в результате действия между атомами электрических сил притяжения....
-
Важнейшей характеристикой раствора является его состав. Содержание растворенного вещества в растворе может быть выражено безразмерными единицами (долями...
-
Ионная полимеризация, Катионная полимеризация - Синтетический каучук
Если в радикальной полимеризации активным центром является радикал, то в ионной - ионы. Полимеризация, при которой ее активный центр - заряд иона -...
-
Основные понятия теории экономико-математического моделирования Кибернетический подход к исследованию экономико-математических систем Обычно...
-
Процесс нитрования углеводородов смесью азотной и серной кислот протекает в гетерогенной среде, так как образуются две фазы - органическая...
-
Пластичными массами называют материалы, полученные на основе полимеров, содержащие различные добавки и способные под влиянием температуры и давления,...
-
ВИДЫ РАСТВОРОВ. РАСТВОРИМОСТЬ. ПРОЦЕСС РАСТВОРЕНИЯ - Характеристика основных видов растворов
Растворы - гомогенные системы, состоящие из двух или более компонентов (растворителя, растворенного вещества и продуктов их взаимодействия), состав...
Cлабые электролиты. Равновесие в р-ре слаб. электролита. степень и конст. дисс. з-н разведения Оствальда, Сильные электролиты. Понятие об активности и коэф-те активности. Ионная сила раствора - Основные понятия неорганической химии