Дія різних видів амілаз - Будова і властивості ферментів
Ферменти мають дуже високою специфічністю. Ця специфічність обумовлена особливою формою молекули ферменту, точно відповідній формі молекули субстрату. Цю гіпотезу називають гіпотезою "ключа і замка": субстрат порівнюється в ній з ключем, який точно підходить до замку, тобто до ферменту. Далі на підставі цієї гіпотези вже в 1959 році нову інтерпретацію гіпотези "ключа і замка" запропонував Кошланд. Він робить висновок про гнучкість активних центрів ферментів. Згідно з цим припущенням, субстрат з'єднуючись з ферментом, викликає зміни в структурі останнього. Підходящої аналогією в цьому випадку може служити рукавичка, яка при надяганні на руку відповідним чином змінює свою форму. А-Амілази різного походження мають багато спільних властивостей: добре розчиняються у воді або в сильно розбавлених розчинах солей. Більш концентровані розчини солей (наприклад... 20-30% - ні розчини сульфату амонію) викликають осадження цих ферментів. Амілаза легко розчиняються у розведених розчинах етилового спирту, але осідають при його концентрації в середовищі понад 60%. Білок амілаз володіє слабокислими властивостями; ізоелектрична точка ферментів коливається в межах рН 4,2 - 5,7. Іони кальцію надають стабілізуючу дію на амілазу. Це вперше було виявлено Воллерштейном, потім підтверджено Накамурою. В даний час це явище відзначено майже для всіх амілаз.
Гідроліз крохмалю амілазами. Амілаза діє на -1,4-глікозидні зв'язку, розщеплюють амілозу всередині її ланцюга, в результаті чого з великою швидкістю утворюються низькомолекулярні продукти гідролізу - нормальні декстрини. Їх подальший гідроліз дає мальтозу, мальтотріозу і глюкозу. Було знайдено, що розщеплення -1,4-глюкозидним зв'язків у амілоза носить випадковий характер і підпорядковується законом статистичного розподілу продуктів реакції. Розщеплення дрібніших фракцій на останньому етапі амілоза носить вже не випадковий характер - дія ферменту спрямовано лише на певні -1,4-Глікозидні зв'язку. У кінцевому рахунку амілаза перетворюють амілозу в мальтозу і глюкозу, хоча й відзначені деякі несуттєві відмінності в динаміці гідролізу цими ферментами зазначеного субстрату.
Субстратами для дії амілаз є крохмаль, що складається з амілози і амілопектину, продукти часткового гідролізу крохмалю і глікоген. Крохмаль - рослинний полісахарид з дуже складною будовою. Цей двокомпонентний з'єднання, що складається з 13-30% амілози і 70-85% амілопектину. Обидва компоненти неоднорідні, їх молекулярна маса (М. м.) коливається в широких межах і залежить від природи крохмалю. Амілоза - це необертающийся полімер, в якому залишки глюкози Сполучених б-1,4-Глікозидний зв'язком; ступінь полімеризації близько 2000. У "аномальних" амілози з однією-двома б-1,6-зв'язками полімеризація може зрости до 6000. Амілоза практично не має відновлюючої здатності, тому що в кожній молекулі амілози є тільки один вільна альдегідна група.
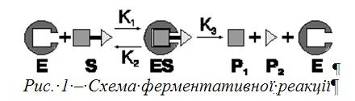
Реакції, що каталізуються амілазами, мають дві стадії: коротку передстаціонарну і тривалу - стаціонарну. Під час першої стадії ендоамілаза швидко зменшує молекулярну масу субстрату, утворюючи суміш лінійних та розгалужених олігосахаридів. Другий етап реакції триває, поки продукти гідролізу не перестануть забарвлюватися йодом; він протікає значно повільніше і залежить від індивідуальних властивостей ферменту та його природи.
Б-амілаза (1,4-б-D-глюканглюканогідролаза) є ендоамілазою, що викликає гідролітичні розщеплення б-1,4-глікозидних зв'язків всередині полімерного субстрату. Це водорозчинний білок, що має властивості глобуліну і має молекулярну масу 45-60 кДа. Всі б-амілази відносяться до металоензимів, вміст у них Са коливається від 1 до 30 г-атом / 1 г-моль ферменту. Повне видалення Са приводить до інактивації ферменту. Глутамінова і аспарагінова кислоти становлять 25 мас. % Від маси білка. Залежно від виду мікроорганізму властивості б-амілаз можуть сильно відрізнятися не тільки за механізмом дії на субстрат і по кінцевим продуктам, але і за оптимальними умовами для прояву максимальної активності. Присутність в промислових препаратах протеїназ знижує каталітичну активність б-амілази. У результаті впливу б-амілази на перших стадіях в гідролізаті накопичуються декстрини, потім з'являються тетра - і тримальтоза, що не зафарбовуються йодом і які дуже повільно гідролізуються б-амілазою до ди - і моносахаридів.
В-амілаза (в -1,4-глюкан мальтогідролаза) - активний білок, що володіє влатсивостями альбуміну. Каталітичний центр ферменту має сульфгідрильні і карбоксильні групи і імідозольний цикл залишків гістидину. в-Амілаза - екзофермент кінцевої дії, що виявляє спорідненість до передостаннього в -1,4-зв'язку з нередукуючого кінця лінійного ділянки амілози і амілопектину.
На відміну від б-амілази в-амілаза практично не гідролізує нативний крохмаль, тоді як клейстеризований крохмаль гідролізуєтся нею з утворенням мальтози в-конфігурації. Якщо гідролізу піддається амілоза, то гідроліз йде повністю до мальтози. Незначна кількість декстринів може здіснюватися при гідролізі "аномальної" амілози, тому що гідроліз в-амілазою йде тільки по лінійній ланцюга до б -1,6-зв'язків. Якщо субстратом для в-амілази служить амілопектин, то гідроліз йде в значно меншому ступені. в-Амілаза відщеплює фрагмент з нередукуючим кінцем ділянки від зовнішніх лінійних гілок, які мають по 20-26 глюкозних залишків, з утворенням 10-12 молекул мальтози. Гідроліз призупиняється на передостанній б -1,4-зв'язку, що межує з б -1,6-зв'язком. У гідролізатінакопичується 54-58% мальтози, решту становлять високомолекулярні декстрини, що містять значну кількість б -1 ,6-зв'язків - так звані в - декстрини.
В-амілази виявляють більшу стабільність у відсутність іонів Са2+. Молекулярна маса в-амілази рослин досить висока, вона складає від 50000 до 200000. Фермент може складатися з однієї або чотирьох субодиниць до 50 000 кожна. Фермент містить SH-групи та чутливий до дії важких металів. Вважається, що (в-амілазу має високу здатність до нескінченої атаки субстрату. Для амілози середньої молекулярні маси в одному при з'єднанні ферменту до субстрату можливо відчеплення до чотирьох залишків мальтози. При збільшенні молекулярної маси субстрату можлива і більша кількість місць атаки.
Продукт реакції - мальтоза - має в-конфігурацію. Гідроліз іде по лінійному ланцюзі тільки до б-1,6-зв'язків. При гідролізі крохмалю утворюється 54-58% мальтози і 42-46% високомолекулярних декстринів (в-декстринів). в-амілази виявляють більшу стабільність у відсутність іонів Са. Фермент може складатися з однієї або чотирьох субодиниць, містить SH-групи та чутливий до дії важких металів. Властивості в-амілаз залежать від джерел їх виділення. Для отримання мальтози з крохмалю використовують бактеріальні в-амілази.
Глюкоамілаза (1,4-б-D-глюканглюкогідролаза) широко розповсюджена в природі. Вона синтезується багатьма мікроорганізмами і утворюється в тканинах тварин. У літературі фермент відомий під різними назвами: амілоглюкозідаза, г-амілаза, лізосомальних б-глюкозидази, кисла мальтаза, матулаза, екзо-б-1 ,4-глюкозидази. Глюкоамілаза каталізує послідовне відщеплення кінцевих залишків б-D-глюкози з нередуцірующіх решт субстрату. Цей фермент проявляє екзогенний механізм впливу на субстрат. Багато глюкоамілази володіють також здатністю гідролізувати б-1 ,6-глюкозідние зв'язку. Однак це відбувається в тому випадку, коли за б-1 ,6-зв'язком слід б-1 ,4-зв'язок, тому декстран ними не гідролізується. Глюкоамілаза значно швидше гідролізують полімерний субстрат, ніж оліго-і дисахариди. Майже всі глюкоамілази є глікопротеїдів, що містять від 5 до 35% вуглеводів, які складаються з оліго-, ди - і моносахаридів.
Майже всі глюкоамілази є глікопротеїдів, що містять від 5 до 35% вуглеводів, які складаються з оліго-, ди-і моносахаридів. Угле водний компонент може бути цілісним фрагментом або ж розбитими на індивідуальні сполуки, які прикріплюються до білка через треонін і серин. Наприклад, у глюкоамілази A. niger їх 20. Більшість відомих глюкоамілаз має оптимум при рН 4,5-5,2, рідше - при 5,7-6,0, в основному для дріжджових глюкоамілаз.
Фермент пуллуланаза (пуллулан-6-глюканогідролаза) раніше був відомий під назвами: R-фермент, гранична декстриназа або амілопектин-6-глюканогідролаза. Пуллуланаза, як і б-амілаза, є ендогенних ферментом, але на відміну від неї здатна невпорядковано гідролізувати б-1 ,6-зв'язку в пуллулані, амілопектину, глікогену та граничних декстрину, одержуваних при спільному впливі на крохмаль і глікоген б-і в - амілаз. Якщо між двома б-1 ,6-зв'язками розташовано більше трьох залишків глюкози, то розрив б-1 ,6-зв'язку йде значно повільніше, тому амілопектин гідролізується пуллуланазой гірше за інших розгалужених полісахаридів. Найбільш частим відщеплює фрагментом є мальтотріоза. Пуллуланази з різних джерел мають різні властивості. Ізоамілаза (глікоген-6-глюканогідролаза), або дебранчінг-фермент, гідроліз б-1 ,6-зв'язку в розгалужених полісахаридів, таких як амілопектин, глікоген, в-граничні декстрини. Відмінною особливістю ізоамілази в порівнянні з пуллуланазой є те, що вона не здатна гідролізувати пуллулан і слабко діє на граничні в-декстрини. Бактеріальна ізоамілаза розщеплює б-1 ,6-зв'язку в глікогенній повністю, а пуллуланаза діє на цей субстрат слабо. Ізоамілазу утворюють багато мікроорганізмів, такі як B. amyloliquefacie, Cytophaga, Streptomyces, Pseudomonas amyloderamosa, Saccharomyces cerevisiae та ін, ферменти яких мають здатність гідролізувати субстрат при рН від 3,5 до 6,5 і температурах від 25 до 53 ° С. Ізоамілаза не стабілізується кальцієм, за винятком ферменту з Cytophaga. Молекулярна маса ізоамілаз коливається від 90 до 120 кДа.
Б-глюкозидази (б-D-глюкозідглюкогідролаза) має здатність гідролізувати б-1 ,4-зв'язку від нередуцірующего кінця субстрату з відщеплення залишку глюкози. Фермент проявляє найбільшу спорідненість до низькомолекулярним субстрату, легко гідролізують мальтозу, олігосахариди, а полісахариди гідролізують повільно або зовсім не гідролізують. б-глюкозидази об'єднує групу ферментів і має ряд інших назв: мальтаза, глюкоінвертаза, глюкозідосахараза. Властивості ферментів, які продукуються різними мікроорганізмами, можуть значно відрізнятися. Фермент має здатність до перенесення б-D-глюкозільних залишків на відповідні акцептори, часто з утворенням б-1 ,6-зв'язків[5].
Декстраназа (1,6-б-D-глюкан-6-глюканогідролаза) каталізує розщеплення б-1 ,6-зв'язків у бактеріальному полісахариди декстрану. Серед продуцентів декcтраназ слід зазначити B. subtilis, B. megaterium, Lactobacillus befidus, Streptococcus mutans, Bravibacterium fuscum, Pseudomonas UQM-733, різні грунтові бактерії, а також численні види мікроскопічних грибів роду Penicilium, Aspergillus і Fusarium. Декстранази мають молекулярну масу від 35 до 71 кДа; вони є слабокислими білками. Ізоелектричної точка для всіх грибних декстраназ лежить в діапазоні від 4,0 до 4,6. Для більшості бактеріальних декстраназ оптимальна температура каталітичної дії 35-37 ° С; для грибних продуцентів температура трохи вище - 55-60 ° С. Оптимальне значення рН коливається в залежності від виду продуцента від 4,4 до 7,5. За допомогою ендодекстраназ можна отримувати з декстрану кровозамінники необхідної молекулярної маси; їх також використовують у стоматології для зняття зубних бляшок, що складаються з декстраноподобних глюканов.
Амілаза B. Macerans [1,4-б-D-глюкан-4-б-(1,4-б-глюкану) трансфераза (ціклізуюча)] Ця унікальна амілаза, яка вперше була знайдена в культурі B. macerans. Вона циклізує частину ланцюга 1,4-б-глюкану шляхом утворення 1,4-б-глюкозідной зв'язку. Робоча назва цього ферменту - циклодекстринглюканотрансфераза. При дії на крохмаль і аналогічні субстрати утворюються циклічні нередукуючі декстрини різних розмірів.
Фермент діє на лінійні полісахариди, гідролізуючи насамперед б-1 ,4-зв'язок, і потім переносить звільнився редукуючий кінець ланцюга на НРК. Фермент також здатний перебудовувати лінійну структуру мальтодекстрин без циклізації, може переносити залишки глюкози і мальтози на олігосахариди, тобто має за певних умов трансферазну активність і здатний ввести реакцію конденсації.
Похожие статьи
-
Амілаза її види та будова - Будова і властивості ферментів
Амілази (грец. бmylon -- крохмаль) -- ферменти класу гідролаз, які забезпечують гідроліз б-1,4-глікозидних зв'язків у молекулах полісахаридів --...
-
Специфічність дії ферментів, Класифікація і номенклатура ферментів - Будова і властивості ферментів
Кожен ензим діє на певний субстрат або групу речовин, які подібні за своєю структурою. Специфічність дії ферментів пояснюється схожістю конфігурації...
-
Способи вираження активності ферментів - Будова і властивості ферментів
У біологічних об'єктах ферменти знаходяться в дуже мізерних концентраціях, тому для оцінки ферментативних процесів визначають не вміст ферментів, що...
-
Залежність швидкості ферментативної реакції від температури - Будова і властивості ферментів
Підвищення температури завжди збільшує швидкість хімічних реакцій, зокрема ферментативних. Як показник зростання швидкості реакції використовують...
-
Механізм дії ферментів - Будова і властивості ферментів
З'ясування механізмів, що лежать в основі каталітичного дії ензимів, є однією з фундаментальних завдань і актуальних проблем не тільки ензимології, а й...
-
Літературний огляд, Будова ферментів - Будова і властивості ферментів
Будова ферментів За хімічною природою ферменти - це білки, що проявляють каталітичні властивості, тобто вони прискорюють перебіг різних хімічних...
-
Вступ - Будова і властивості ферментів
Обмін речовин в організмі живої істоти можна визначити як сукупність всіх хімічних перетворень, яким піддаються сполуки, що надходять ззовні. Ці...
-
Іммобілізовані ферменти та їх застосування - Будова і властивості ферментів
Ферменти виявляють свою активність не тільки в мікропросторі клітини, але й поза організмом. Вони є виключно активними і специфічними каталізаторами,...
-
Форма тіла пінгвінів обтічна, що ідеально для пересування у воді. Мускулатура і пристрій кісток дозволяють їм під водою працювати крилами майже як...
-
Энзимотерапия - Использование ферментов в медицинской практике в качестве лекарственных средств
Энзимотерапия - это использование ферментов в качестве лекарственных средств. Использование ферментов в качестве терапевтических средств имеет много...
-
В каждом организме (животном, растительном или микробной клетке) все время происходят сложные процессы превращения веществ. Велика роль в этих процессах...
-
Наукові здобутки у вивчені проблеми критичних періодів та поступове впровадження їх в життя батьками, соціальними інституціями сприяють оптимізації...
-
Переносимость и побочные эффекты - Ферменты в гастроэнтерологии
Побочные эффекты при применении ферментных препаратов встречаются крайне редко (менее 1%) и носят чаще всего дозазависимый характер. В моче больных,...
-
Состав ферментных препаратов - Ферменты в гастроэнтерологии
При нарушении пищеварения применяются различные лекарственные средства, содержащие ферменты. В зависимости от состава ферментные препараты можно...
-
Энзимодиагностика - Использование ферментов в медицинской практике в качестве лекарственных средств
Энзимодиагностика заключается в постановке диагноза заболевания (или синдрома) на основе определения активности ферментов в биологических жидкостях...
-
1. Самыми распространенными ферментативными препаратами являются комплексы ферментов желудочно-кишечного тракта (Фестал, Панзинорм форте, Мезим форте,...
-
Роль витаминов в построении ферментов
Витамины - это низкомолекулярные органические вещества самого разнообразного строения, которые не синтезируются в организме, но являются жизненно...
-
ЗАГАЛЬНА ХАРАКТЕРИСТИКА РОБОТИ Актуальність теми. Більшість відомих на сьогодні антибіотиків, які успішно використовуються в медицині, ветеринарії і...
-
Клинические особенности применения - Ферменты в гастроэнтерологии
Одним из важных факторов, определяющих успех лечения, является правильный выбор ферментного препарата, его дозы и продолжительности лечения. При выборе...
-
Соматологічні особливості тілобудови спортсменів різних спеціалізацій
Вступ Соматологічні особливості тілобудови спортсменів в більшості випадків є базовими для досягнення високого спортивного результату. При цьому тотальні...
-
Клінічні симптоми отруєння тварин різних видів - Токсикологія сполук ртуті
Ртуть пестициди лабораторія Отруєння ртуттю в теперішній час зустрічається, як правило в хронічній формі. Однак можливі і гострі інтоксикації препаратами...
-
Серед різних з'єднань ртуті найбільшу популярність одержали наступні з'єднання. Двохлориста ртуть (Hg CI 2), або сулема . В чистому вигляді являє собою...
-
Україна за підсумком 2014 року експортувала 27 млн ??тонн зернових вантажів. Експорт цих вантажів відбувається через морські порти (95%), з...
-
Антидіабетичні властивості лікарських рослин, поширених на території України
Вступ На сьогоднішній день у світі нараховується понад 170 млн хворих на цукровий діабет (ЦД); більше того, передбачається, що у 2025 р. показник...
-
Краткая фармакологическая характеристика - Ферменты в гастроэнтерологии
Ацидин-пепсин - препарат, содержащий протеолитический фермент. Получают из слизистой оболочки желудка свиней. Таблетки по 0,5 и 0,25 г содержат 1 часть...
-
В зависимости от химической природы ферменты делятся на простые и сложные [11]: Простые ферменты состоят только из аминокислот - например, пепсин,...
-
ФЕРМЕНТНЫЕ ПРЕПАРАТЫ В ГАСТРОЭНТЕРОЛОГИИ - Ферменты в гастроэнтерологии
Ферментные препараты - это группа фармакологических средств, способствующих улучшению процесса пищеварения. Нарушения процесса пищеварения различной...
-
Ферменты, или энзимы (от лат. fermentum, греч. жэмз, ?нжхмпн -- закваска) -- обычно белковые молекулы или молекулы РНК (рибозимы) или их комплексы,...
-
Ферменты рестриктазы - Великие открытия в генетике ХХ века
Прорыва, приведшего ко всем предыдущим открытиям, могло и не случиться, если бы не бактериальный вирус, следующее открытие было также сделано благодаря...
-
Ферменты (от латинского слова fermentum - закваска) - белки, которые обладают каталитической активностью и характеризуются очень высокой специфичностью и...
-
Глутатіон редуктаза (GR, NADPH-залежна глутатіон оксидоредуктаза; ЕС 1.6.4.2.) - фермент, який відновлює глутатіон за рахунок окиснення NADPH. GSSG + 2...
-
Розвиток різних типів зародкового мішка Зародковим мішком чи жіночим гаметофітом, називають статеве покоління покритонасінних рослин. Зародковий мішок...
-
Свойства ферментов - Питательные вещества
Важнейшим свойством ферментов является преимущественное одной из нескольких теоретически возможных реакций. В зависимости от условий ферменты способны...
-
Фермент витамин гормон здоровье Нормальное существование человеческого организма и здоровья в целом зависит от многих фактором, немаловажным из которых...
-
Гормоны могут влиять на поведение, воздействуя на сенсорно-перцептивные механизмы, на активность нервной системы и на эффекторные механизмы, необходимые...
-
Ферменты участвуют в процессе пищеварения, помогая организму перерабатывать пищу. Они нормализуют обмен веществ, способствуя снижению веса. Укрепляют...
-
Ферменты используют различные вещества для создания нашего организма. Но они могут не только созидать, но и разрушать уже построенное. Ферменты --...
-
Гриби розмножуються безстатевим і статевим способами. Безстатеве розмноження відбувається частинами міцелію або окремими клітинами, які дають початок...
-
Властивості води, Чудесні зцілення водою - Водойми рідного краю. Їх стан та охорона
Володимир Леліков вважає, що вода, яку ми споживаємо, впливає на емоційний стан людини та здатність її організму до цілісного, ефективного...
-
Дефицит витаминов чаще всего встречается у людей в холодное время года, когда свежие полезные продукты не всегда доступны. Существует два вида недостатка...
Дія різних видів амілаз - Будова і властивості ферментів