Основные понятия химической термодинамики - Химическая термодинамика. Термохимия. Решение задач
Прежде чем приступить к изучению предмета химической термодинамики, необходимо ввести ряд терминов и понятий, используемых в этом разделе.
Изучаемые химической термодинамикой объекты принято объединять понятием системы. Система - это совокупность изучаемых в данной задаче объектов, мысленно или физически отделенных от остального пространства. По своим взаимоотношениям с окружающим миром системы принято подразделять на открытые, закрытые и изолированные.
Открытыми называются системы, способные обмениваться с окружающим пространством, как веществом (иногда используют термин "масса"), так и энергией. Примером такой системы может служить открытый реакционный сосуд (колба, лабораторный стакан, пробирка и т. д.). Его можно охладить или нагреть, можно добавить в него какие-либо вещества или отобрать часть веществ оттуда. В процессе химического превращения определенная часть веществ может самопроизвольно покидать такую систему, например, испаряться.
Закрытыми называются системы, которые могут обмениваться с окружающим пространством только энергией, но не веществом. Примером такой системы может быть закрытый реакционный сосуд (реторта, химический реактор и т. д.). Нагревание, охлаждение, облучение светом такой системы возможно, изменение массы - нет.
Изолированными называются системы, неспособные обмениваться с окружающей средой ни массами, ни энергией. Абсолютно изолированных систем в природе, конечно, не бывает, но условия близкие к ним можно создать, например, в термосе или сосуде Дьюара.
Системы подразделяют также по фазовому составу. Определим сначала само понятие фазы.
Фаза - совокупность всех однородных частей системы, обладающих одинаковым составом и одинаковыми свойствами, отделенная от остальных частей системы поверхностью раздела.
Однофазиую систему называют Гомогенной, Многофазную систему - Гетерогенной. Примером однофазной системы может служить воздух, несмотря на то, что он состоит из нескольких газообразных веществ. Однофазной системой является также водный раствор какого-либо вещества - в нем отсутствуют границы раздела фаз. Вода вместе с плавающим в ней льдом, напротив, является двухфазной системой, хотя обе фазы имеют одну химическую природу. Система останется двухфазной, даже если в воде будет плавать несколько кусочков льда: все они имеют одинаковый состав и свойства.
Приведите самостоятельно примеры различных термодинамических систем.
Любая термодинамическая система характеризуется совокупностью так называемых термодинамических параметров.
Здесь надо пояснить, как описывает термодинамика все происходящие в системе явления. Термодинамические системы состоят обычно из очень большого числа частиц, находящихся к тому же в постоянном тепловом движении.
Описать происходящее в такой системе методами классической механики невозможно даже для самой простой ситуации. Вспомните, что один моль любого вещества состоит из 6,02-1023 молекул. Решить для каждой частицы уравнение движения (уравнения Ньютона), чтобы точно знать координаты и скорости каждой молекулы в любой момент времени, не под силу не только человеку, но и самому мощному компьютеру. Поэтому приходится удовлетвориться описанием системы с помощью тех величин, которые характеризуют ее состояние в целом, дают усредненную картину происходящего. Такой подход к решению задачи называется Статистическим. Величины, описывающие состояние системы в целом, называются Термодинамическими параметрами. Наиболее важными из них являются температура (T°), давление (Р), объем (V), количество вещества (Н), концентрация вещества (С) и т. п.
Вспомните из школьного курса физический смысл этих величин.
Те параметры, значение которых не зависит от количества вещества, называются Интенсивными, а те, значение которых зависит от количества вещества - Экстенсивными. К первому типу относятся, например, температура и давление, ко второму - объем.
Изменение одного из параметров ведет, как правило, к изменению состояния системы и, следовательно, других параметров. Состояние системы аналитически, т. е. в виде математического выражения, можно представить так называемым Уравнением состояния, Связывающим между собой все параметры системы. В общем виде уравнение состояния выглядит следующим образом:
F(p, V,Т, н, ...) = 0
Уравнения состояния позволяют проследить, как меняются параметры системы на всем пути ее перехода из одного состояния в другое. Конкретный вид уравнения состояния известен только для некоторых очень простых систем, например, уравнение Менделеева-Клапейрона, описывающее состояние идеального газа:
PV = (m/M)RT
К сожалению, для большинства реальных систем подобные простые уравнения записать невозможно. Это приводит к необходимости введения понятия Функций состояния. Эти величины также определяются через параметры состояния. Для каждого конкретного случая эти функции будут иметь свой вид, связывая термодинамические параметры в математические выражения. Они могут быть простыми или сложными, в зависимости от свойств данной системы и условий ее существования. Самая важная особенность функций состояния - изменение таких функций не зависит от пути, по которому система перешла из одного состояния в другое, а зависит только от начального и конечного состояний изучаемой системы. В термодинамике известно большое количество величин, обладающих свойствами функций состояния, но ниже будут рассмотрены только самые важные из них.
Фундаментальной функцией состояния является Полная энергия системы Е, которая представляет собой сумму трех составляющих - кинетической энергии ЕКин. движущейся системы, потенциальной энергии ЕПот., связанной с воздействием на систему внешних сил (гравитационных, электростатических или иных) и внутренней энергии системы U:
Е = ЕКин.+ ЕПот.+U (1)
В термодинамике предполагают, что система находится в состоянии относительною покоя, а воздействие внешних сил пренебрежимо мало. Тогда полная энергия системы равна ее внутренней энергии. Точное значение внутренней энергии определить невозможно, потому что она складывается из большого числа различных взаимодействий, природа и величина которых до конца не изучена. Внутреннюю энергию системы определяют кинетическая и потенциальная энергия молекул, энергия взаимодействия атомов в молекулах, энергия взаимодействия электронов и протонов в атомах, из которых состоят молекулы, энергия взаимодействия частиц, составляющих атомное ядро и т. д. К счастью, для решения вопросов термодинамики абсолютное значение внутренней энергии знать не обязательно. Вполне достаточно определить только изменение внутренней энергии ДU, происходящее при переходе системы из одного состояния в другое. Эти изменения происходят в соответствии с законом сохранения энергии, который для термодинамических систем формулируется, как Первое начало Термодинамики:
Q = ДU + A (2)
Сообщенная системе теплота (Q) расходуется на приращение внутренней энергии (ДU) и на совершение системой работы (А) против внешних сил. То есть, общий запас внутренней энергии остается постоянным, если отсутствует тепловой обмен с окружающей средой. В ходе процессов, протекающих в изолированной системе, возможно лишь перераспределение внутренней энергии между отдельными составляющими системы.
Теплота является мерой энергии, передаваемой от одного тела к другому за счет разницы температур этих тел. Эта форма энергии связана с хаотическим столкновением частиц соприкасающихся тел. При столкновениях частиц происходит передача энергии от более нагретого тела к менее нагретому. Переноса вещества при этом не происходит.
Работа является мерой энергии, передаваемой от одного тела к другому за счет перемещения частиц (тел) под действием каких-либо сил.
Теплота и работа измеряются в единицах энергии (джоуль, калория, эрг и т. п.).
Важно, что обе величины не являются функциями состояния и зависят от способа передачи энергии (пути перехода системы из одного состояния в другое).
Рассмотрим два, наиболее часто встречающихся, случая изменения состояния системы:
- А) процесс может протекать при постоянном объеме (V = сonst); Б) процесс может протекать при постоянном давлении (Р = сonst).
Первый случай. Если не происходит изменения объема, то не совершается и работа системы против внешних сил, так как отсутствуют какие-либо перемещения. Следовательно, математическое выражение первого начала термодинамики примет следующий вид:
QV = ДU = U2 - U1 (3)
Т. е. вся теплота, поступающая в систему или уходящая из системы, связана только с изменением внутренней энергии. Такая ситуация имеет место в закрытом сосуде, объем которого меняться не может. Подстрочный индекс "V" в формуле (3) показывает, что процесс протекает при постоянном объеме.
Для того чтобы разобрать Второй случай, надо сначала получить выражение для работы системы против внешних сил. Будем считать, что имеется очень простая система: идеальный газ, находящийся в цилиндре с поршнем, который может перемещаться без трения (см. рис. 1).
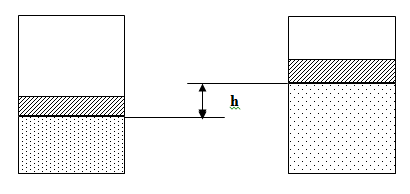
Рисунок 1 - К расчету работы расширения.
Если давление газа равно Р, а площадь сечения цилиндра S, то сила, действующая на поршень, будет равна, соответственно:
F = p-S (4)
Теперь, если поршень переместится на высоту H, то работа расширения, совершенная газом, будет равна:
A = p-S-h (5)
Так как произведение площади основания на высоту равно объему тела, то формулу можно изменить следующим образом:
A = p -ДV = p(V2 -V1) (6)
Где V2 и V1 - объемы системы, соответственно, после и до изменения
Состояния системы.
Полученную формулу подставим в алгебраическое выражение для первого начала термодинамики:
QP = (U2 - U1) + p(V2 - V1) (7)
Раскроем скобки и сгруппируем величины, соответствующие конечному и начальному состояниям системы:
OP = (U2 + pV2) - (U1 + pV1) (8)
Введем новую функцию состояния, которая больше величины внутренней энергии на величину работы расширения, и называется Энтальпией:
H = U + pV (9)
Таким образом, теплота, поступающая или уходящая из системы при постоянном давлении, равна изменению энтальпии системы:
Qp = H2 - H1 = ДH (10)
Являясь функцией состояния, энтальпия зависит только от начального и конечного состояний системы. Описанный случай изменения состояния системы может иметь место в открытом реакционном сосуде. Все процессы будут протекать при постоянном атмосферном давлении, что отражено в уравнениях (7), (8), (10) нижним индексом у символа теплоты.
Жидкие и твердые вещества расширяются или сжимаются незначительно при изменении состояния системы. Поэтому, при работе с конденсированными системами (жидкими или твердыми), изменением объема можно пренебречь. Работа в этом случае совершаться не будет, и, следовательно, тепловой эффект реакции подсчитывается как для систем при постоянном объеме, т. е., он равен изменению внутренней энергии.
Тепловые эффекты химических реакций и фазовых превращений изучаются в разделе химической термодинамики, называемом Термохимией.
Похожие статьи
-
Энтропия. Самопроизвольный процесс - Химическая термодинамика и ее процессы
Самопроизвольный процесс - процесс, который может протекать без затраты работы извне, причем в результате может быть получена работа в количестве,...
-
Термодинамика - наука о взаимопревращениях различных форм энергии и законах этих превращений. Термодинамика базируется только на экспериментально...
-
Введение - Химическая термодинамика. Термохимия. Решение задач
Химия изучает химическую форму движения материи, под которой понимают превращение одних веществ в другие. В результате химических процессов появляются...
-
ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА - Неограническая химия
Задание 3.1. Запишите реакцию взаимодействия указанного по варианту элемента с кислородом. Используя приведенные в табл. III.1 данные, рассчитайте...
-
Основные понятия теории экономико-математического моделирования Кибернетический подход к исследованию экономико-математических систем Обычно...
-
РЕШЕНИЕ ЗАДАЧИ О КОММИВОЯЖЕРЕ МЕТОДОМ ВЕТВЕЙ И ГРАНИЦ: ОСНОВНАЯ СХЕМА - Задача коммивояжера
Пусть - конечное множество и - вещественно-значная функция на нем; требуется найти минимум этой функции и элемент множества, на котором этот минимум...
-
К основным понятиям и категориям статистической науки относятся следующие: - совокупность, - признак, - показатель, - система показателей и др....
-
В данном разделе речь идет об особом уровне развития химических знаний, на котором главенствующую роль играет структура молекулы реагента. Свойства...
-
Наша группа работала над учебным межпредметным проектом "Математические модели в рыночной экономике". Мы покажем применение в экономике систем уравнений....
-
В условиях рыночной экономики возникают ситуации, в которых сталкиваются интересы двух и более сторон. Такие ситуации относятся к конфликтным. Например,...
-
Пусть функция определена в промежутке Х (рис.1). Исходя из некоторого значения независимой переменной, придадим ему приращение, не выводящее его из...
-
Основные понятия линейного программирования - Оптимальное программирование
Математические исследования отдельных экономических проблем, математическая формализация числового материала проводилась еще в XIX веке. При...
-
Основные понятия корреляционно-регрессионного анализа Теория и методы корреляционного анализа используются для выявления связи между случайными...
-
Химическим равновесием называется такое состояние химической системы, при котором количества исходных веществ и продуктов не меняются со временем. 1....
-
Динамическое программирование Динамическое программирование -- один из разделов оптимального программирования, в котором процесс принятия решения и...
-
Скорость реакции определяется изменением молярной концентрации одного из реагирующих веществ: V=dC/dtV. Факторы, влияющие на скорость химических...
-
При взаимодействии атомао м/у ними может возникнуть хим. связь, приводящая к образованию устойчивой многоатомной с-мы - молекулы, кристалла. Чем прочнее...
-
Провести комплексное исследование численных методов для задачи решения нелинейных уравнений. 1. Решить нелинейные уравнения А) ; Б) ; В) . 2....
-
Ответ: Функция y=arctgx, ее график, свойства Ответ: Функция y=arcctgx, ее график, свойства Ответ: Решение уравнений sinx=a, частные случаи Ответ:...
-
Условие задачи. Пусть имеются n кандидатов для выполнения этих работ. Назначение кандидата i на работу j связано с затратами CIj (i, j = 1,2,..., n)....
-
Цель и задачи исследования операций Исследование операций - научная дисциплина, занимающаяся разработкой и практическим применением методов наиболее...
-
Составление химических уравнений, Расчеты по химическим уравнениям - Основные понятия и законы химии
Включает три этапа: 1. Запись формул веществ, вступивших в реакцию (слева) и продуктов реакции (справа), соединив их по смыслу знаками "+" и "®" : HgO ®...
-
При решении экономических задач часто анализировать ситуации, в которых сталкиваются интересы двух или более конкурирующих сторон, преследующих различные...
-
Модель в общем смысле (обобщенная модель) есть создаваемый с целью получения и (или) хранения информации специфический объект (в форме мысленного образа,...
-
Основные понятия и определения проблемы прогнозирования - Прогнозирующие системы
Необходимо отметить, что мы рассматриваем прогнозирование в целях планирования производства или управления запасами. Таким образом, наш интерес лежит в...
-
ФУНКЦИИ, Основные понятия - Свойства функций
Основные понятия При изучении различного рода явлений приходится иметь дело с совокупностью переменных величин, которые связаны между собой таким...
-
Роберт Бойль, Михаил Васильевич Ломоносов - Становление понятий о химическом элементе
Бойль жил в эпоху великих общественных и духовных преобразований. Однако несмотря на сильные религиозные тенденции, Бойль научными работами расчистил...
-
Вариации коэффициентов целевой функции ЗЛП приводят к изменению направления вектора градиента. Так как при этом не затрагивается допустимое множество, то...
-
Исходная задача: При ограничениях: Двойственной является следующая задача: При ограничениях: Число неизвестных в двойственной задаче равно 2....
-
Пусть { , , ..., } - множество возможных состояний некоторой физической системы. В любой момент времени система может находиться только в одном...
-
Основные задачи анализа временных рядов - Динамические ряды
Принципиальные отличия временного ряда от последовательности наблюдений, образующих случайную выборку, заключаются в следующем: Во-первых, в отличие от...
-
Описание процессов, происходящих на поверхности, изобилует специальными терминами, и при рассмотрении адсорбционных явлений приходится говорить на языке,...
-
Введение, Основные положения - Эволюционные процедуры решения комбинаторных задач на графах
Среди набора комбинаторно-логических задач на графах важное место занимает проблема определения паросочетаний, раскраски графа, выделения в графе...
-
В термодинамике понятие "энтропия" было введено Р. Клаузиусом (1865), который показал, что процесс превращения теплоты в работу следует общей физической...
-
Вопросы: 1. Общее понятие о системах одновременных уравнений. 2. Структурная и приведенная формы модели. 3. Проблема идентификации. 4. Оценивание...
-
Понятие квантовой химии - Квантовые концепции в химии
Квантовая химия - это раздел теоретической химии, в котором строение и свойства химических соединений, их взаимодействие и превращение в химических...
-
Динамическое программирование (ДП) - Методики решения задач линейного и нелинейного программирования
Динамическими называются задачи экономики, организации и управления, в которых необходимо распределять ресурсы на каждом этапе какого - либо промежутка...
-
Прототипом разработанной автором системы моделей служит "точечная" модель [1], представляющая собой пространственно осредненный вариант уравнений горения...
-
Основные законы химии - Основные понятия и законы химии
Стехиометрия - это особый раздел химии, в котором изучают количественный состав веществ, а также количественные изменения, происходящие с ними при...
-
В последнее десятилетие в нашей стране очень сильно возросло потребление парфюмерно-косметических товаров. На российском рынке постоянно появляются новые...
Основные понятия химической термодинамики - Химическая термодинамика. Термохимия. Решение задач