Гетерогенный катализ - Гомогенный и гетерогенный катализ. Промышленный катализ. Технологические приемы ускорения и замедления реакций
Гетерогенный катализ - каталитические реакции, идущие на поверхности раздела фаз, образуемых катализатором и реагирующими веществами. Механизм гетерогенно-каталитических процессов значительно более сложен, чем в случае гомогенного катализа. В каждой гетерогенно-каталитической реакции можно выделить как минимум шесть стадий: Механизм гетерогенного катализа включает пять стадий, причем все они
Обратимы.
- 1. Диффузия исходных веществ к поверхности катализатора. 2. Адсорбция исходных веществ на поверхности с образованием некоторого промежуточного соединения:
А + В + К --> АВК
3. Активация адсорбированного состояния (необходимая для этого энергия есть истинная энергия активации процесса):
АВК --> АВК#
4. Распад активированного комплекса с образованием адсорбированных продуктов реакции:
АВК# --> СDК
5. Десорбция продуктов реакции с поверхности катализатора.
СDК --> С + D + К
6. Диффузия продуктов реакции от поверхности катализатора.
Специфической особенностью гетерокаталитических процессов является способность катализатора к промотированию и отравлению.
Промотирование - увеличение активности катализатора в присутствии веществ, которые сами не являются катализаторами данного процесса (промоторов). Например, для катализируемой металлическим никелем реакции.
Катализатор, замедляющий скорость химической реакции, называют ингибитором.
СО + Н2 --> СН4 + Н2О
Введение в никелевый катализатор небольшой примеси церия приводит к резкому возрастанию активности катализатора.
Отравление - резкое снижение активности катализатора в присутствии некоторых веществ (т. н. каталитических ядов). Например, для реакции синтеза аммиака (катализатор - губчатое железо), присутствие в реакционной смеси соединений кислорода или серы вызывает резкое снижение активности железного катализатора; в то же время способность катализатора адсорбировать исходные вещества снижается очень незначительно.
Для объяснения этих особенностей гетерогенно-каталитических процессов Г. Тэйлором было высказано следующее предположение: каталитически активной является не вся поверхность катализатора, а лишь некоторые ее участки - т. н. активные центры, которыми могут являться различные дефекты кристаллической структуры катализатора (например, выступы либо впадины на поверхности катализатора). В настоящее время нет единой теории гетерогенного катализа. Для металлических катализаторов была разработана теория мультиплетов. Основные положения мультиплетной теории состоят в следующем:
- 1. Активный центр катализатора представляет собой совокупность определенного числа адсорбционных центров, расположенных на поверхности катализатора в геометрическом соответствии со строением молекулы, претерпевающей превращение. 2. При адсорбции реагирующих молекул на активном центре образуется мультиплетный комплекс, в результате чего происходит перераспределение связей, приводящее к образованию продуктов реакции.
Теорию мультиплетов называют иногда теорией геометрического подобия активного центра и реагирующих молекул. Для различных реакций число адсорбционных центров (каждый из которых отождествляется с атомом металла) в активном центре различно - 2, 3, 4 и т. д. Подобные активные центры называются соответственно дублет, триплет, квадруплет и т. д. (в общем случае мультиплет, чему и обязана теория своим названием).
Например, согласно теории мультиплетов, дегидрирование предельных одноатомных спиртов происходит на дублете, а дегидрирование циклогексана - на секстете (рис. 2.10 - 2.11); теория мультиплетов позволила связать каталитическую активность металлов с величиной их атомного радиуса.
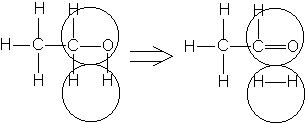
Рис. 1.2 Дегидрирование спиртов на дублете
Рис. 1.3 Дегидрирование циклогексана на секстете

Похожие статьи
-
Катамлиз (греч. кбфЬлхуйт восходит к кбфблэейн -- разрушение) -- избирательное ускорение одного из возможных термодинамически разрешенных направлений...
-
Введение, Гомогенный и гетерогенный катализ - Гомогенный и гетерогенный катализ
Химические реакции протекают с различными скоростями. Некоторые из них полностью заканчиваются за малые доли секунды, другие осуществляются за минуты,...
-
Гомогенный катализ - каталитические реакции, в которых реагенты и катализатор находятся в одной фазе. В случае гомогенно-каталитических процессов...
-
Энергетический профиль каталитической реакции - Гомогенный и гетерогенный катализ
Энергетический профиль реакции - это кривая, которая показывает зависимость координаты реакции (насколько прошла реакция) от времени (при постоянном...
-
"Катализ. Гомогенный и гетерогенный катализ" - Гомогенный и гетерогенный катализ
В 1835 году Берцелиус впервые использовал термин "катализатор" для обозначения "веществ, которые способны пробудить сродство, дремлющее при данной...
-
Гомогенный и гетерогенный катализ - Систематика химических элементов
Вещества, увеличивающие скорость химической реакции, называются Катализаторами. Явление возрастания скорости реакции под действием таких веществ,...
-
Высокая каталитическая эффективность. Отличительной особенностью любого фермента является его чрезвычайно высокая каталитическая эффективность. Так,...
-
Гетерогенный катализ - Гомогенный и гетерогенный катализ
Механизм гетерогенного катализа включает пять стадий, причем все они обратимы. 1. Диффузия реагирующих веществ к поверхности твердого вещества. 2....
-
Гомогенный и гетерогенный катализ. Механизм действия катализатора - Основы химии
При гомогенном катализе катализатор и реагирующие вещества образуют одну фазу (газовая смесь или раствор). При гетерогенном катализе катализатор и...
-
Гомогенный катализ - Гомогенный и гетерогенный катализ
Среди многочисленных каталитических реакций особое место занимает катализ в цепных реакциях. "Цепными реакциями, как известно, называются такие...
-
Активность и селективность катализатора - Гомогенный и гетерогенный катализ
Все процессы переработки углеводородного сырья сопровождаются фазообразованием (испарение, катализ, крекинг и др.). Одна из задач физико-химической...
-
КАТАЛИЗ - процесс, заключающийся в изменении скорости химических реакций в присутствии веществ, называемых катализаторами. Катализаторы - вещества,...
-
Катализ, Разновидности катализа:, Принципы катализа: - Гомогенный и гетерогенный катализ
Явление катализа - Это изменение скорости реакции под действием некоторых веществ, которые к концу реакции остаются в химически неизменном виде....
-
НЕМНОГО О ПРОМЫШЛЕННОМ КАТАЛИЗЕ - Процесс катализа
На всю жизнь запомнилась мне проводившаяся по Энглеру разгонка полученного конденсата, в котором уже в начале опыта бензиновая фракция составляла 67%. Мы...
-
Общие сведения Гетерогенные реакции еще труднее для изучения, чем гомогенные, и в обычных учебниках общей химии им уделяется мало внимания, хотя они...
-
ГОМОГЕННЫЙ КАТАЛИЗ - Процесс катализа
Среди многочисленных каталитических реакций особое место занимает катализ в цепных реакциях. "Цепными реакциями, как известно, называются такие...
-
КАТАЛИЗ В БИОХИМИИ - Процесс катализа
Ферментативный катализ неразрывно связан с жизнедеятельностью организмов растительного и животного мира. Многие жизненно важные химические реакции,...
-
ГЕТЕРОГЕННЫЙ КАТАЛИЗ - Процесс катализа
К сожалению, до сих пор, несмотря на достаточно большое число теорий и гипотез в области катализа, многие основополагающие открытия были сделаны случайно...
-
В предыдущих разделах рассмотрены отдельные аспекты кинетики, а теперь пора подвести общие итоги: от чего зависят скорости реакций и как можно ими...
-
Скорость реакции определяется изменением молярной концентрации одного из реагирующих веществ: V=dC/dtV. Факторы, влияющие на скорость химических...
-
Общее понятие о цепных реакциях и автокатализе - Принципы горения и взрыва
К цепным реакциям относят реакции, протекающие с образованием свободных радикалов, способных превращать реагенты в конечные продукты, поддерживая...
-
Катализ - Концепции современного естествознания: химическая составляющая
Наиболее сильное влияние на скорость реакции оказывает присутствие в реагирующей системе Катализатора -- вещества, которое повышает (а иногда и уменьшает...
-
При использовании разомкнутых химико-технологических систем в большинстве случаев принципиально невозможно проведение процессов при практически полной...
-
Введение - Разработка технологической схемы получения анизола и крезола
Известно в некоторых случаях невозможно достичь высокой селективности химико-технологических процессов. Это происходит вследствие наличия побочных...
-
Получение синтезированного газа - Анализ и технологическая оценка химического производства
Химические методы переработки нефти проводят при высоких температурах без катализатора (термический крекинг), при высоких температурах в присутствии...
-
Теоретические основы процесса Реакторы смешения - это емкостные аппараты с мешалкой или циркуляционным насосом. Человечество давно пользуется...
-
ВИДНЫЕ ДЕЯТЕЛИ ХИМИИ О КАТАЛИЗЕ - Процесс катализа
И. Берцелиус (1837): "Известные вещества оказывают при соприкосновении с другими веществами такое влияние на последние, что возникает химическое...
-
Уравнение Михаэлиса-Ментен и его анализ - Гомогенный и гетерогенный катализ
Уравнемние Михаэмлиса -- Мемнтен -- основное уравнение ферментативной кинетики, описывает зависимость скорости реакции, катализируемой ферментом, от...
-
Был проведен сравнительный анализ зависимости температуры охлажденных продуктов реакции от расхода охлаждающей воды для теплообменников с разной длиной...
-
Реакции окисления и восстановления - Особенность синтеза фенолов
Окислительно-восстановительные реакции, также редокс -- это встречно-параллельные химические реакции, протекающие с изменением степеней окисления атомов,...
-
Реакции с механизмом SN1 для ароматических соединений встречаются крайне редко и, по сути, характерны только для солей диазония. Эти реакции идут в...
-
ПРОХОЖДЕНИЕ ЧЕРЕЗ ЭНЕРГЕТИЧЕСКИЙ БАРЬЕР - Процесс катализа
Закон Аррениуса - экспериментально установленный факт. Он утверждает, что скорость реакции возрастает с увеличением температуры для преобладающего...
-
Типы окислительно-восстановительных реакций - Окислительно-восстановительные процессы
Различают три типа окислительно-восстановительных реакций. Межмолекулярные реакции - это реакции, которые протекают с изменением степеней окисления...
-
Один из способов повысить селективность - это правильно подобрать катализатор. Рассмотрим этот метод, на примере получения анизола и крезола. Анизол и...
-
Таблица 2 - Структура сырья в производстве метанола, %. Сырье В мире Беларусь и Россия Природный газ 73,8 70,7 Нефть и нефтепродукты 24,4 4,0 Отходы...
-
Общие понятия и определения. Термодинамический и кинетический критерий реакционной способности химической системы. Скорость химической реакции. Факторы,...
-
Качественные методы анализа - Разработка технологической схемы получения анизола и крезола
Рециркуляционных реакционно-ректификационных процессов. При анализе сложных ХТС, характеризующихся большим числом параметров и переменных необходимо...
-
Скорость химической реакции. Энергия активации химической реакции Химическая термодинамика изучает возможность, направление и пределы самопроизвольного...
-
Кинетика химических реакций - Концепции современного естествознания: химическая составляющая
Одна из особенностей химических реакций заключается в том, что они протекают во времени. Одни реакции протекают медленно, месяцами, как, например,...
-
Кинетика и катализ, Теоретические основы термического пиролиза - Пиролиз углеводородного сырья
Теоретические основы термического пиролиза Термическое разложение углеводородов представляет собой сложный процесс, который можно представить как ряд...
Гетерогенный катализ - Гомогенный и гетерогенный катализ. Промышленный катализ. Технологические приемы ускорения и замедления реакций