ГЕТЕРОГЕННО-КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ, Общие представления о катализе - Химические процессы и реакторы
Явления ускорения химических превращений в результате присутствия веществ, не принимающих видимого участия в реакции, были открыты уже на ранних этапах становления химической науки. Особый интерес к катализу проявился в период интенсивного развития промышленной химии, так как возможность ускорять химические реакции в нужном направлении без расхода энергии и, по существу, без расхода самого вещества катализатора придали катализу большую практическую значимость. С использованием катализа решаются задачи, стоящие перед технологией связанного азота, более 80 % нефти перерабатывается с использованием каталитических процессов, невозможно без катализаторов осуществление большинства процессов органического синтеза. В последние годы катализаторы стали применять для решения энергетических и экологических задач, таких, как создание топливных элементов, очистка выхлопных газов автомобилей и промышленных производств и т. д.
Общие представления о катализе
Катализаторы - это вещества, которые, многократно вступая в промежуточное взаимодействие с участниками реакции, изменяют ее механизм и увеличивают скорость реакции. Они восстанавливают свой химический состав после каждого цикла промежуточных взаимодействий.
Влияние катализатора на механизм химической реакции можно пояснить на условном примере. Пусть протекает одностадийная реакция с энергией активации E0
А+В R.
Ход реакции на энергетической диаграмме (см. рис. 8.1) изображен кривой 2. В присутствии катализатора механизм реакции изменяется, она протекает через несколько последовательных стадий (кривая 1). Например, первой стадией может быть образование промежуточного активированного комплекса (АКт):
А + Кт АКт
(здесь Кт - катализатор). Затем активированный комплекс реагирует со вторым реагентом с образованием комплекса катализатора и продукта:
АКт + В RKt.
Последней стадией является разложение комплекса RKt с образованием продукта R и высвобождением катализатора для нового каталитического цикла:
RKт R + Кт.
Каждая из этих последовательных стадий характеризуется своими значениями энергии активации E1, E2, Е3 (кривая 2), но, как правило, высота каждого из этих потенциальных барьеров ниже энергии активации Е0. Таким образом, в присутствии катализатора реакция протекает по энергетически более выгодному пути, что позволяет проводить процесс с большей скоростью.
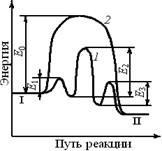
Рис. 8.1. Энергетические диаграммы каталитической и некаталитической реакций. Энергетический уровень: I - исходных реагентов; II - продуктов реакции; 1 - путь каталитической реакции; 2 - путь реакции без катализатора
Исходное (I) и конечное (II) энергетические состояния реакционной системы в присутствии катализатора и без него остаются одинаковыми. Следовательно, Катализатор не может изменить состояние химического равновесия, которое не зависит от пути реакции.
Роль катализатора состоит в изменении скорости достижения состояния равновесия. Катализатор может увеличивать скорость только тех процессов, которые разрешены термодинамически, но не может инициировать реакции, протекание которых невозможно при данных условиях в соответствии с законами химической термодинамики.
Некоторые химические реакции без катализаторов практически неосуществимы, например, из-за слишком большой энергии активации. Казалось бы, что для преодоления высокого энергетического барьера можно повысить кинетическую энергию молекул, т. е. увеличить температуру. Но для многих обратимых экзотермических реакций повышение температуры приводит к смещению равновесия в обратную сторону и делает реакцию неразрешенной термодинамически. В таких случаях применение катализатора не только оправдано, но и необходимо. Катализатор снижает энергию активации реакции и позволяет тем самым проводить ее при существенно более низких температурах.
В качестве примера рассмотрим реакцию синтеза аммиака, характеризующуюся очень большим значением энергии активации (примерно 280 кДж/моль). Для преодоления такого высокого энергетического барьера реагенты необходимо было бы нагреть до температур выше 1000 °С, при которых равновесная степень превращения даже при очень высоких значениях давления ничтожно мала.
В присутствии катализатора на основе железа энергия активации синтеза аммиака снижается примерно до 160 кДж/моль, что позволяет проводить реально процесс с достаточно высокой скоростью при температурах 400-500 °С и высоких давлениях, достигая 20-35%-ной степени превращения исходного сырья.
Чрезвычайно важна роль катализаторов в осуществлении сложных реакций, так как катализаторы обладают способностью избирательно влиять на скорость только какой-то одной нужной реакции. Так, например, сейчас трудно представить процесс крекинга нефтепродуктов (система сложных последовательных и параллельных реакций) без селективно действующих цеолитных катализаторов, позволяющих направить процесс в сторону получения высококачественного бензина.
Каталитические процессы подразделяют на две большие группы: Гомогенные И Гетерогенные. Наибольшее распространение в промышленности получили Гетерогенно-каталитические Процессы. В свою очередь, при протекании подавляющего большинства гетерогенно-каталитических процессов границей раздела фаз служит поверхность твердого катализатора, находящегося в газообразной или жидкой реакционной среде. Существенным преимуществом таких процессов является простота разделения продуктов реакции и частиц катализатора для повторного использования катализатора.
В конце XX в. активно развивались новые направления катализа, которые в какой-то степени сближают гомогенный и гетерогенный катализ. Большие перспективы открывает иммобилизация гомогенных комплексных катализаторов в полимерных гелях, т. е. закрепление их на макромолекулах химическим или иным связыванием. Новые возможности проведения технологических процессов в сравнительно мягких условиях (невысокие значения температуры, давления) могут появиться с использованием катализа на иммобилизованных ферментах. Хотя это направление еще не получило широкого развития вследствие высокой стоимости ферментов, развитие современной биотехнологии и инженерной генетики обеспечивает все большую доступность ферментов.
В данной главе будут рассмотрены особенности кинетики гетерогенно-каталитических процессов применительно к системе "твердый катализатор - газообразная (жидкая) реакционная среда".
Похожие статьи
-
Способы изменения скорости простых и сложных реакций - Химические процессы и реакторы
Как указывалось, скорость химической реакции зависит от большого числа различных факторов. Из кинетических уравнений следует, прежде всего, что скорость...
-
ГЕТЕРОГЕННЫЕ ПРОЦЕССЫ, Общие особенности - Химические процессы и реакторы
Большинство химических реакций, используемых в химико-технологических процессах, протекает с участием веществ, находящихся в разных фазах. В зависимости...
-
КАТАЛИЗ В БИОХИМИИ - Процесс катализа
Ферментативный катализ неразрывно связан с жизнедеятельностью организмов растительного и животного мира. Многие жизненно важные химические реакции,...
-
НЕМНОГО О ПРОМЫШЛЕННОМ КАТАЛИЗЕ - Процесс катализа
На всю жизнь запомнилась мне проводившаяся по Энглеру разгонка полученного конденсата, в котором уже в начале опыта бензиновая фракция составляла 67%. Мы...
-
КАТАЛИЗ - процесс, заключающийся в изменении скорости химических реакций в присутствии веществ, называемых катализаторами. Катализаторы - вещества,...
-
Равновесие химических реакций - Химические процессы и реакторы
Под воздействием подвода или отвода энергии в форме теплоты или работы происходит изменение состояния термодинамической системы (значений...
-
Об эффективности осуществления любого промышленного процесса судят прежде всего по экономическим показателям, таким, как приведенные затраты,...
-
Теоретические основы процесса Реакторы смешения - это емкостные аппараты с мешалкой или циркуляционным насосом. Человечество давно пользуется...
-
ХИМИКО-ТЕХНОЛОГИЧЕСКИЙ ПРОЦЕСС И ЕГО СОДЕРЖАНИЕ - Химические процессы и реакторы
Химико-технологический процесс представляет собой совокупность операций, позволяющих получить целевой продукт из исходного сырья. Все эти операции входят...
-
ЭНЕРГЕТИЧЕСКИЙ БАРЬЕР - Процесс катализа
Все каталитические реакции - самопроизвольный процесс, т. е. протекают в направлении убыли энергии Гиббса - убыли энергии системы. Давно уже было...
-
Общие понятия и определения. Термодинамический и кинетический критерий реакционной способности химической системы. Скорость химической реакции. Факторы,...
-
РОЛЬ КАТАЛИЗА В ЭКОЛОГИИ - Процесс катализа
Огромную роль призван сыграть катализ в решении актуальнейшей проблемы - охраны окружающей среды. По словам Кусто, земной шар напоминает "одиноко...
-
ВИДНЫЕ ДЕЯТЕЛИ ХИМИИ О КАТАЛИЗЕ - Процесс катализа
И. Берцелиус (1837): "Известные вещества оказывают при соприкосновении с другими веществами такое влияние на последние, что возникает химическое...
-
Способы смещения равновесия - Химические процессы и реакторы
Положение равновесия всегда зависит от внешних условий, а так как внешние условия не могут сохраняться неизменными, то равновесие рано или поздно...
-
Скорость химического превращения зависит от большого числа переменных. Результаты экспериментальных исследований различных реакций показали, что на...
-
Скорость гомогенных химических реакций - Химические процессы и реакторы
Скорость химической реакции W RJ принято выражать количеством (моль) N J одного из реагентов или продуктов, прореагировавшим (или образовавшимся) в...
-
Как видно из примеров 5.1 и 5.2, при одинаковых условиях проведения одной и той же реакции для достижения равной глубины превращения среднее время...
-
Гетерогенные процессы в системе "газ - жидкость" - Химические процессы и реакторы
Газожидкостные реакции - гетерогенные процессы, включающие в себя химическое взаимодействие между реагентами, один из которых находится в газовой фазе, а...
-
В предыдущих параграфах были рассмотрены варианты тепловых режимов химических реакторов и способы учета теплопереноса в реакторе при разработке...
-
ТЕПЛОПЕРЕНОС В ХИМИЧЕСКИХ РЕАКТОРАХ - Химические процессы и реакторы
Характер распределения температуры в химическом реакторе чрезвычайно важен при анализе протекающих в нем процессов, так как температура - один из...
-
Реактор идеального вытеснения - Химические процессы и реакторы
Реактор идеального вытеснения представляет собой длинный канал, через который реакционная смесь движется в поршневом режиме (рис. 5.4). Каждый элемент...
-
Классификация химических реакторов и режимов их работы - Химические процессы и реакторы
Химические реакторы для проведения различных процессов отличаются друг от друга по конструктивным особенностям, размеру, внешнему виду. Однако, несмотря...
-
В современной химии известно большое число различных химических реакций. Многие из них осуществляются в промышленных химических реакторах и,...
-
Центральным аппаратом в любой химико-технологической системе, включающей целый ряд машин и аппаратов, соединенных между собой различными связями,...
-
Гомогенный и гетерогенный катализ - Систематика химических элементов
Вещества, увеличивающие скорость химической реакции, называются Катализаторами. Явление возрастания скорости реакции под действием таких веществ,...
-
Катализ - Концепции современного естествознания: химическая составляющая
Наиболее сильное влияние на скорость реакции оказывает присутствие в реагирующей системе Катализатора -- вещества, которое повышает (а иногда и уменьшает...
-
ПРОХОЖДЕНИЕ ЧЕРЕЗ ЭНЕРГЕТИЧЕСКИЙ БАРЬЕР - Процесс катализа
Закон Аррениуса - экспериментально установленный факт. Он утверждает, что скорость реакции возрастает с увеличением температуры для преобладающего...
-
Структура математической модели химического реактора - Химические процессы и реакторы
Математические модели высоких уровней иерархии включают в себя, как правило, несколько уравнений, как конечных, не содержащих операторов...
-
Расчет равновесия по термодинамическим данным - Химические процессы и реакторы
Расчет константы равновесия и изменения энергии Гиббса позволяет определить равновесный состав реакционной смеси, а также и максимально возможное...
-
Гетерогенные процессы в системе "газ - твердое вещество" - распространенный вид промышленных химико-технологических процессов. Это процессы обжига...
-
Диффузионные стадии - Химические процессы и реакторы
В результате протекания гетерогенной химической реакции в разных точках реакционного пространства устанавливаются различные концентрации реагирующих...
-
Химическая термодинамика позволяет решать вопрос о направлении протекания химических реакций и оценить предельно достижимые (равновесные) состояния...
-
Стехиометрия химических реакций - Химические процессы и реакторы
Для описания химических реакций, лежащих в основе промышленных химико-технологических процессов, используют основные законы химии - законы стехиометрии,...
-
"Катализ. Гомогенный и гетерогенный катализ" - Гомогенный и гетерогенный катализ
В 1835 году Берцелиус впервые использовал термин "катализатор" для обозначения "веществ, которые способны пробудить сродство, дремлющее при данной...
-
Введение, Гомогенный и гетерогенный катализ - Гомогенный и гетерогенный катализ
Химические реакции протекают с различными скоростями. Некоторые из них полностью заканчиваются за малые доли секунды, другие осуществляются за минуты,...
-
Катамлиз (греч. кбфЬлхуйт восходит к кбфблэейн -- разрушение) -- избирательное ускорение одного из возможных термодинамически разрешенных направлений...
-
СО2 + С = 2СО Если известно, что для СО2 ДG2980 = - 394572 Дж/моль и для СО ДG2980 = - 137334 Дж/моль. Рассчитаем ДG2980 = 2ДGСО - ДGСО2 = 2*(137,334)...
-
Один из способов повысить селективность - это правильно подобрать катализатор. Рассмотрим этот метод, на примере получения анизола и крезола. Анизол и...
-
Прежде чем рассмотреть отдельные типы химических реакторов в соответствии с приведенной классификацией, составим уравнение материального баланса по...
-
Проточный реактор идеального смешения в неизотермическом режиме - Химические процессы и реакторы
При составлении балансовых уравнений в качестве элементарного объема для реактора идеального смешения принимают полный реакционный объем V. Тепловые...
ГЕТЕРОГЕННО-КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ, Общие представления о катализе - Химические процессы и реакторы