Физико-химические основы процесса - Термический крекинг в ТОО "Павлодарский нефтехимический завод"
Термические превращения нефтяных фракций - весьма сложный химический процесс. Сырье состоит из большого числа индивидуальных компонентов. Совершенно очевидно, что предсказать или проследить судьбу каждого компонента сырья при воздействии высоких температур невозможно. Поэтому на практике о результатах того или иного высокотемпературного процесса судят обычно по выходам целевых продуктов: газа, бензина, кокса, а также по групповому или, в лучшем случае, компонентному составу бензинов. Однако многочисленные исследования термических превращений отдельных углеводородов позволяют делать выводы о характерных для данного класса углеводородов типах реакций.
Молекулярные - элементарные реакции, реагенты и продукты которых являются молекулами. В молекулярной реакции имеется только одно промежуточное состояние активированный комплекс.
Радикальные - реакции протекающие благодаря свободным радикалам:
Если на данной связи в молекуле сосредоточится энергия, равная или большая энергии связи то эта связь разрывается.

Механизм термического крекинга - радикально-цепной, протекает в 3стадии.
Инициирование цепи
Продолжение цепи
Обрыв цепи
Превращения алканов.
Инициирование цепи. Так как энергия С-С меньше, чем связи С-Н, то под воздействием повышенной температуры происходит разрыв связи С-С.
СН3(СН2)5 СН3 = С4Н9* + С3Н7* - инициирование цепи
- радикалы более высокой молекулярной массы, не обладающие в данных условиях хотя бы минимальной стабильностью, мгновенно распадаются с образованием устойчивого этиленового углеводорода и нового радикала
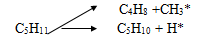
- свободные радикалы, сталкиваясь с молекулами исходного сырья, вызывают образование новых радикалов
R*H +H* =H2 + R|*
R|H +R* = RH +R| *
Цепная реакция развивается. Основная масса продуктов реакции получается в результате развития именно цепной реакции через свободные радикалы.
При достижении равновесия вероятность встречи свободных радикалов друг с другом становится не меньшей, чем вероятность их соударения с молекулами исходного сырья. Происходит обрыв цепи.
А) рекомбинация радикалов
СН3 *+ СН3 *= С2Н6
Б) реакция диспропорционирования радикалов
СН3* + С2Н5* = СН4 + С2Н4
Продукты реакции: устойчивые при данной температуре предельные и непредельные углеводороды и молекулярный водород.
Вывод: основной вид термических превращений алканов реакция распада по связи С-С с образованием алкана и алкена.
CNH2n+2 = CMH2m + CQH2q+2
Полученные предельные осколки вновь распадаются на алкен и алкан. Распад может происходить по всем связям С-С. место разрыва зависит от температуры и давления.
Чем выше температура и ниже давление, тем место разрыва углеродной цепи все больше смещается к ее концу и тем больше выход газообразных продуктов.
При температуре 4500С разрыв происходит по середине цепи. Повышение давления сдвигает место разрыва к центру молекулы. Поэтому крекинг под давлением позволяет получать больше жидких продуктов и меньше газа.
2. Превращения алкенов. Алкены не содержатся в нефтяных фракциях, но образуются при термическом разложении алканов и циклоалканов. Реакции распада алкенов имеют цепной механизм.

При температуре ниже 6000С винильный радикал может вступать только в реакцию присоединения к исходному этилену
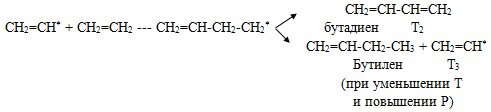
Отсюда следует:
Т1 Т2 Т3
Р1 Р2 Р3
Правило - связи определяет наиболее вероятное место распада в углеродной цепи. Связи С-С и С-Н в алкенах у атома углерода с двойной связью значительно прочнее, а положении сильно ослаблены.
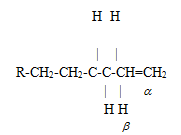
Механизм распада алкенов, так же как и алканов, имеет цепной характер. Первичный распад по -связи Дает начало двум радикалам. Так, для пентана:
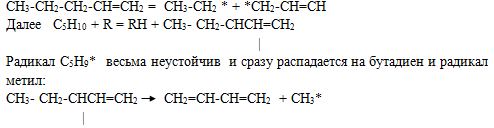
Дальнейшее развитие цепной реакции идет через радикал метил. Этот механизм хорошо объясняет получение из пентена бутадиена и метана:
С5Н10 = С4Н6 +СН4
Превращение циклоалканов.
Для нафтеновых углеводородов наиболее характерны следующие типы превращения при высоких температурах:
Деалкилирование - реакция, аналогичная распаду алканов. При температуре около 5000С расщепление происходит главным образом посередине цепи. Полное деалкилирование возможно лишь при более высоких температурах. Повышение давления препятствует деалкилированию.
Дегидрирование - более высокотемпературная реакция, ведущая к накоплению в продуктах крекинга и пиролиза циклоолефинов и ароматических углеводородов. Реакции благоприятствует пониженное давление.
Дециклизация - полициклических нафтенов приводит к последовательному упрощению молекул и сопровождается деалкилированием. Одновременно протекают реакции дегидрирования. Распад не имеет цепного характера. Термодинамически и кенитически реакция распада конкурирует с реакцией дегидрирования. Поэтому в продуктах крекинга можно обнаружить в сравнимых количествах и непредельные, и ароматические углеводороды.
Превращения аренов.
Ароматические углеводороды наиболее термически устойчивы. Поэтому они накапливаются в жидких продуктах крекинга тем в больших количествах, чем выше температура процесса. При пиролизе ароматические углеводороды являются главной составной частью так называемой смолы пиролиза. Ароматические углеводороды с длинными боковыми цепями способны деалкилироваться. Преимущественное место отрыва боковой цепи находится между первым и вторым атомами углерода в цепи, т. е. - положении от углеродного кольца. Поэтому при деалкилировании получаются главным образом монометилированные ароматические углеводороды. Голоядерные углеводороды любой степени цикличности (бензол, нафталин, антрацен и др.), так же как и алкилированные углеводороды с короткими боковыми цепями, практически не подвергаются распаду. Единственным направлением их превращений является конденсация с выделением водорода. В результате происходит накопление полициклических углеводородов. В результате конденсации бензола, нафталина и других голоядерных углеводородов образуется дифенил, динафталин и им подобные углеводороды:
- 2С6Н6 =С6Н5-С6Н5 + Н2 2С10Н8 = С10Н7-С10Н7 + Н2
Эти реакции легко объясняются радикально-цепным механизмом. Образующийся радикал водорода порождает ароматические радикалы.
С6Н6 + Н* = Н2 +С6Н5*
Которые в дальнейшем рекомбинируют, что приводит к образованию конденсированных молекул. Развитие реакций конденсации разнообразных циклических углеводородов приводит в конечном итоге к образованию карбоидов (кокса).
Что касается сернистых соединений, то они либо разлагаются с выделением сероводорода, меркаптанов и углеводородных осколков, либо накапливаются в более высокомолекулярных продуктах.
Подводя итог рассмотрению химических превращений углеводородов различного строения при температурах крекинга и пиролиза, можно сделать вывод, что при деструктивной переработке нефтяного сырья должны осуществляться следующие основные реакции: распад, деалкилирование, дегидрирование, полимеризация, циклизация непредельных, дециклизация нафтенов, деструктивная конденсация олефинов, конденсация ароматических углеводородов, реакции глубокого уплотнения кокса. От глубины этих реакций и преобладания того или иного типа превращений углеводородов сырья и зависят выходы газа, бензина, промежуточных фракций, крекинг-остатка и кокса, а также качество и химический состав целевых продуктов.
При любом термическом крекинге в результате переработки образуются газы, бензины, средние дистиллятные фракции, тяжелые остаточные фракции и кокс. Выход, соотношение между продуктами реакции, свойства этих продуктов зависят от многих факторов, но главную роль играют состав сырья, температура, давление и продолжительность реакции. Температура и продолжительность процесса. Факторы влияющие на выход и качество продуктов термического крекинга, при определенных температурах взаимозаменяемы. Увеличивая температуру крекинга и уменьшая продолжительность времени пребывания в зоне высоких температур, можно получить ту же глубину разложения сырья, что и при более мягкой температуре, но большей длительности крекинга. Термическое разложение углеводородов начинается при 380- 400 ОС. Давление. При увеличении давления повышаются температуры кипения сырья и продуктов крекинга. Термический крекинг может осуществляться в паровой, жидкой и смешанной фазах. Тепловые эффекты реакций различаются по величине и знаку. Суммарный тепловой эффект термического крекинга отрицателен, и поэтому необходимо подводить тепло со стороны. Теплота реакции термического крекинга составляет 1,26-1,37 МДж/кг бензина при крекинге газойля и 0,63-0,75 МЖж/кг бензина при крекинге мазута.
Похожие статьи
-
При термическом крекинге получают газ, бензин, газойль и крекинг-остаток. В газе термического крекинга содержатся предельные (от метана до бутана) и...
-
Краткая характеристика установки - Термический крекинг в ТОО "Павлодарский нефтехимический завод"
При любом термическом процессе в результате переработки образуются газы, бензин, средние дистиллятные фракции (керосино - газойлевые), тяжелые остаточные...
-
Химические основы процесса - Каталитический крекинг
При каталитическом крекинге протекают реакции расщепления, алкилирования, изомеризации, ароматизации, полимеризации, гидрогенизации и деалкилирования....
-
Характеристика сырья. Состав сырья. В одинаковых условиях крекинга скорость реакции растет с повышением температуры кипения сырья. Такая особенность...
-
Термический крекинг. - Технология переработки нефти
Расщепление молекул углеводородов протекает при более высокой температуре (470-550°С) и давлении 2-7МПа. Процесс протекает медленно, образуются...
-
Для технологии процессов химической переработки нефтяного сырья характерно преимущественное применение высоких температур и зачастую высоких давлений....
-
Характеристики продуктов гидрокрекинга в очень сильной степени определяются свойствами катализатора -- его гидрирующей и кислотной активностью....
-
Назначение процесса - Каталитический крекинг
Основное назначение каталитического крекинга - получение высокооктановых компонентов бензина. Крекинг осуществляется при 420-550С и является процессом...
-
Ассортимент современных катализаторов гидрокрекинга достаточно обширен, что объясняется разнообразием назначений процесса. Обычно они состоят из...
-
Получение сульфата аммония основано на поглощении аммиака из коксового газа раствором серной кислоты и протекании реакции нейтрализации....
-
Каталитический крекинг - важнейший процесс нефтепереработки, существенно влияющий на эффективность НПЗ в целом. Сущность процесса заключается в...
-
Термический крекинг первый процесс, позволивший увеличить выход светлых продуктов из нефти и получить сырье для зарождавшейся нефтехимической...
-
Мороженое обладает высокой пищевой ценностью. Оно содержит молочный жир, белки, углеводы, минеральные вещества и витамины, легко усваивается организмом....
-
Алюминиевый сплав марки Д16 больше известен как дюраль или дюралюминий. Такое название носят все сплавы, в которых к алюминию добавлены медь и магний....
-
Физико-химические свойства сырья и продуктов - Процессы химической технологии
В качестве абсорбента чаще всего используют воду, не вступающую в реакцию с извлекаемым газом. Вода - бинарное неорганическое соединение с химической...
-
Физические основы процесса - Технологический расчет теплообменника
Пиролиз - термическое разложение органических и многих неорганических соединений. Основная цель процесс - получение углеводородного газа с высоким...
-
Факторы процесса: Качество сырья - Сырье не должно содержать примесей ядов кат-ра, S-, N-, O - - кислородсодержащих соед-ий и мех. примесей. Сырье должно...
-
Введение - Термический крекинг в ТОО "Павлодарский нефтехимический завод"
ТОО "Павлодарский нефтехимический завод" - крупнейшее в Казахстане предприятие по переработке нефти. Уникальный набор установок позволяет достигать...
-
При замене секции подготовки сырья FCC методом гидроочистки на гидрокрекинг с частичной конверсией сырья плотность сырья FCC уменьшается. Таким образом,...
-
Сернистые соединения, содержащиеся в нефтепродукте, подвергаются в процессе гидроочистки следующим реакциям: 1. Меркаптаны гидрируются до сероводорода и...
-
Замедленное коксование - длительный процесс термолиза тяжелых нефтяных остатков или ароматизированных высоко кипящих дистиллятов при невысоком давлении и...
-
Степень превращения (конверсия) показывает на сколько полно в хим.- технологическом процессе используется исходное сырье. Степень превращения - это...
-
При механической и тепловой кулинарной обработке происходят глубокие изменения в продуктах. Правильная обработка влияет на качество готового блюда....
-
Сплав Д1 - относится к числу дюралюминов. Такой вид сплавов обладает достаточно высокой прочностью, пластичностью и относится к числу нормальных...
-
Таблица 4 - Режимы термообработки Операция T, °С Охлаждающая среда HRC Цементация 930 Охлаждение медленное в колодцах или ящиках Закалка 820 - 840...
-
Хром - очень распространенный легирующий элемент. Он повышает точку А3 и понижают точку А4 (замыкает область г-железа). Температура эвтектоидного...
-
Физико-химические изменения, происходящие в процессе копчения, связаны с тепловым воздействием, влиянием посолочных веществ и значительным...
-
Физико-химические основы переработки пластмасс - Изготовление деталей из пластмасс
В основе процессов переработки пластмасс находятся физические и физико-химические процессы структурообразования и формования: 1) нагревание, плавление,...
-
Под созреванием сыра понимают глубокие изменения составных частей свежеприготовленного сыра, в результате которых он приобретает свойственные ему вкус,...
-
Превращения при отпуске - Характеристика термической обработки
Отпуском называют термическую операцию, заключающуюся в нагреве закаленной стали до температуры ниже ac1, с последующей выдержкой и охлаждением с...
-
Продукты каталитического крекинга - Каталитический крекинг
Количество и качество продуктов каталитического крекинга зависят от характеристики перерабатываемого сырья и катализаторов, а также от режима процесса....
-
Температура. Оптимальный интервал температуры для процессов гидрокрекинга 360-440оС с постепенным повышением от нижней границы к верхней по мере падения...
-
Кристаллизация - это переход вещества из газообразного (парообразного), жидкого или твердого аморфного состояния в кристаллическое, а также из одного...
-
Назначение цеха Цех предназначен для производства стирола методом дегидрирования этилбензола. Характеристика цеха: Год ввода в эксплуатацию - IV квартал...
-
Термические процессы. К числу термических процессов, проводимых при высоких температурах в зоне реакции (до 900 °С), относят: 1) термический крекинг и...
-
Технологическая схема - Каталитический крекинг
Рисунок 1. Схема установки каталитического крекинга с пневмотранспортом катализатора потоком высокой кон-центрации: П-1 - печь; Р-1 - реактор; Р-2 -...
-
Свойства титана Титан - металл серого цвета. Он имеет две полиморфные модификации. Отличительными особенностями являются хорошие механические свойства,...
-
Для анализа кристаллизационного процесса был выполнен ДТА сплавов системы Al - Si с содержанием Si: 0.25, 0.5, 1.0, 3.0 и 5.0 %. Основные параметры...
-
Теоретические основы процесса меднения - Серебрение алюминиевых деталей
Медные покрытия обычно не применяются как самостоятельные электролитические покрытия ни для защиты стальных деталей от коррозии, ни для декоративной цели...
-
Основы теории термической обработки Термической обработкой называют технологические процессы, состоящие из нагрева и охлаждения металлических изделий с...
Физико-химические основы процесса - Термический крекинг в ТОО "Павлодарский нефтехимический завод"