Использование белков семян овса для целей сортового контроля и идентификации
Введение
В получении оптимального уровня урожая особенно важное значение имеет использование семенного материала высокого сортового качества в сочетании со сбалансированной генетической структурой, близкой к оригинальному уровню. Вместе с тем точно, объективно и оперативно оценить семенной материал по данным критериям на основе традиционных методов контроля не всегда возможно.
В связи с этим в последнее время особый интерес вызывают разработки, направленные на поиск, создание и внедрение в практику более точных методов контроля, которые позволяют на уровне семян как определить показатели сортового качества, так и оценить генетическую структуру сорта. Особенно важным представляется разработка точных методов оценки для культур, определенные сорта которых могут быть использованы строго на планируемые цели - пивоваренный ячмень, безглютеновые сорта овса.
Разработка и практическая адаптация подобных методик оценки ведется многими исследовательскими центрами и лабораториями, работающими в области молекулярного маркирования генотипов растений, однако, несмотря на имеющиеся наработки, остается еще целый ряд моментов, требующих детального анализа и отработки применительно к целям семенного контроля и сертификации семян.
Цель работы - провести сопоставительный анализ белкового комплекса семян овса по критериям приемлемости использования в рамках разрабатываемой методики определения качества на основе метода электрофоретического анализа белков.
Анализ источников
До недавнего времени контроль качества сельскохозяйственной продукции осуществлялся исключительно визуальным путем, однако впоследствии такая практика не всегда давала ожидаемые и точные результаты. Лишь с повсеместным развитием системы нормирования и сертификации семенной продукции можно было говорить о более точном контроле и предсказуемых результатах. В то же самое время стандартизация сельскохозяйственной продукции и на сегодняшний день является недостаточно изученной областью и требует совершенствования применения методов контроля качества на основе точных и современных методов.
Современные методы, используемые для тестирования семян, основаны на научных достижениях молекулярной биологии и генетики. Открытия в этих областях позволили разработать методы биохимического анализа для сортовой идентификации зерна и муки, используемые Международной ассоциацией по испытанию cемян - ISTA [8, 9, 10, 15].
Электрофоретический белковый спектр очень сложен и сопряжен с показателями качества зерна, тем более что запасные белки составляют клейковинный комплекс хлеба [15, 18].
Для обеспечения единых требований в сортовой идентификации необходимы арбитражные стандартные методы электрофореза. С 1988 г. действуют Международные арбитражные стандартные методы идентификации пшеницы и ячменя электрофорезом глиадина и гордеина [10, 14].
Кроме использования метода в области контроля качества семян, В. Г. Конаревым были определены направления использования метода белковых маркеров в сортоиспытании, семеноводстве и семенном контроле по целому ряду приоритетных направлений, имеющих большое практическое значение для сохранения всех качеств сорта в ходе селекционно-семеноводческой работы [3, 6]. Как показал целый ряд проведенных исследований, даже в том случае, если сорт прошел испытания и был районирован, существует определенная доля риска, когда под воздействием различных факторов (чаще всего неконтролируемых) определенные ценные биотипы, генотипы сорта могут исчезать. Так, многолетние исследования российских селекционеров-генетиков показали, что в процессе репродуцирования сорт теряет отдельные биотипы, а при 30-летнем использовании приобретает такой биотипный состав, в котором уже трудно было отыскать исходный [2, 7].
Как указывает А. В. Конарев [4, 5, 6], для каждой культуры должны подбираться оптимальные маркерные системы, что требует кропотливой и продолжительной работы.
Для многих культур практически каждому сорту соответствуют свои собственные, характерные только для него электрофоретические спектры белков - их "отпечатки пальцев", что связано с адаптивным характером полиморфизма маркерных белков [5, 6]. Именно с использованием запасных белков семян в качестве маркеров связаны реальные практические достижения в идентификации и регистрации сортов в семеноводстве и семенном контроле, что закреплено в решениях Международной ассоциации по контролю за качеством семян (ISTА) и ряда других авторитетных организаций [11, 12].
Ранее проведенными исследованиями по сравнительной оценке особенностей и разрешающей способности двух способов идентификации сортов зерновых культур (на основе морфологических и молекулярных маркеров) была установлена необходимость комплексного использования данных маркирующих систем для более корректного анализа и точности [1].
Методы исследования
В качестве метода исследований использовался электрофоретический анализ белков семян.
Лабораторные испытания проводились на базе Испытательной лаборатории качества семян УО БГСХА, соответствующей критериям системы аккредитации Республики Беларусь и международным требованиям по СТБ ИСО / МЭК 17025-2007 (Аттестат № BY/112 02.1.0.0425 от 15.03.2004 г.).
Электрофоретический анализ белков овса, идентификацию и интерпретацию результатов полученных белковых спектров проводили в рамках отработки и адаптации с помощью методики определения в профильных испытательных лабораториях.
Отработка критериев приемлемости белков семян для целей методики определения, критериев идентификации компонентов белковых спектров проводилась с использованием обновленной, модернизированной и поверенной (аттестованной) приборно-технической базы Испытательной лаборатории качества семян.
Для точной оценки дифференцирующих позиций (зон) спектра, оценки молекулярных масс белков использовались стандартные маркер-растворы белков "Thermo Scientific"- Unstained Protein Ladder (диапазон 5-112 кДа, число идентифицируемых белков - 11).
Основная часть
В ходе проводимой работы ставилось несколько базовых задач: во-первых, оценить варианты белкового комплекса семян овса по критериям приемлемости для целей методики определения сортовых качеств; во-вторых, отработать алгоритмы идентификации сортовых маркеров и уровня полиморфности сортов овса.
Для оценки особенностей элементов белкового комплекса овса нами были использованы варианты с альбуминами, глобулинами и авенинами в различных сочетаниях экстрагирующих растворов и фракционирующих гелевых систем.
Прежде всего необходимо было установить вид белкового комплекса, наиболее полно отражающий внутреннюю генетическую структуру сортов овса на предмет выявления внутрисортовых различий и уровня генетического полиморфизма. В ходе своих исследований мы учитывали примерное процентное содержание различных типов белков в зерне овса - авенины на уровне 4-14 %, альбумины на уровне 9-20 %, глобулины на уровне 54-46 % от общего содержания белкового комплекса [15, 16].
1. Экстракция альбуминов и глобулинов раствором 1М NaCl
Данный вариант позволил получить белковый экстракт, содержащий альбуминовую и глобулиновые фракции. Экстракция проводилась при температуре 25 °С в течение 8 часов или при температуре 35 °С в течение 3,5 часов. В силу того что зерна овса содержат некоторое количество жировых и слизистых веществ [15], объем экстрагирующего агента был увеличен в 1,5 раза в сравнении с обычными объемами, принятыми для представителей зерновых.
Белковый экстракт центрифугировался при 7000 об./мин., очищенный супернатант использовался для фракционирования белков. Для электрофоретического разделения использовался экстракт белков в объеме 30 мкл с добавлением 30 мкл буфера нанесения, содержащего DS-Na. Для точного определения молекулярных масс компонентов белков и значений относительной электрофоретической подвижности (Rf) в крайние карманы гелевой пластины были нанесены кратные объемы растворов стандартных белков.
Формирование гелевого носителя для электрофоретического разделения белков производилось по методу Лаемли, что предполагает использование гелевой пластинки, состоящей из двух частей: концентрирующей белок и разделяющей его. Эффект концентрирования белка перед вхождением в разделяющий гель достигается тем, что концентрирующий гель имеет более крупные поры и более низкое значение рН.
Параметры напряжения и силы тока устанавливались по типу ступенчатых с градацией по зонам гелевой пластины.
Фиксация белковых компонентов и их окраска производились стандартным методом, фиксирующий агент - трихлоруксусная кислота, красящий агент - кумасси R-250.
Результаты проведенных испытаний были оценены по двум критериям: первый - получение белкового спектра высокой разрешающей способности, второй - возможность оценки внутри и межсортовых отличий. Данные проведенной оценки представлены на рис. 1 и 2.
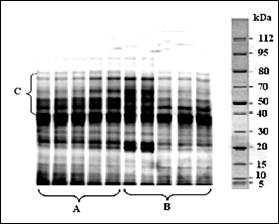
Рис. 1 Результаты SDS-ПААГ электрофореза альбуминов и глобулинов (овес "Юбиляр") Примечание: А - глобулины; В - альбумины; С - дифференцирующая зона
Как следует из данных распределения белковых компонентов, представленных на рис. 1, наиболее вариабельными оказались фракции альбуминов, на основе анализа которых возможна оценка внутренней структуры сортов. Наибольшей дифференцирующей способностью характеризовались компоненты белка с молекулярной массой от 47 до 78 кДа и значением относительной подвижности 55-70 Rf.

I II
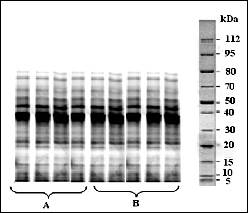
Рис. 2 Сравнительный анализ сортов овса на основе электрофоретического анализа альбуминов (I) и глобулинов (II)
Примечание: А - сорт Юбиляр; В - сорт Эрбграф
Вместе с тем при межсортовом сравнении (рис. 2) компоненты альбуминов и глобулинов не позволяют четко выявить сортовые маркеры и, следовательно, не могут быть рекомендованы для использования в целях сортовой идентификации.
В ходе исследования нами целенаправленно использовались сорта овса различных селекционных зон, что с большой долей вероятности должно обеспечивать их не только фенотипические, но и генетические отличия, выявляемые методом электрофоретического анализа белков. Однако в ходе исследований нами не была установлена четкая межсортовая дифференциация на основе анализа компонентов альбуминов и глобулинов для генетически различных генотипов.
2. Экстракция авенинов растворами Na - фосфата, водным раствором этилового спирта
Белки экстрагировались 2-кратным объемом буферного раствора с Na - фосфатом при комнатной температуре в течение 5 часов, 70 %-м раствором этанола при температуре 25°С в течение 2,5 часов, раствором 6М мочевины при температуре 4°С. По истечении времени экстрагирования супернатант центрифугировался при 9000 тыс. об./мин. (вариант с Na - фосфатом) и 3000 тыс. об./мин. (вариант с раствором этилового спирта).
В варианте с Na - фосфатом была использована гелевая система по методу Лаемли с градацией напряжения по зонам пластины и рабочим буфером, содержащим DS-Na; при использовании 70 %-го этанола использовался ПААГ с параметрами Т= 13,36 %, С= 2,69 % и алюминий-лактатным буфером; в варианте с 6М мочевиной использовался 7,5 %-ый ПААГ с ацетатным буфером.

Рис. 3 Результаты SDS-ПААГ электрофореза на основе буфера с Na - фосфатом
Примечание: А - сорт Юбиляр; В - сорт Эрбграф
Как наглядно свидетельствует рис. 3, экстракция белков семян овса на основе буфера с Na - фосфатом не выявила четких дифференцирующих позиций ни при внутрисортовом сравнении, ни при сравнении сортов между собой. Несмотря на то что компонентная представленность авенинов имела довольно четкую степень выраженности в зоне 50-80 кДа и 15-20 кДа, оценить характер внутрисортового полиморфизма, а тем более идентифицировать сорт не представляется возможным.
На рис. 4 представлена картина распределения и дифференциации белковых фракций авенинов, экстрагированных водным раствором этанола с предварительным очищением супернатанта центрифугированием.
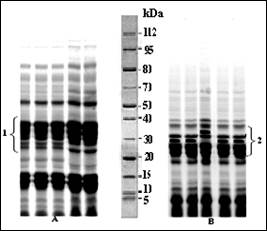
Рис. 4 Результаты ПААГ электрофореза на основе экстрагирования 70 % раствором этанола
Примечание: А - сорт Юбиляр; В - сорт Эрбграф; 1 и 2 - зоны дифференциации
В данном варианте проявились довольно четкие дифференцирующие маркерные компоненты белка, позволяющие четко оценить как характер и степень внутрисортового разнообразия анализируемых сортов, так и наличие четко выраженных генетических отличий сортов. Так, наибольшую разрешающую способность в оценке внутрисортового полиморфизма проявляли белковые компоненты с молекулярными массами 15-20 и 25-30 кДа у сорта Юбиляр, 30-35 кДа у сорта Эрбграф. Число дифференцирующих компонентов составляло 4 (Юбиляр) и 2 единицы (Эрбграф), что является вполне достаточным для четкой и однозначной идентификации белковых биотипов сорта и контроля генетической конституции анализируемых сортов.
Число белковых компонентов, являющихся маркерами межсортовых отличий, составляло 5 единиц, расположенных в довольно широком диапазоне молекулярных масс - от 15 до 75 кДа, что также является подтверждением приемлемости выявленных белковых фракций для идентификации сорта.
Таким образом, на основании проведенной оценки особенностей экстракционного режима белков, типа белкового комплекса и ряда режимов электрофоретического фракционирования можно сделать вывод о приемлемости для целей практического использования в области сортовой идентификации и оценке сортовой чистоты белков типа авенинов с экстракционным агентом в виде водного раствора этанола. Для оценки внутрисортового разнообразия, идентификации белковых биотипов, точного определения молекулярных масс определенных белковых фракций и их относительной электрофоретической подвижности допустимо использовать вариант с экстракцией альбуминовой фракции с проведением электрофоретического разделения белков на гелевом носителе по методу Лаемли в системе SDS-ПААГ электрофореза.
Заключение
- 1. В результате проведенных исследований установлен различный характер распределения и формирования фракций белкового комплекса зерна овса. 2. По результатам сравнительной оценки белков альбуминовой и глобулиновой природы наиболее вариабельными оказались фракции альбуминов, на основе анализа которых возможна оценка внутренней структуры сортов. 3. Не установлена приемлемость альбуминовых белков для целей сортовой идентификации и сортового контроля на основе метода электрофореза. 4. По результатам оценки разрешающей способности фракций авенинов, экстрагируемых буфером на основе Na - фосфата, не выявлено четких дифференцирующих позиций ни при внутрисортовом сравнении, ни при сравнении сортов между собой. 5. В варианте с экстракцией авенинов водным раствором этанола выявлены дифференцирующие маркерные компоненты, что позволяет на их основе четко оценить как характер и степень внутрисортового разнообразия анализируемых сортов, так и наличие четко выраженных генетических отличий сортов. 6. В качестве процедурного элемента методики определения качества семян овса рекомендовано включать вариант экстракции авенинов раствором этилового спирта с очищением супернатанта центрифугированием. Для идентификации белковых биотипов допускается использовать белки альбуминовой природы с фракционированием в системе SDS-ПААГ электрофореза.
Литература
- 1. Дуктова, Н. А. Сравнительная оценка методов идентификации сортов зерновых культур / Н. А. Дуктова, С. В. Егоров, Е. В. Егорова // Земляробства i ахова раслiн. 2011. № 2. С. 3-6. 2. Колючий, В. Т. Электрофоретический анализ биотипного состава пшеницы на начальном этапе изменения яровых зерновых культур / В. Т. Колючий // Селекция, семеноводства и агротехника зерновых культур. 1983. № 2. С. 71-74. 3. Конарев, А. В. Использование молекулярных маркеров в работе с генетическими ресурсами растений / А. В. Конарев. СПб.: ВИР, 1998. №5. С. 3?25. 4. Конарев, А. В. Адаптивный характер молекулярного полиморфизма и его использование в решении проблем генетических ресурсов растений и селекции / А. В. Конарев // Аграрная Россия. 2002. № 3. С. 4-44. 5. Конарев, А. В. Использование молекулярных маркеров в решении проблем генетических ресурсов растений и селекции / А. В. Конарев // Аграрная Россия. 2006. № 6. С. 4-22. 6. Конарев, В. Г. Морфогенез и молекулярно-биологический анализ растений / В. Г. Конарев. СПб.: ВИР, 1998. 370 с. 7. Неттевич, Э. Д. Метод электрофореза при изучении внутрисортовой изменчивости качества пшеницы / Э. Д. Неттевич, Н. С. Беркутова, Л. Г. Погорелова // Селекция и семеноводство. 1983. № 1. С. 8-10. 8. Павлов, А. Н. Глиадины зерновки пшеницы в процессе их развития / А. Н. Павлов, Г. И. Колесник, И. Ф. Шаяхметов // Физиология растений. 1975. Т. 22. Вып. I. С. 80-84. 9. Перуанский, Ю. В. Биохимический контроль в селекции зерновых / Ю. В. Перуанский // Биохимические показатели селекции зерновых культур. Алма-Ата, 1986. С. 3-11. 10. Перуанский, Ю. В. Электрофоретический метод в определении биотипов сорта / Ю. В. Перуанский, Б. Т. Назиров // Селекция и семеноводство. 1981. № 3. С. 38-40. 11. Применение электрофореза белков в первичном семеноводстве зерновых культур: методические указания / Под ред. В. Г. Конарева, В. Г. Еникеева. СПб.: ВИР, 1993. 42 с. 12. Biochemical Identification of Varieties // Mater. Of III Int. Symp. ISTA ( L., 1987)/ Eds. V. Konarev, I. Gavriljuk. 1988.257 p. 13. Brinegar, A. C. (1983): Isolation and characterization of oat seed globulin and synthesis of oat seed storage proteins. Ph. D. Thesis, Univ. Wisconsin, Madison. 1995. 356 р. 14. Draper, S. R., Craig E. A. Aphenotypic classification of Wheat gliadin electrophorograms J. matu. Just. agric Bot. 1981. № 15. Р. 390 - 398. 15. Pogna, N. E., Borgli B., Mellini F. A., Dal Belin Perubbo, Nash R. J. Electrophoresis of gliadins for estimating the genetic purity in hybrid Wheat seed production // Genet agr. 1986, 40, №2. Р. 205-212. 16. Webster F. H. (1986): Oats, Chemistry and technology. AACC, Inc. St. Paul, Minnesota: 153-204. 17. Wieser H., Seilmeier W., Belitz H. D. (1980): Vergleichende Untersuchungen uber partielle Aminosauresequenzen von Prolaminen und Glutelinen verschiedener Getreidearten. I. Proteinfraktionierung nach Osborne. Z. Lebensm.-Unters. Forsch., 170: Р. 17-26. 18. Wrigley C., Bлkлs and Buschuk W. Gliadin and glutenin. The unique balance of wheat quality. AACC International, 2006. 466 р.
Похожие статьи
-
Оценка районированных сортов зерновых культур для целей сертификации семенного материала
Введение Проблема точной оценки сортового качества семенного материала является одной из наиболее актуальных в современном сельскохозяйственном...
-
Введение В настоящее время животноводство Республики Беларусь испытывает серьезные трудности с обеспечением полноценности комбикормов для...
-
Научно-методическое положение государственной кадастровой оценки земель населенных пунктов Методические указания по государственной кадастровой оценке...
-
1. В вариантах 3 и 4 наблюдается запаздывание появления всходов и наступления фазы трех пар листьев на 2-3 дня по сравнению с вариантом 1 и 2. при...
-
Таблица 2. Индивидуальные оценки диагностической чувствительности и специфичности РПИФ и ПЦР для подтверждения АЧС (WinEpiscope 2.0, Р=0,05) Вид Домашние...
-
Рынок недвижимости зависит от множества факторов, определяющих социально-экономическое развитие как страны в целом, так и отдельных регионов, в т. ч....
-
Конечной целью возделывания конопли является получение продукции - семян, тресты. Получение ее в запланированном количестве возможно лишь при...
-
Семена - Анализ деятельности сельскохозяйственного предприятия
Подготовка семян зерновых культур к посеву способствует получению лучшей всхожести и прорастанию растений, позволяет получить высокий урожай, повысить...
-
Анализ семян сельскохозяйственных культур на посевные качества осуществляется государственными семенными инспекциями по единым методам (ГОСТ 12036-85...
-
Таблица №3 Потребность в семенах и посадочном материале Наименование культуры Наименование сорта (гибрида) Площадь поля, Га Схема и способ посева,...
-
Работы по расчету кадастровой стоимости земельных участков 1-10 видов разрешенного использования осуществляются с использованием специального...
-
Атмосферное электричество представляет собой значительную опасность. Эффективным средством защиты от него является молниезащита. Она включает комплекс...
-
Анализ результатов Государственного сортоиспытания показывает обоснованность принимаемых решений по районированию новых сортов и гибридов озимых зерновых...
-
Введение С ростом продуктивности сельскохозяйственных животных проблема дефицита кормового белка с каждым годом усиливается. Основным источником его...
-
Таблица 1 Размеры положительных АЧС выборок (количества страт и животных по видам), использованные в расчетах для определения диагностической...
-
Смотри вопрос №7 Общие принципы серологических реакций и их использование в диагностике вирусных болезней В целях определения вида данного вируса при...
-
Лучшими предшественниками для конопли являются: зернобобовые, картофель, кукуруза и сахарная свекла. По данным ряда авторов для конопли предусматривается...
-
Рост и развитие конопли происходит неравномерно. Среднерусская конопля интенсивно растет от начала бутонизации до массового цветения, примерно 30-40...
-
Влияние обогащения семян медью на урожайность риса
Учитывая возможности производства зерна, каждая страна стремится, прежде всего, произвести необходимое его количество для обеспечения потребностей своего...
-
Земельные ресурсы представляют особый объект социально-экономических и общественно-политических отношений, что, в свою очередь, диктует необходимость...
-
О П А К С - 1 (7988). Допущен к использованию с 1986 года для возделывания на богарных землях Алматинской области. Метод создания - индивидуальный отбор...
-
Основной особенностью семилетнего развития эпизоотического процесса АЧС в сильно структурированном свиноводстве Российской Федерации является наблюдаемая...
-
Расчет количества яиц для цеха выращивания Инкубация - искусственное выведение цыплят из яиц. Инкубирование яиц позволяет в любые сроки и в любом объеме...
-
Корма, используемые для кормления лошадей - Кормление рабочих лошадей
Кишечник лошади физиологически предназначен для непрерывной переработки пищи, что заставляет животное постоянно потреблять корм. Эту особенность...
-
На ранних порах (1975-1990 гг.) для скрещиваний привлекали лучшие сорта селекции СНГ (преимущественно России, Украины) а также зарубежные сорта,...
-
Введение - Кормление сельскохозяйственных животных
Кормление производитель телочка рацион Знание научных основ и систем полноценного кормления животных, использование новейших достижений в области...
-
К основным параметрам, влияющим на физиологическое состояние животных, относят температуру, влажность, газовый состав атмосферы, освещенность, уровень...
-
Интенсивный путь развития коноплеводства предусматривает возделывание перспективных (высокоурожайных) сортов внедрение передовых агротехнических и...
-
Девяткин А. И. (Рациональное использование кормов) рекомендует такие способы. В первую очередь разберем способы рационального использования зеленого...
-
Таблица 12. Посевные качества семян Показатели Масса 1000 семян, г Энергия прораста-ния, % Всхо-жесть, % Семена с растений без чеканки 16 93,5 98,5...
-
Таблица 9. Агрохимические показатели экспериментального участка Название почвы Мощность пахотного слоя, см Механи-ческий состав Пахотный слой содержание...
-
Цель и задачи исследования Цель данной работы - изучение посевных качеств семян конопли при использовании их после чеканки. Цель предусматривала решение...
-
Первичная обработка Молока заключается в его очистке от механических примесей и охлаждении до 4-6 оС. Очистка молока от механических примесей. Молоко...
-
Ботанические особенности конопли Конопля относится к семейству Cannabinaceaea (коноплевые) к семейству Cannabis sativa L. Конопля является однолетним...
-
Введение - Оценка посевных качеств семян конопли при использовании их после чеканки
Конопля является одной из важнейших сельскохозяйственных культур. В сельском хозяйстве из конопли получают волокно (пеньку) и семена. Волокно благодаря...
-
Характеристика рынка недвижимости Ханты-Мансийского автономного округа В Ханты-Мансийском автономном округе рынок недвижимости развивается хорошо....
-
Расчет показателей экологической адаптивности, включающий в себя показатели пластичности и стабильности, позволил дифференцировать все сорта озимой...
-
Определение потребности в органических удобрениях для севооборотов. Потребность органических удобрений (П) равно насыщенность (Н) * площадь (S), (средняя...
-
Сегодня 70 % цифрового картографического материала создается с использованием технологии, основанной на векторизации растровых копий бумажных карт....
-
Тара для меда - Современная пасека с использованием павильонов "Берендей"
В среднем за сезон на одну пчелосемью используется 90-100% объема фляги-бидона алюминиевого объемом 38 л. Чистый вес меда во фляге 50-56кг. 40-45 фляг...
Использование белков семян овса для целей сортового контроля и идентификации