Соединения Pt (II) - Платина и ее соединения
Для Pt (II) типичны плоскоквадратные комплексы. При большом значении в октаэдрическом комплексе два электрона оказываются на сильно разрыхляющих молекулярных *d-орбиталях. Поэтому энергетически выгодней становится потеря этих электронов и переход Pt (II) в степень окисления +4 либо перерождение октаэдрического комплекса в плоскоквадратный. Распределение восьми электронов на орбиталях плоскоквадратного комплекса оказывается энергетически выгоднее, чем на молекулярных орбиталях октаэдрического комплекса. Сосредоточение восьми электронов на четырех молекулярных орбиталях определяет диамагнетизм комплексов плоскоквадратного строения.
Соединения Pt (II) интенсивно окрашены. Структурной единицей соединений Pt (II) является квадрат. Так, в кристаллах PtO (рис. 1) атомы Pt окружены четырьмя атомами кислорода по вершинам четырехугольника. Эти квадраты соединены сторонами в цепи, которые перекрещиваются под углом 90°. Аналогично построены кристаллы PtS.
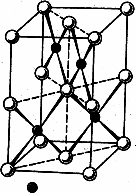
Рис. 1. Структура PtO и PtS
Дихлорид платины имеет совершенно другое строение. Красно-черные кристаллы PtCl2 состоят из октаэдрических кластерных группировок Pt6Cl12.
Хлориды платины могут быть получены прямым синтезом:
Pt + Cl2 = PtCl2 (t = 500 0C)
Pt + 2Cl2 = PtCl4 (t = 250 0C)
Дихлорид PtCl2 можно получить и диссоциацией PtCl4, а также нагреванием платинохлористоводородной кислоты:
(Н3О)2РtCl6*nH2O = PtCl2 + НС1 + (n + 2)Н2О + Cl2 (t > 300 0C)
Генетическую связь безводных хлоридов платины передает следующая схема:
370 C 475 C 581 C 583 C
PtCl4 РtC13 PtCl2 PtCl Pt
Обращает на себя внимание очень малая величина температурного интервала, разделяющего области существования хлоридов платины различного состава. Это одно из специфических свойств соединений Pt, имеющих в своей основе высококовалентную кинетически инертную химическую связь.
Оксиды и гидроксиды Pt (II) черного цвета, в воде не растворяются; PtO устойчив также по отношению к кислотам. PtS в кислотах не растворяется.
Из катионных комплексов Pt (II) очень устойчивы и легко образуются амминокомплексы [Pt(NH3)4]2+
PtCl2 + 4NH3 = [Pt(NH3)4]Cl2
Известно также большое число производных катионных комплексов Pt (II) с органическими лигандами. Еще более устойчивы тетрацианидоплатинат (II) [Pt(CN)4]2--иoны (для последнего 4=1*1041). Известен также H2[Pt(CN)4]*3H2O; в водных растворах --это двухосновная сильная кислота (называемая платиносинеродистой).
Платинаты (II) очень многообразны и устойчивы. Например, комплексные галогенйды Pt (II) характеризуются следующими константами устойчивости:
Ион... [PtCl4]2- [PtBr4]2- [PtI4]2-
Lg.... 16,0 20,5 -30
![структура k2[ptcl4]](/images/image002-4183.png)
Рис 2. Структура K2[PtCl4]
Соли М2[PtС14] (красного цвета) образуются при взаимодействии соединений Pt (II) в соляной кислоте с соответствующими солями щелочных металлов. Наиболее важны растворимые в воде K2[PtCl4] и Na2[PtCl4] (рис. 2), являющиеся исходными веществами для синтеза различных соединений платины.
Известны также соединения, в которых Pt (II) входят одновременно в состав и катиона, и аниона, например [Рt(NН3)4][РtСl4]. Это соединение (зеленого цвета) осаждается при смешении растворов [Рt(NН3)4]Сl2 и
K2[PtCl4]:
[Pt(NH3)4]Cl2 + K2[PtCl4] = [Pt(NH3)4][PtCl4] + 2KC1
Наряду с катионными и анионными комплексами весьма разнообразны нейтральные комплексы Pt (II) типа [Pt(NH3)2Х2] (где Х = С1-, Вг-, NO2-). Для соединений этого типа характерна геометрическая (цис-транс) изомерия. Например, составу [Рt(NН3)4С12] отвечают два соединения, которые отличаются свойствами, в частности окраской: цис-изомер -- оранжево-желтый, транс-изоиер -- светло-желтый. Цис - и транс-изомеры всегда имеют несколько (а иногда и сильно) различающуюся растворимость в воде, кислотах, а также кинетические и термодинамические характеристики.
В отличие от транс-изомера, цис-изомер обладает ярко выраженной противораковой физиологической активностью. Существенно различны и способы получения этих изомеров. Цис-изомер образуется при замещении двух хлорид-ионов молекулами аммиака в тетрахлороплатинат (II)-комплексе:
K2[PtCl4] + 2NH3 = [Pt(NH3)2Cl2] + 2КС1
Циc-изомер
Транc-изомер получается при замещении двух молекул аммиака на хлорид-ионы в комплексе тетрааммин-платина (II):
[Pt(NH3)4]Cl2 +2HC1 = [Pt(NH3)2Cl2] + 2NH4C1
транс-изомер
Для понимания направления течения реакций замещения лигандов в комплексах важное значение имеет принцип транс-влияния ("Поведение комплексов зависит от трансзаместителей"), установленный И. И. Черняевым (1926). Согласно этому принципу некоторые лиганды облегчают замещение лигандов, находящихся с ними в транс-положении. Таким образом, при синтезе соединений платины играет важную роль не только природа реагентов, но и порядок их смешения, временные и концентрационные соотношения: в зависимости от условий синтеза могут быть получены изомеры положения.
Трансзаместители находятся на линии (координате) проходящей через центральный атом, цисзаместители находятся как бы сбоку от центрального атома -- на линии (координате), не проходящей через центральный атом.
Экспериментально установлено, что для соединений Pt (II) транс-влияние лигандов увеличивается в ряду
Н2О < NH3 < ОН - < С1- < Br - < NCS-, I - < NO2 < СО, CN-
Принцип транс-влияния сыграл выдающуюся роль в развитии синтеза комплексных соединений.
Одним из хорошо изученных комплексов платины, носящих имя его открывателя, является соль Цейзе K[PtCl3(С2H4)]. Это окрашенное в желтый цвет соединение было синтезировано датским фармацевтом Цейзе еще в 1827г. Соль Цейзе -- одно из первых синтетически полученных металлоорганических соединений; одним из лигандов в координационной сфере платины (II) здесь является этилен (донорные свойства проявляет двойная связь Н2С==СН2).
Похожие статьи
-
Вещество [Co] Лиганды и Комплексообразователь Координационное число 6 Для комплексов с координационным числом 6 характерно октаэдрическое расположение...
-
Общая характеристика комплексов кобальта - Свойства кобальта и его комплексных соединений
Для кобальта характерно образование комплексных соединений. Так, в качестве лигандов при образовании комплексов с кобальтом часто выступают молекулы...
-
Германиевая кислота, Водородные соединения германия - Свойства германия
H4GeO4 (H2GeO3-H2O) - метагерманиевая кислота. В свободном виде (как и мономерные кислородные кислоты углерода и кремния) не получена. При подкислении...
-
Введение, Основные свойства - Платина и ее соединения
Платина - один из самых ценных благородных металлов, обладающий рядом важных свойств, благодаря которым используется не только в ювелирной...
-
При изучении реакций замещения в бензольном кольце было обнаружено, что если в нем уже содержится какой-либо заместитель, то в зависимости от его...
-
Комплексные соединения, их номенклатура, типы, строение, свойства - Основы химии
Соединения, в состав которых входят сложные ионы, существующие как в кристалле, так и в растворе, называются комплексными, или координационными. Согласно...
-
Для проверки фотоактивности и возможности управления люминесценцией гибридного соединения за счет изменения изомерного состояния органического лиганда,...
-
Соединение Магния., Неорганические соединения магния. - Химический элемент Магний
Для аналитической химии магния имеют значение его труднорастворимые и особенно внутрикомплексные (бесцветные, окрашенные или флуорисцирующие) соединения....
-
Выбор метода получения 1 способ Готовят отдельно два раствора: 9 г хлорида кобальта (II) в 25 мл воды (раствор 1) , 10 г хлорида аммония и 14 г нитрата...
-
Порфиразины с аннелированными шестичленными N - гетероциклами - пиридиновыми и пиразиновыми кольцами, среди которых первыми были синтезированы...
-
В виду того, что целью настоящей работы является синтез фталоцианинов, аннелированных гетероциклическими хинонами, получение которых предусматривает...
-
Осторожно! Яд! - Сера и ее соединения
Как известно, в природе сера часто встречается в соединениях с металлами в форме сульфидов металлов. Широко используемый в лабораториях сульфид железа...
-
На графиках 1-6 приведены построенные на основе экспериментальных данных зависимости концентрации АА и ПВ от поглощенной дозы для чистого этанола и в...
-
Синтез МФ-4 СК партии 29 с применением в качестве восстановителя боргидрида натрия был взят из диссертационной работы Черняевой [18], согласно которой...
-
Принципы получения гибридных соединений на основе квантовых точек и органических хромофоров В литературе для получения соединений, обладающих...
-
Соединения Pt (0) - Платина и ее соединения
Платина благородный катализатор окисление Как и у других d-элементов, нулевая (а также отрицательная) степень окисления у платины проявляется в...
-
Катализаторы При алкилировании ароматических углеводородов (бензол, толуол и др.) хлорпроизводными в промышленности в качестве катализатора используют...
-
Оксид кадмия CdO можно получить сжиганием металла на воздухе или в кислороде, обжигом его сульфида или термическим разложением некоторых соединений. Это...
-
Магнийорганические соединения. - Химический элемент Магний
Соединения магния с органическими кислотами. Ацетат магния Mg(CH3COO)2 - хорошо растворимое в воде соединение. Оксалат магния MgC2O4 - труднорастворимое...
-
ОСОБЫЕ СВОЙСТВА ЭЛЕМЕНТА И ЕГО СОЕДИНЕНИЙ, ИХ ПРИМЕНЕНИЕ. - Галлий
Не стоит брать этот элемент в руки - тепла человеческого тела достаточно, чтобы этот серебристый мягкий (его можно резать ножом) металл превратился в...
-
Химические свойства алюминия и его соединений - Алюминий и его свойства
Алюминий легко взаимодействует с кислородом при обычных условиях и покрыт оксидной пленкой (она придает матовый вид). I. Взаимодействие с простыми...
-
Важнейшие строительные материалы и их соединения - Химия в строительстве
Большинство строительных материалов представляют собой смеси разнообразных химических соединений, которые, в свою очередь, состоят из химических...
-
Оптически активные соединения с одним асимметрическим атомом Рис.1. Энантиомерыбутанола-2 При рассмотрении пространственной модели бутанола-2 (рис.1.)...
-
Электронные пары, Ионная связь, Соединения металлов - Химия в строительстве
Некоторые химические элементы, атомы которых укомплектованы на электронных орбитах 8 электронами, не склонны вступать в соединения с другими элементами....
-
Маслорастворимые молибденсодержащие органические соединения - Молибденсодержащие присадки
В последние годы особый интерес вызывают маслорастворимые молибденсодержащие органические соединения; они не только снижают износ при трении, но и...
-
Окисление сахара хлоратом калия На двух кафельных плитках смешать по лопаточке растертого сахара и бертолетовой соли. Поднести к одной смеси горящую...
-
Выводы - Свойства нейтральной формы гибридного соединения
1. Отработана методика синтеза гибридного соединения QD-L на основе квантовой точки CdS (QD) и фотоактивного лиганда -...
-
Рассмотрим теперь, какое влияние на свойства веществ оказывает порядок соединения атомов в молекуле. Обратимся сначала к историческим фактам. Изучая...
-
Фотолиз гибридного соединения QD-L в кислой среде - Свойства нейтральной формы гибридного соединения
Для проверки фотоактивности и возможности управления люминесценцией протонированной формы гибридного соединения при помощи облучения светом с различными...
-
Гибридные системы на основе квантовых точек (КТ) и органических лигандов могут быть использованы в качестве хемо-, био - и фотосенсоров, а также...
-
На графиках 7-14 приведены построенные на основе экспериментальных данных зависимости концентрации АА и ПВ от поглощенной дозы для чистого этанола и в...
-
ЗАКЛЮЧЕНИЕ, БИБЛИОГРАФИЧЕСКИЙ СПИСОК - Свойства кобальта и его комплексных соединений
Проведен литературный обзор. Изучены физические и химические свойства кобальта и его комплексных соединений. Исследованы способы получения кобальта и его...
-
Комплексные соединения - соед-я, обр-ся сочетанием нескольких, способных к существованию ионов, сост. из атома в опр. валентном сост-ии, связ. с одной...
-
Кислоты и их соли - Фосфор и его соединения
А) Фосфористая кислотаH3PO3. Безводная фосфористая кислота Н3РО3образует кристаллы плотностью 1,65 г/см3, плавящиеся при 74°С. Структурная формула: При...
-
Или N экв.1=n экв.2 для газообразных ве-в наряду с понятием молярного V (22,4 моль/л), исп-ся понятие - молярный объем эквивалента-это V одного моль...
-
Соединения мышьяка со степенью окисления -3 Мышьяковистый водород (арсин) AsH 3 . Бесцветный, очень ядовитый газ с чесночным запахом. tПл=-113ОС [1],...
-
Б-Гидроксиэтильные радикалы, возникающие при радиолизе этанола, являются одними из простейших представителей монофункциональных б-ГУР. В настоящей работе...
-
Применение кобальта и его комплексных соединений - Свойства кобальта и его комплексных соединений
Кобальт в виде порошка используют в основном в качестве добавки к сталям. При этом повышается жаропрочность стали, улучшаются ее механические свойства...
-
Синтез гетероциклических соединений Синтез 4-амино-1,2-бензотиазола К раствору 5-8 г (31 ммоль) 2,6-диметилтолуола в 15 мл мезителена (температура...
-
Полимеры в машиностроении - Полимерные соединения
Ничего удивительного в том, что эта отрасль - главный потребитель чуть ли не всех материалов, производимых в нашей стране, в том числе и полимеров....
Соединения Pt (II) - Платина и ее соединения