Теорія електролітичної дисоціації - Теория электролитической диссоциации
Більшість хімічних реакцій, які використовуються у якісному аналізі, протікають у водних розчинах. Якщо речовина розчиняється у воді чи іншому розчиннику, то утворюється однорідний гомогенний розчин. Розчини не можна розглядати як прості механічні суміші. Процес розчинення завжди супроводжується виділенням чи поглинанням теплоти.
Водні розчини деяких речовин є провідниками електричного струму. Ці речовини належать до електролітів. Електролітами є кислоти, солі та луги. Багато речовин виявляють властивості електролітів у розплавленому стані. Електрична провідність розчинів і розплавів електролітів зумовлена наявністю у розчині негативно та позитивно заряджених іонів, які утворюються з молекул або кристалічних речовин. Уявлення про утворення іонів у розчинах електролітів утвердилося в хімії в першій половині XIX ст. завдяки працям англійського фізика і хіміка М. Фарадея. Процес розщеплення електролітів на іони у водних розчинах і розплавах називається електролітичною дисоціацією. Розчини деяких речовин у воді не проводять електричний струм. Такі речовини називаються неелектролітами. Неелектролітами є багато органічних сполук, наприклад сахари, спирти.
Теорія електролітичної дисоціації для водних розчинів була сформульована шведським ученим С. Арреніусом у 1887 р. Розглянемо основні положення цієї теорії.
При розчиненні у воді молекули електролітів дисоціюють (розщеплюються) на позитивно і негативно заряджені іони. Іони можуть бути утворені з одного атома - прості іони ( Na+, Cl- ) і кількох атомів - складні іони ().
Дисоціація - оборотний процес. Як правило, він не відбувається до кінця, а в системі встановлюється динамічна рівновага, тобто такий стан, при якому швидкість дисоціації дорівнює швидкості зворотного процесу - утворення вихідних молекул. Тому у рівняннях дисоціації замість знака " дорівнює " ставлять знак оборотності, наприклад:
Іони у водному розчині перебувають у хаотичному безперервному русі. Якщо у розчин електроліту занурити електроди і прикласти до них електричну напругу, то іони набудуть направленого руху: позитивно заряджені іони переміщуватимуться у напрямі до катода (негативно зарядженого електрода), а негативно заряджені іони у напрямку анода (позитивно зарядженого електрода). Іони також одержали назви: позитивні іони - аніони, а негативні - катіони.
Теорія С. Арреніуса не пояснює причин електролітичної дисоціації, вони були встановлені пізніше.
Розглянемо електролітичну дисоціацію речовин з іонним і полярним ковалентним зв'язком. Припустимо, що у воду помістили кристали хлориду натрію NаСІ - речовини з іонним зв'язком. Полярні молекули води електростатично притягуються позитивно зарядженими кінцями до негативно заряджених іонів С1- у хлориді натрію, а не-гативно зарядженими кінцями - до позитивно заряджених іонів Na+ ( див. рис. 1 ).
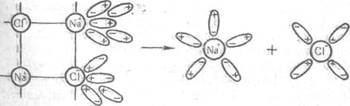
Рис. 1. Схема дисоціації хлориду натрію у водному розчині
Внаслідок такої взаємодії іонів з диполями води послаблюється зв'язок між іонами кристала, і вони переходять у розчин у вигляді гідратованих іонів. Уявлення про гідратацію іонів, тобто про виникнення хімічного зв'язку між іонами і молекулами води, введено російським вченим І. О. Каблуковим і стало розвитком хімічної теорії розчинів.
У неводних розчинниках також можлива електролітична дисоціація з утворенням соль ватованих іонів.
Гідратації зазнають всі іони у водних розчинах, у тому числі й іони водню, які можуть утворювати хімічні зв'язки з однією, двома і більшим числом молекул води. Звичайно гідратовані іони водню зображують формулою Н3О+ ( точніше, Н3О+ Ч nН2О, де n = 0...4 ) і називають іоном гідроксонію.
На рис. 2 зображено схему розщеплення молекули хлороводню з полярним ковалентним зв'язком. При взаємодії полярної молекули НС1 з диполями води відбувається розрив зв'язку між атомами водню і хлору, і молекула набуває іонної структури. Потім молекула із іонним зв'язком розщеплюється на окремі гідратовані іони.
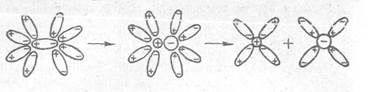
Рис. 2 Схема дисоціації молекули хлороводню у водному розчині
Для кількісної характеристики електролітичної дисоціації введено поняття ступінь дисоціації, який дорівнює відношенню кількості речовини електроліту, що розщепився на іони, до загаль-ної кількості речовини цього електроліту, введеного в розчин:
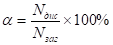
Ступінь дисоціації - безрозмірна величина, його виражають у частках одиниці або в процентах. При повній дисоціації електроліту на іони щ= 1, або 100 %. Для неелектролітів, які не дисоціюють на іони, щ = 0.
Ступінь дисоціації залежить від концентрації електроліту і температури. З теорії електролітичної дисоціації випливає, що чим менша концентрація електроліту в розчині, тим більший ступінь дисоціації. При безкінечному розбавлянні розчину ступінь дисоціації наближається до 1 (100 %). Наприклад, ступінь дисоціації гідроксиду натрію NаОН залежно від концентрації електроліту змінює-ться так: для розчину з концентрацією с=1 моль/л щ = 0,73 (18°С), для с = 0,1 моль/л щ =0,84 і для с = 0,01 моль/л щ = 0,95.
Залежно від ступеня електролітичної дисоціації всі електроліти поділяють на сильні та слабкі. Такий поділ досить умовний, оскільки ступінь дисоціації залежить від температури розчину, концентрації електроліту, і внаслідок цього може змінюватися у досить широких межах.
Слабкі електроліти - це речовини, які лише частково дисоціюють на іони. Із неорганічних сполук до них належить вода, пероксид водню, деякі неорганічні кислоти, як, наприклад, вугільна Н2СО3. Силу електроліта зручно характеризувати за допомогою константи дисоціації:
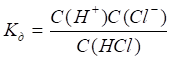
Якщо електроліт дисоціює ступінчато, то константу дисоціації слід записати для кожного ступеня дисоціації. Виходячи із значень константи дисоціації можна визначати та порівнювати силу електролітів, чим менше КД тим електроліт слабший і навпаки.
Для слабких електролітів між константою та ступенем дисоціації існує зв'язок, який для розбавлених розчинів можна виразити формулою:
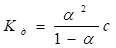
,
Де с - молярна концентрація електроліту.
Сильні електроліти практично повністю дисоційовані на іони. До них відносять майже всі неорганічні кислоти ( сульфатна, нітратна, хлоридна ) та їх розчинні солі, луги.
Електростатична взаємодія із утворенням іонних пар зменшує реальну концентрацію іонів у розчині, а отже ступінь дисоціації електроліту менший за 100 %. Ступінь дисоціації сильного електроліту. Який визначають експериментально називають уявним ступенем дисоціації. Тому замість концентрації використовують активність. Активність - це ефективна концентрація іонізованої частини електроліту в розчині, визначена із врахуванням взаємодії іонів: , де - це коефіцієнт активності речовини, який враховує сили взаємодії іонів, значення, якого завжди менше або дорівнює одиниці.
П. Дебай та Г. Гюккель встановили, що в розведених розчинах сильних електролітів логарифм коефіцієнта активності пропорційний кореню квадратному із його іонної сили: , де А - це стала, яка залежить від зарядів іонів, температури та діелектричної проникності розчинів. Поняття про іонну силу розчину ввели Г. Люїс та Рендель. Згідно із законом іонної сили коефіцієнт активності в розбавлених розчинах залежить не від природи електроліту, а тільки від величини іонної сили розчину. У різних електролітів із однаковими значеннями іонної сили коефіцієнти активності будуть однакові.
Величина іонної сили І визначається як напівсуха добутків концентрацій іонів С на квадрати їх валентностей z:
Похожие статьи
-
В аналітичній хімії більшість хімічних реакцій проводять у розчинах. Для вираження вмісту аналізованої речовини у розчинах використовують поняття...
-
Рівняння дисоціації кислот, лугів і солей - Дисоціація
Електролітичну дисоціацію виражають рівняннями, як і будь-які інші хімічні реакції. Записуючи ці рівняння, звичайно не зазначають формул молекул води,...
-
Рівняння дисоціації кислот, лугів і солей - Електролітична дисоціація солей та лугів
Електролітичну дисоціацію виражають рівняннями, як і будь-які інші хімічні реакції. Записуючи ці рівняння, звичайно не зазначають формул молекул води,...
-
ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ - Характеристика основных видов растворов
Все вещества по способности в растворе или в расплавленном состоянии проводить электрический ток можно подразделить на две группы: электролиты и...
-
Електролітична дисоціація солей та лугів - Електролітична дисоціація солей та лугів
Розпад електролітів на іони під час розчинення у воді або розплавлення називається електлолітичною дисоціацією. Розглянемо розчинення у воді такої,...
-
Комплексные соединения - соед-я, обр-ся сочетанием нескольких, способных к существованию ионов, сост. из атома в опр. валентном сост-ии, связ. с одной...
-
ТЕМПЕРАТУРА - Основные положения молекулярно-кинетической теории, ее опытные обоснования
Любое макроскопическое тело или группа макроскопических тел называется термодинамической системой. Тепловое или термодинамическое равновесие - такое...
-
Властивості розчинників електролітів - властивості іонів. - Дисоціація
Хлор отруйний, а в міру посолена їжа, крім користі, нашому організму не приносить. Але проста речовина Na складається з атомів натрію, а проста речовина...
-
Електролітична дисоціація солей та лугів - Дисоціація
Розпад електролітів на іони під час розчинення у воді або розплавлення називається електлолітичною дисоціацією. Розглянемо розчинення у воді такої,...
-
Моделирование в условиях противодействия, игровые модели - Основы теории систем и системного анализа
Как уже неоднократно отмечалось, системный анализ невозможен без учета взаимодействий данной системы с внешней средой. Ранее упоминалась необходимость...
-
Кинетическая теория вещества - Строение и превращение веществ
Движением атомов и молекул с давних пор уже пытались объяснить тепловые явления. Параллельно с развитием этого, несомненно, существовавшего общего...
-
Модели теории игр. Основные определения и термины В разных областях целенаправленной деятельности, например при разработке и эксплуатации АСУ, часто...
-
Следствия теоремы, Послесловие к доказательству - Об одной теореме теории чисел
Не существует ЦЕЛЫХ чисел, для которых выполняется равенство (1). При четных значениях показателя степени уравнение вида (1) идентично как для...
-
Прогностическая сила - Базовые результаты математической теории классификации
С целью поиска приемлемого показателя качества диагностики рассмотрим восходящую к Р. Фишеру [20] широко известную параметрическую вероятностную модель...
-
Часто используют такой показатель качества алгоритма диагностики, как "вероятность (или доля) правильной классификации (диагностики)" [12, 13] - чем этот...
-
Основные понятия теории экономико-математического моделирования Кибернетический подход к исследованию экономико-математических систем Обычно...
-
В ряде случаев в экономической практике возникает потребность расчета среднего размера признака, выраженного в квадратных или кубических единицах...
-
Контрольная работа По дисциплине: Теория вероятностей Контрольная работа № 1 Вариант 1 Задача № 1 Условие: Из 10 изделий, среди которых 4 бракованные,...
-
Модель в общем смысле (обобщенная модель) есть создаваемый с целью получения и (или) хранения информации специфический объект (в форме мысленного образа,...
-
В современной экономической теории доминирующую роль играют труды зарубежных экономистов. Однако русская экономическая наука также ярко представлена...
-
Теория вероятностей и математическая статистика
Задача 1 Малое предприятие имеет два цеха - А и В. Каждому установлен месячный план выпуска продукции. Известно, что цех А свой план выполняет с...
-
Зарождение современной химии, Теория флогистона и система Лавуазье - Химия сегодня
Представления древнегреческих натурфилософов оставались основными идейными истоками естествознания вплоть до XVIII в. До начала эпохи Возрождения в науке...
-
Средняя арифметическая Средней арифметической величиной называется такое среднее значение признака, при вычислении которого общий объем признака в...
-
"Квантовая химия" Квантовая химия - область теоретической химии, в которой вопросы строения и реакционной способности химических соединений, химические...
-
Основная теория сезонности временного ряда - Методы изучения сезонных колебаний. Примеры расчетов
Основными составляющими временного ряда являются тренд и сезонная компонента. Составляющие этих рядов могут представлять собой либо тренд, либо сезонную...
-
Методы непараметрической статистики - Основы теории систем и системного анализа
Использование классических распределений случайных величин обычно называют "параметрической статистикой" - мы делаем предположение о том, что...
-
Електролітична дисоціація кислот - Електролітична дисоціація солей та лугів
Між атомами в молекулах кислот, наприклад, соляної HCl, сірчаної H2SO4, азотної HNO3, фосфорної H3PO4 існують полярні ковалентні зв'язки. Розглянемо...
-
Їдкі луги - Натрій: історія, властивості
Їдкими лугами називаються добре розчинні у воді гідроксиди. Найважливіші з них NaOH і KOH. Гідроксид натрію - білий, непрозорий, тверда кристалічна...
-
ПОНЯТТЯ ПРО АЛОТРОПІЮ. ОЗОН - Неметали та їхні сполуки
Хімічні елементи у вільному стані існують у формі простих речовин. Так, елемент Оксиген утворює дві прості речовини - кисень О2 та озон О3. Озон. Якщо на...
-
Гідроліз солей - Електролітична дисоціація солей та лугів
Як вам відомо, солі утворюються в результаті нейтралізації кислот і основ. Можна припустити, що розчин солей на відміну від розчинів кислот і лугів,...
-
Електролітична дисоціація кислот - Дисоціація
Між атомами в молекулах кислот, наприклад, соляної HCl , сірчаної H 2 SO 4 , азотної HNO 3 , фосфорної H 3 PO 4 існують полярні ковалентні зв'язки....
-
ПОНЯТТЯ ПРО АЛОТРОПІЮ. ОЗОН - Загальні відомості про елементи
Хімічні елементи у вільному стані існують у формі простих речовин. Так, елемент Оксиген утворює дві прості речовини -- кисень О2 та озон О3. Озон. Якщо...
-
Растворы - термодинамические устойчивые системы переменного состава, состоят не менее чем из двух компонентов и продуктов их взаимодействия. Это...
-
Теория оптической изомерии - Оптические изомеры и их влияние на организм человека
Работа Пастера, доказывающая возможность "расщепления" оптически неактивного соединения на антиподы - энантиомеры, первоначально вызвала у многих химиков...
-
Анализ систем массового обслуживания с отказами. А) Задана многоканальная СМО с отказами. Она имеет состояния: - в СМО нет ни одной заявки; - в СМО...
-
СМО с очередью - Теория массового обслуживания
В качестве показателей эффективности СМО с ожиданием, кроме уже известных показателей -- абсолютной A и относительной Q пропускной способности,...
-
Теория массового обслуживания - теория, которая изучает статистические закономерности в массовых операциях, состоящих из большого числа однородных...
-
Пожары и взрывы причиняют значительный материальный ущерб, в ряде случаев вызывают тяжелые травмы и гибель людей. Ущерб от пожаров и взрывов в...
-
Моделирование системы в условиях неопределенности - Основы теории систем и системного анализа
Как уже отмечалось в первой части нашего курса, в большинстве реальных больших систем не обойтись без учета "состояний природы" -- воздействий...
-
Растворы электролитов. Диссоциация кислот, солей и оснований - Основы химии
Электролиты - вещества, которые при растворении подвергаются диссоциации на ионы. В результате раствор приобретает способность проводить электрический...
Теорія електролітичної дисоціації - Теория электролитической диссоциации