Водородные соединения, Водородная связь - Свойства водорода
В этой таблице слева легкой тенью выделены клетки элементов, образующих с водородом ионные соединения - гидриды. Эти вещества имеют в своем составе гидрид-ион Н-. Они представляют собой твердые бесцветные солеобразные вещества и реагируют с водой с выделением водорода.
Элементы главных подгрупп IV-VII групп образуют с водородом соединения молекулярного строения. Иногда их также называют гидридами, но это некорректно. В их составе нет гидрид-иона, они состоят из молекул. Как правило, простейшие водородные соединения этих элементов - бесцветные газы. Исключения - вода, являющаяся жидкостью, и фтороводород, который при комнатной температуре газообразен, но при нормальных условиях - жидкость.
Темными клетками отмечены элементы, образующие с водородом соединения, проявляющие кислотные свойства.
Темными клетками с крестом обозначены элементы, образующие с водородом соединения, проявляющие основные свойства.
Водородная связь
Водородная связь, строго говоря, не является химической связью. Это - очень сильное межмолекулярное взаимодействие.
Где образуется водородная связь?
Один из атомов, образующих водородную связь, очевидно, водород. Но не любой атом водорода, а только связанный с каким-то из трех наиболее электроотрицательных атомов - F, O, N. Соответственно, второй атом, образующий водородную связь - атом F, O или N, НЕ связанный с данным атомом водорода ковалентной связью (как правило, атом из соседней молекулы).
Как образуется водородная связь?
Атомы F, O, N настолько сильно смещают к себе общую электронную пару, что ковалентная связь F-H, O-H, N-H становится ОЧЕНЬ полярной. Частичные отрицательные заряды, возникающие на атомах Н (+) и F, O, N (-) настолько велики, что притяжение между + одной молекулы и - соседней молекулы приближается по энергии к химической связи. Это притяжение и формирует водородную связь, показанную на рисунке точечной линией.
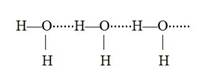
Такое дополнительное связывание между молекулами приводит, в частности, к аномально высоким температурам плавления и кипения веществ, имеющих водородную связь. Например, вода кипела бы при температуре около -70ОС, если бы не было водородных связей. Наличие водородных связей приводит также к повышению теплоемкости. Из-за высокой теплоемкости ночью вода остывает медленно, а днем так же медленно нагревается (наверное, некоторые замечали, что утром вода холоднее песка на пляже, а ночью -- теплее). Медленно остывая осенью, постепенно отдавая аккумулированное тепло, и медленно нагреваясь весной, водные массы смягчают переход от лета к зиме и от зимы к лету (в местностях, примыкающих к морям, и на островах более мягкий и "смазанный" климат, чем контрастный климат центральных областей материков).
Похожие статьи
-
Химическая связь - это взаимное сцепление атомов в молекуле и кристаллической решетке в результате действия между атомами электрических сил притяжения....
-
Свойства азота - Азот, его соединение и свойства. Азот в природе
Всем известно: азот инертен. Часто мы сетуем за это на элемент № 7, что естественно: слишком дорогой ценой приходится расплачиваться за его относительную...
-
Винилхлорид -- достаточно активное химическое соединение, чьи химические свойства определяются как наличием двойной связи, так и атома хлора. Наибольший...
-
Строение, физические свойства, значение воды - Свойства водорода
Вода -- самое распространенное соединение водорода. Общая масса воды на нашей планете около 1,4*1018 т. Вода -- это единственное вещество, все три...
-
Водород - двухатомный газ Н2. Он не имеет ни цвета, ни запаха. Это самый легкий газ. Благодаря этому свойству он использовался в аэростатах, дирижаблях и...
-
Рассмотрим теперь, какое влияние на свойства веществ оказывает порядок соединения атомов в молекуле. Обратимся сначала к историческим фактам. Изучая...
-
Соединения и их свойства, Оксиды алюминия - Алюминий и его свойства
Оксиды алюминия Оксид алюминия образует несколько полиморфных разновидностей, или форм, имеющих одинаковый химический состав, различное строение...
-
Свойства и важнейшие характеристики. - Полимерные соединения
Линейные полимеры обладают специфическим комплексом физико-химических и механических свойств. Важнейшие из этих свойств: способность образовывать...
-
ВВЕДЕНИЕ, СТРОЕНИЕ МОЛЕКУЛ И СВОЙСТВА ВОДЫ - Химические свойства и строение воды
Вода - ценнейший природный ресурс. Вода играет исключительную роль в процессах обмена веществ, составляющих основу жизни. Огромное значение вода имеет в...
-
Химические свойства алюминия и его соединений - Алюминий и его свойства
Алюминий легко взаимодействует с кислородом при обычных условиях и покрыт оксидной пленкой (она придает матовый вид). I. Взаимодействие с простыми...
-
Основы новой теории сформулировал 1861 г. профессор Казанского университета Александр Бутлеров. В химии к тому времени уже значительное распространение...
-
Предмет органической химии. Изучая неорганическую химию, мы знакомились с веществами самого разнообразного состава и при этом ни разу не встречали, чтобы...
-
Химические свойства. Образование ковалентной связи по донорно-акцепторному механизму - Аммиак
1. Аммиак - основание Льюиса. Его раствор в воде (аммиачная вода, нашатырный спирт) имеет щелочную реакцию (лакмус - синий; фенолфталеин - малиновый)...
-
Периодический закон химических элементов: свойства химических элементов, а также простых и сложных веществ, ими образуемых, находятся в периодической...
-
Вода реагирует с некоторыми кислотными и основными оксидами, давая гидроксид - соответственно кислоту или основание: Н2О + CaO = Ca(OH)2 основание H2O +...
-
Молекулярные кристаллы фуллеренов -- полупроводники, однако в начале 1991 г. было установлено, что легирование твердого С60 небольшим количеством...
-
Взаимодействие водорода со сложными веществами, Получение водорода - Свойства водорода
Водород проявляет восстановительные свойства и в реакциях со сложными веществами: 1) Восстановление оксидов металлов, стоящих в электрохимическом ряду...
-
Технологические свойства метанола Метанол (метиловый спирт) СН3ОН представляет бесцветную легкоподвижную жидкость с температурой кипения 64,65°С,...
-
Разработав теорию и подтвердив правильность ее синтезом новых соединений, А. М. Вутлеров не считал теорию абсолютной и неизменной. Он утверждено, что она...
-
А) Углерод (С), кремний (Si), германий (Ge), олово (Sn), свинец (РЬ) - элементы 4 группы главной подгруппы ПСЭ. На внешнем электронном слое атомы этих...
-
Соединения азота - Азот, его соединение и свойства. Азот в природе
Из почвы соединения азота попадают в растения. Далее: "лошади кушают овес", а хищники -- травоядных живот-ных. По пищевой цепи идет круговорот вещества,...
-
Комплексные соединения, их номенклатура, типы, строение, свойства - Основы химии
Соединения, в состав которых входят сложные ионы, существующие как в кристалле, так и в растворе, называются комплексными, или координационными. Согласно...
-
Химическая связь и строение молекул вещества. - Роль химии в повседневной жизни
Атомистические воззрения возникли первоначально на Древнем Востоке, в античных Греции и Риме. Первоначально атомное учение предполагало существование...
-
Выводы - Свойства нейтральной формы гибридного соединения
1. Отработана методика синтеза гибридного соединения QD-L на основе квантовой точки CdS (QD) и фотоактивного лиганда -...
-
1. В результате линейной комбинации две атомные орбитали (АО) формируют две молекулярные орбитали (МО) - связывающую, энергия которой ниже, чем энергия...
-
Оксид кадмия CdO можно получить сжиганием металла на воздухе или в кислороде, обжигом его сульфида или термическим разложением некоторых соединений. Это...
-
ОСОБЫЕ СВОЙСТВА ЭЛЕМЕНТА И ЕГО СОЕДИНЕНИЙ, ИХ ПРИМЕНЕНИЕ. - Галлий
Не стоит брать этот элемент в руки - тепла человеческого тела достаточно, чтобы этот серебристый мягкий (его можно резать ножом) металл превратился в...
-
Реагирует с неметаллами: 4Al + 3O2 > 2Al2O3 ; 2Al + 3Br2 > 2AlBr3 c оксидами металлов:2Al + Fe2O3 > Al2O3 + 2Fe (алюмотермия)c водой (если...
-
Принципы получения гибридных соединений на основе квантовых точек и органических хромофоров В литературе для получения соединений, обладающих...
-
Спектральные свойства нейтральной формы гибридного соединения QD-L На рис. 28 представлены спектры поглощения растворов исходных квантовых точек CdS...
-
Оборудования, используемые для определения ртути Класс опасности - 1, ПДК в населенных пунктах (среднесуточная) -- 0,0003 мг/мі ПДК в жилых помещениях...
-
Введение - Свойства нейтральной формы гибридного соединения
Гибридный фотохромный хемосенсор лиганд Материалы, обладающие контролируемой люминесценцией, востребованы в настоящее время в различных областях науки и...
-
Химические свойства Бора. - Третья группа периодической системы
Химически Бор при обычных условиях довольно инертен (взаимодействует активно лишь с фтором), причем кристаллический Бор менее активен, чем аморфный. С...
-
Сплавы. Применение алюминия и его соединений - Алюминий и его свойства
5 .1 Сплавы алюминия Алюминий всех марок содержит более 99% чистого алюминия. В зависимости от химического состава он подразделяется на алюминий особой,...
-
Фотолиз гибридного соединения QD-L в кислой среде - Свойства нейтральной формы гибридного соединения
Для проверки фотоактивности и возможности управления люминесценцией протонированной формы гибридного соединения при помощи облучения светом с различными...
-
Заключение - Азот, его соединение и свойства. Азот в природе
Проделанная работа позволяет сделать вывод о том, что азоту принадлежит одна из главных ролей среди многочисленных химических элементов. Для человечества...
-
Свойства связей и отношений - Системная революция и принцип дуального управления
Отвлекаясь от конкретного содержания реальных связей и отношений, можно выделить три наиболее общих группы синтаксических свойств бинарных связей и...
-
Спектральные свойства протонированной формы гибридного соединения QD-L На рис. 34 представлены спектры поглощения квантовой точки CdS (QD), лиганда (LH)...
-
Для проверки фотоактивности и возможности управления люминесценцией гибридного соединения за счет изменения изомерного состояния органического лиганда,...
-
Введение, История открытия азота - Азот, его соединение и свойства. Азот в природе
Целью данной работы является изучение и анализ химического элемента - азота. Азот - это бесцветный газ, без вкуса и запаха. Один из самых...
Водородные соединения, Водородная связь - Свойства водорода