Синтезы на основе ацетилена - Анализ и технологическая оценка химического производства
Ацетилен СН=СН -- газ, легко вступающий в самые различные химические реакции с образованием многочисленных соединений, используемых при получении волокон, каучуков, смол и т. д. Например, из ацетилена получают ацетальдегид, этиловый спирт, бутадиен, этил-ацетат, хлористый винил, винилацетат, хлоропрен, акрилонитрил и др. Он используется для получения высоких температур (3200° С) при сварке и резке металлов.
Ацетилен получают путем обработки карбида кальция водой (СаС2 + 2Н2О ->Са(ОН)2 + С2Н2) или путем термоокислительного крекинга при 1400--1500С различных углеводородов (СН4, С2Н4 и до.)
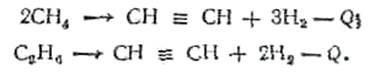
Для примера рассмотрим синтез ацетальдегида на основе ацетилена.
Ацетальдегид СНзСНО -- альдегид уксусной кислоты, летучая жидкость с резким запахом, хорошо смешивается с водой и спиртом. Он используется для получения уксусной кислоты.
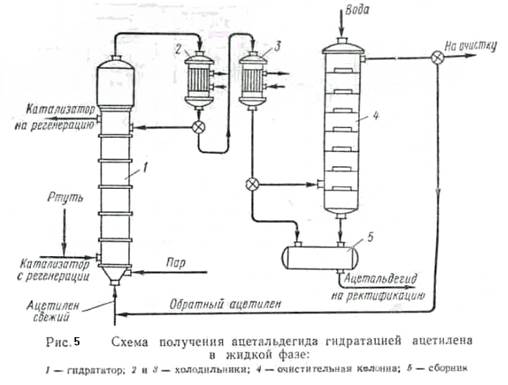
В промышленности ацетальдегид по одной из схем (рис.5) получают следующим образом. Очищенный от примесей ацетилен, смешанный с циркуляционным газом, непрерывно подается в гидрататор 1, в котором находится нагретая до 80--100° С жидкость, содержащая сульфаты железа и ртути (в 1 Л Н2О 200 е H2S04, 0,4 Г Hg, 40 Г окислов железа). Ацетилен, барботируя через жидкость, переходит в ацетальдегид по реакции:
СН = СН + Н2О --> СНзСНО + 1416 Кдж.
Степень перехода ацетилена в ацетальдегид составляет 50--60%. Газы, содержащие ацетальдегид, ацетилен и примеси, поступают на охлаждение сначала в холодильник 2, где частично конденсируются пары воды, и конденсат возвращается в гидрататор 1, а затем в холодильник 3, где конденсируются пары ацетальдегида и воды, собираемые в сборнике 5 и направляемые на ректификацию (на схеме не показано).
Газы, содержащие ацетилен, поступают в колонну 4, орошаемую водой, где из них извлекаются остатки ацетальдегида, и снова возвращаются в процесс. Для очистки оборотного газа от окислов углерода и азота часть его (10%) непрерывно отбирается из цикла и направляется на очистку. Выход ацетальдегида составляет примерно 96% от теоретического. Так как пары ртути и ее соединения ядовиты, начинают применяться не ртутные катализаторы в виде окислов Zn, Mg, Ni, Со, Cr.
Уксусная кислота находит применение в текстильной, фармацевтической, парфюмерной промышленности, для получения сложных эфиров, в производстве ацетилцеллюлозы, уксусного ангидрида, ацетона, ацетатного шелка, каучука, пластических масс и т. д.
Раньше кислоту получали сухой перегонкой древесины, брожением этанола, а в настоящее время -- окислением ацетальдегида или гидратацией кетона.
Окисление ацетальдегида кислородом воздуха происходит в присутствии солей марганца при темпеатуре 60--70° С. Так как надуксусная кислота может взрываться, то парогазовая смесь разбавляется азотом. Образование СНзСООН идет по следующей схеме:
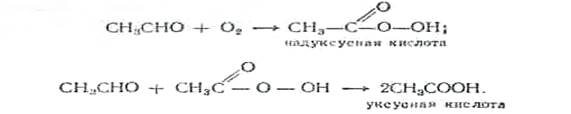
Для очистки от примесей синтетическую кислоту подвергают перегонке. Техническая кислота после перегонки содержит 97--99% СНзСООН, 0,1--0,5% НСООН, 0,5--2% Hp.
Безводная уксусная кислота плотностью 1049 Кг/м3 (20 С) застывает при 16,6° С, кипит при 118,1° С. Она хорошо смешивается с Во" Дои и многими органическими жидкостями. При попадании на кожу вызывает ожоги.
Похожие статьи
-
Производство азотной кислоты - Анализ и технологическая оценка химического производства
Безводная азотная кислота HNO3--тяжелая бесцветная жидкость плотностью 1520 Кг/м 3 (при 15° С). Она замерзает при температуре --47° С и кипит при 85°С,...
-
Подготовка угля к коксованию - Анализ и технологическая оценка химического производства
Коксование-- Процесс сухой перегонки каменных углей при их нагревании до 900--1050° С без доступа воздуха. В результате сложных физических и химических...
-
Технология производства соляной кислоты - Анализ и технологическая оценка химического производства
Соляная кислота--бесцветная жидкость, представляющая собой раствор хлористого водорода в воде. Она энергично растворяет многие металлы и их окислы. В...
-
Производство пластмасс - Анализ и технологическая оценка химического производства
Пластические массы делят на простые (ненаполненные) и сложные (композиционные). Основу пластических масс составляет высокомолекулярное соединение --...
-
Производство полимеров - Анализ и технологическая оценка химического производства
Высокомолекулярные соединения получают из мономеров полимеризацией, сополимеризацией, поликонденсацией и методами привитой полимеризации и...
-
Таблица 2 - Структура сырья в производстве метанола, %. Сырье В мире Беларусь и Россия Природный газ 73,8 70,7 Нефть и нефтепродукты 24,4 4,0 Отходы...
-
Получение синтезированного газа - Анализ и технологическая оценка химического производства
Химические методы переработки нефти проводят при высоких температурах без катализатора (термический крекинг), при высоких температурах в присутствии...
-
Производство химических волокон - Анализ и технологическая оценка химического производства
Волокнами называют тела, длина которых во много раз превышает очень малые (микроны) размеры их поперечного сечения. По происхождению волокна делят на...
-
МАЗЕВЫЕ ОСНОВЫ, ЛИПОФИЛЬНЫЕ ОСНОВЫ - Производство мазей
Основа в составе мази является активным носителем лекарственного вещества, влияющим на фармакокинетическую активность, консистентные свойства мази и ее...
-
Метанол -- сырье для многих производств органического синтеза. Основное количество его расходуется на получение формальдегида. Он служит промежуточным...
-
Этот способ концентрирования обеспечивает получение чистой концентрированной азотной кислоты без вредных выбросов в атмосферу. Однако у него есть ряд...
-
В 1960-х годах разработан агрегат по производству азотной кислоты мощностью 120 тыс. т год под давлением 0,716 МПа с использованием высокотемпературной...
-
Процесс получения винилхлорида сбалансированным методом из этилена состоит из шести стадий: 1. синтез 1,2-дихлорэтана прямым жидкофазным хлорированием...
-
Один из способов повысить селективность - это правильно подобрать катализатор. Рассмотрим этот метод, на примере получения анизола и крезола. Анизол и...
-
Еще в начале 20 века было установлено, что при взаимодействии СО и Н2 в присутствии соответствующих катализаторов можно получить углеводороды. Так, в...
-
Данные для расчета: Основная реакция: (1) Побочные реакции: Рабочий объем катализатора - 24 м3. Расход оксида углерода и метанола на побочные продукты с...
-
Система усовершенствованных моделей позволяет удовлетворительно воспроизводить кинетику СО-токсичности ДВС при изменении нагрузки, цикловой подачи...
-
Бромистый этил представляет бесцветную прозрачную жидкость, обладающую эфирным запахом и сначала сладким, потом жгучим вкусом. Кипит при 38,4°С. В воде...
-
Введение - Производство нитратной кислоты АК-72. Анализ стадий переработки оксидов азота в HNO3
Азотная кислота - одна из важнейших минеральных кислот. По объему производства в химической промышленности она занимает второе место после серной...
-
Качественные методы анализа - Разработка технологической схемы получения анизола и крезола
Рециркуляционных реакционно-ректификационных процессов. При анализе сложных ХТС, характеризующихся большим числом параметров и переменных необходимо...
-
Технологическая схема - Производство ацетона
Технический результат заключается в том, что представляется возможным производить высококачественный ацетон с минимальными эксплуатационными затратами,...
-
Полимеризация двуокиси азота. Переработка нитрозных газов в азотную кислоту обычно происходит при температурах от О до 50 °С. В этих условиях двуокись...
-
Пластичными массами называют материалы, полученные на основе полимеров, содержащие различные добавки и способные под влиянием температуры и давления,...
-
Гедонистический подход Гедонистический подход используется при анализе ценообразования и заключается в моделировании цены объекта как функции от его...
-
Порфиразины с аннелированными шестичленными N - гетероциклами - пиридиновыми и пиразиновыми кольцами, среди которых первыми были синтезированы...
-
Фотоэлектроколориметрические методы относятся к объективным методам, так как интенсивность окраски растворов оценивают с помощью специальных устройств -...
-
Получение., Применение. - Свойства фтора как химического элемента
Источником для производства фтора служит фтористый водород, получающийся в основном либо при действии серной кислоты H2SO4 на флюорит CaF2, либо при...
-
Технологии производства метанола - Синтез на основе оксидов углерода и водорода
Способ, основанный на сухой перегонке древесины, до 1913 года оставался единственным освоенным процессом получения метанола, а в 1913 г. был разработан...
-
Технологические свойства метанола Метанол (метиловый спирт) СН3ОН представляет бесцветную легкоподвижную жидкость с температурой кипения 64,65°С,...
-
Экономические показатели процесса можно улучшить и за счет комбинирования двух других способов производства винилхлорида: из этилена и ацетилена, когда...
-
Теоретические основы процесса Реакторы смешения - это емкостные аппараты с мешалкой или циркуляционным насосом. Человечество давно пользуется...
-
Применение спиртов - Химические свойства и характеристики спиртов
Способность спиртов участвовать в разнообразных химических реакциях позволяет их использовать для получения всевозможных органических соединений:...
-
1. Спирты реагируют со щелочными металлами (Na, K и т. д.) с образованием алкоголятов: 2R--OH + 2Na 2R--ONa + H2 Реакция протекает не так бурно, как при...
-
Использование предшественников при производстве аминокислот позволяет успешно обходить метаболический контроль, осуществляющийся по механизму обратной...
-
Оценка времени поездки на основе моделирования транспортных потоков
Оценка времени поездки на основе моделирования транспортных потоков С. Н.Козорезова Постоянное увеличение количества транспортных заторов на...
-
Обсуждение результатов - Синтез пара-нитродифенила. Теоретические основы нитрования
Для нитрования дифенила использовалась смесь азотной и уксусной кислот. Так как при нитровании в смеси азотной и серной кислот образуются...
-
В настоящее время из всех полупроводниковых материалов наибольшее применение для изготовления полупроводниковых ИМС получил кремний. Кремний - элемент IV...
-
К числу физических факторов, вызывающих коррозию цементного камня и бетона, относят их попеременное увлажнение и высыхание, которое сопровождается...
-
Кремний - элемент главной подгруппы четвертой группы третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 14....
-
Азотная кислота широко применяется для производства многих продуктов, используемых в промышленности и сельском хозяйстве Список использованной литературы...
Синтезы на основе ацетилена - Анализ и технологическая оценка химического производства