Рассмотрим методы идентификации и количественного анализа на примере рецептуры аптеки №9/249 - Аскорбиновая кислота
Раствор кислоты аскорбиновой 5% (концентрированный раствор)
Определение подлинности
- 1. К 4-5 каплям р-ра прибавляют 2-3 капли р-ра нитрата серебра; образуется металлическое серебро в виде серого осадока. 2. К 4-5 каплям р-ра прибавляют 1-2 капли р-ра хлорида окисного железа и р-ра феррицианида калия ; появляется синее окрашивание. 3. К 4-5 каплям р-ра прибавляют 0,5 мл 1-2 капли 0,1 н. р-ра йода;р-р йода обесцвечивается.
Количественное определение
- 1. К 0,5 мл р-ра прибавляют 2 мл воды и титруют 0,1 н. р-ром йода до желтого окрашивания. 1 мл 0,1 н. р-ра йода соответствует 0,0088 г к-ты аскорбиновой 2. К 1 мл р-ра прибавляют 2 мл воды, 7 капель р-ра фенолфталеина и титруют 0,1 н. р-ром едкого натра до розового окрашивания. 1 мл 0,1 н. р-ра едкого натра соответствует 0,0176 г к-ты аскорбиновой.
Кислота аскорбиновая 0,1
Глюкозы 0.5
Определение подлинности
Глюкоза
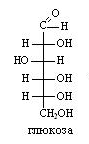
Рис.15
Глюкоза проявляет как окислительные, так и восстановительные свойства, благодаря альдегидной группе.
Она дает реакцию серебряного зеркала:
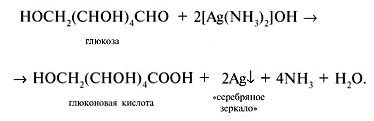
Рис. 16
Реакции со свежеполученным гидроксидом меди (II) при нагревании:
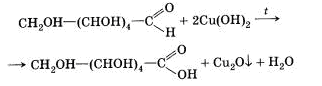
.
Рис. 17
Восстановление альдегидной группы в соответствующий спирт:
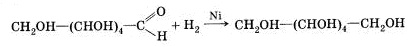
.
Рис. 18
Методика определения подлинности: К 0.01 г порошка прибавляют 0,01 г тимола, 5-6 капель конц. серной кислоты; появляется красно-фиолетовое окрашивание.
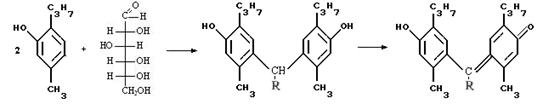
Рис. 19
Кислота аскорбиновая
- 1. К 0,03 г порошка прибавляют 2-3 капли р-ра нитрата серебра; образуется серый осадок. 2. К 0,03 г порошка прибавляют 1-2 капли р-ра феррицианида калия и р-ра хлорида окисного железа; появляется синее окрашивание
Количественное определение
Кислота аскорбиновая
- 1. 0,05 г порошка растворяют в 2 мл воды и титруют 0,1 н. р-ром йода до желтого окрашивания. 1 мл 0,1 н. р-ра йода соответствует 0,0088 г к-ты аскорбиновой 2. 0,05 г порошка растворяют в 2 мл воды, прибавляют 6-7 капель р-ра фенолфталеина и титруют 0,1 н. р-ром едкого натра до розового окрашивания. 1 мл 0,1 н. р-ра едкого натра соответствует 0,0176 г к-ты аскорбиновой.
Глюкоза
0,1 г порошка помещают в сухую пробирку, точно пипеткой прибавляют 1 мл воды, перемешивают до растворения порошка и оставляют стоять около рефрактометра на 3о минут. Далее определяют показатель преломления воды (n0) и полученного раствора (n) с применением рефрактомектра.
Расчет содержания глюкозы в одном порошке в граммах (Х) производят по формуле:
(n-n0) х Р х (а+1) - 100 х а х (F1 x P1 ) (n-n0)x 0,6x1,1 - 100 x 0,1x (0,00160 x P1); где
Х= F2 x a x 100 = 0,00145 x 0,1 x 100
N - показатель преломления полученного раствора (аГ + 1 мл), при 20ОС;
N0- показатель преломления воды при 20ОС ( 0,3330);
Р-вес порошка по прописи, г;
А-навеска порошка, взятая для анализа, г;
(аГ + 1 мл) - вес полученного раствора, в граммах (0,1 г порошка + 1 г воды =1,1г);
Р1 - содержание кислоты аскорбиновой в одном порошке, найденное химическим методом, г;
F1 - фактор показателя преломления раствора кислоты аскорбиновой с весовой концентрацией (аГ + 1 мл), (0,00160);
F2 - фактор показателя преломления растворов глюклзы с весовой концентрацией (аГ + 1 мл), (0,00145).
Рибофлавина 0,002
Калия йодида 0,3
Раствор глюкозы 2% - 10,0
Определение подлинности
Рибофлавин
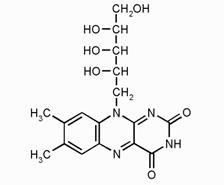
Рис.20
- 1. Р-р желтого цвета с желто-зеленой флюоресценцией. 4.5 Кислота аскорбиновая 1. К 0,5 мл р-ра прибавляют 1 каплю 0,1 н. р-ра йода;р-р йода обесцвечивается. Калия йодид 1. К 1-2 каплям р-ра прибаляют 1 мл р-ра виннокаменной кислоты, 1 мл р=Ра ацетата натрия, охлаждают и сильно встряхивают; постепенно выпадает белый кристаллический осадок, растворимый в разведенных минеральных кислотах и растворах едких щелочей.
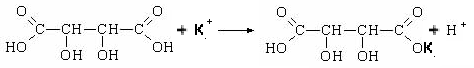
Рис. 21
- 2. Графитовую палочу, смоченную раствором, вносят в бесцветное пламя горелки; пламеня горелки окрашивается в фиолетовый цвет 3. К 1-2 каплям р-ра прибавляют 2-3 капли уксусной к-ты и 2-3 капли р-ра кобильтинитрита натрия; образуется желтый кристаллический осадок. 2К+ + Na+ + [Co(NO2)6] CH3COOH> K2Na[Co(NO2)6] 4. К 2-3 каплям р-ра прибавляют по 3-5 каплям разведенной серной кислоты и р-ра нитрита натрия, 1 мл хлороформа и взбалтывают; хлороформный слой окрашивается в фиолетовый цвет. 2I- + 2NO2- + 4H+ хлороформ> I2 + 2NO + 2H2O
Глюкоза
1. 0,5 мл р-ра выпаривают в фарфоровой чашке на водяной бане досуха. После охлаждения к остатку прибавляют 0,01 г тимола; 5-6 капель канц. серной кислоиы и 1-2 капли воды; появляется фиолетовое окрашивание.
Количественное определение
Кислота аскорбиновая
1. К 1 мл р-ра прибавляют 6-7 капель р-ра фенолфталеина и титруют 0,02 н. р-ром едкого натра до оранжево-розового окрашивания. 1 мл 0,02 н. р-ра едкого натра соответствует 0,00352 к-ты аскорбиновой.
Калия йодид
1. К 0,5 мл р-ра прибавляют 0,5 мл разведенной уксусной к-ты, каплю р-ра эозина натрия и титруют 0,1 н. р-ра нитрата серебра до перехода окраски осадка от желтой до розовой.
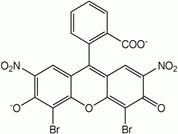
Рис. 22
КI + AgNO3 CH3COOH> AgI + KNO3 + AgI CH3COOH> анион эозина после достижения точки эквивалентности адсорбируется осадком AgI (метод Фаянса)
1 мл 0,1 н. р-ра нитрата серебра соответствует 0,0166 гкалия йодида.
Глюкоза
Определяют показатель преломления р-ра с применением рефрактометра.
Расчет содержания глюкозы в процентах проводят по формуле:
[(n-n0)- (F1XC1+F2XC2)]x100
Где X= Fx100
C1, C2 - концентрации кислоты аскорбиновой и калия йодида в испытуемом р-ре, найденные химическим методом, %;
F1- фактор показателя преломления р-ра к-ты аскорбиновой (0,00160);
F2- фактор показателя преломления р-ра калия йодида (0,00130);
F - фактор показателя преломления р-ра безводной глюкозы (0,00142).
Примечание: 0,02% концентрация рибофлавина в р-ре практически не влияет на показатель преломления р-ра.
Рибофлавина 0,002
Кислоты аскорбиновой 0,02
Тиамина бромида
Кислоты никотиновой по 0,03
Раствор глюкозы 2% - 10,0
Натрия хлорида 0,043 (изотонический эквивалент кислоты аскорбиновой по натрию хлориду = 0,18 ). Определение подлинности
Рибофлавин
1. Р-р окрашен в желтый цвет.
Кислота аскорбиновая
1. 0,5 мл р-равыпаривают в фарфоровой чашке на водяной бане досуха. после охлаждения к остатку прибавляют 2 капли р-ра феррицианида калия и 1-2 капли 3% р-ра хлорида окисного железа; тотчас же появляется синее окрашивание. Тиамина бромид
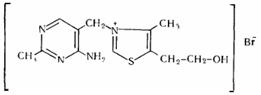
Рис.23
1. 0,5 мл р-ра выпаривают в фарфоровой чашке на водянй бане досуха. После охлаждения к остатку прибавляют несколько кристалликов сульфата меди и 2-3 капли конц. серной кислоты; образуется черное окрашивание, исчезающее при добавлении 2-3 мл воды.
Кислота никотиновая
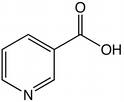
Рис.24
Химический аскорбиновый кислота
1. К 2-3 каплям р-ра прибавляют 2-3 капли р-ра бихромата калия, 1 мл хлороформа и 2-2,5 мл р-ра пергидроля в ацетоне; при взбалтывании хлороформный слой окрашивается в сине-фиолетовый цвет.
Глюкоза
1. 0,5 мл р-ра выпаривают в фарфоровой чашке на водяной бане досуха. После охлаждения к остатку прибавляют 0,01 г тимола; 5-6 капель канц. серной кислоиы и 1-2 капли воды; появляется фиолетовое окрашивание.
Натрия хлорид
NaCI
- 1. Гафрированную палочку, смоченную р-ром, вносят в бесцветное пламя горелки; пламя окрашивается в желтый цвет. 2. К 1-2 каплям р-ра прибавляют 1-2 капли разведенной уксусной к-ты и 1-2 капли р-ра цинк-урасилацетата; образуется желтый кристаллтческий осадок:
Na+ + Zn2+ + 3UO22+ + 9CH3COO- > NaZn(UO2) 3(CH3COO)9 X9H2O
К 3-5 каплям р-ра прибавляют по 3-5 капель разведенной азотной к-ты и и раствора нитрата серебра; образуется белый творожистый осадок, растворимый в растроре аммиака:
CI- + 2AgNO3 HNO3> AgCI v NO3-
AgCI + 2NH3- > [Ag(NH3)2]+ + CI-
Количественное определение
Кислота аскорбиновая, кислота никотиновая и тиомина бромид
К 0,5 мл р-ра прибавляют 6-7 капель р-ра фенолфталеина и титруют 0,02 н. р-ром едкого натра до оранжево-розового окрашивания (А мл).
Кислота аскорбиновая. К оттитрованной жидкости прибавляют 3 капли р-ра крахмала и титруют 0,02 н. р-ром йода до синего окрашивания (Б мл).
1 мл 0,02 н. р-ра йода соответствует 0,00176 г к-ты аскорбиновой.
Разносттьь между количеством мл 0,02 н. р-ра едкого натра и количеством мл 0,02 н. р-ра йода, деленного на два - (А-Б/2)мл, рассчитывают на сумму тиамина бромида и кислоты никотиновой.
1 мл 0,02 н. р-ра едкого натра соответствует 0,003838 г суммы тиамина бромида и кислоты никотиновой.
Примечание. Б мл делится на 2, т. к. кол-во мл 0,1 н. р-ра йода на титрование к-ты аскорбиновой расходуется вдвое больше, чем 0,1 н р-ра едкого натра.
Тиамина бромид и натрия хлорид.
К 1 мл р-ра прибавляют 0,5 мл разведенной азотной кислоты, 15 капль р-ра железо-аммониевых квасцов, 2 мл 0,1 н. р-ра нитрата серебра и сильно взбалтывают до отстаивания осадка. Избыток 0,1 н. р-ра нитрата серебра оттитровывают 0,1 н р-ром роданида аммонои до желто-розового окрашивания.
Параллельно проводят контрольный опыт.
1 мл 0,1 н. р-ра нитрата серебра соответствует 0,0092 г суммы тиамина брмиба и натрия хлорида.
Глюкоза
Определяют показатель преломления р-ра с применением рефрактометра.
Расчет содержания глюкозы в процентах проводят по формуле:
[(n-n0)- (F1XC1+F2XC2+F3XC3+F4XC4]x100
Где X= Fx100
C1, C2 - концентрации кислоты аскорбиновой, тиамида бромида, кислоты никотиновой, натрия хлорида в испытуемом р-ре, найденные химическим методом, %;
F1- фактор показателя преломления р-ра к-ты аскорбиновой (0,00160);
F2- фактор показателя преломления р-ра тиамина бромида (0,00200);
F3- фактор показателя преломления р-ра к-ты никотиновой (0,00210);
F4- фактор показателя преломления р-ра натрия хлорида (0,00173);
F - фактор показателя преломления р-ра безводной глюкозы (0,00142).
Примечание: 0,02% концентрация рибофлавина в р-ре практически не влияет на показатель преломления р-ра.
Похожие статьи
-
При кипячении с разведенной хлороводородной кислотой происходит процесс гидролиза с образованием бензгидрола: Обнаружение димедрола методом ТСХ....
-
Испытания на чистоту, Количественное определение - Аскорбиновая кислота
В качестве допустимых примесей рассматривают сульфатную золу (не более 0,1 %) и тяжелые металлы (не более 0,001 %). Содержание органических примесей...
-
Строение и физико-химические свойства аскорбиновой кислоты - Аскорбиновая кислота
Аскорбиновая кислота (Acidumascorbinicum) - это белые кристаллы с резким кислым вкусом. Молекулярная масса = 176,13. Температура плавления аскорбиновой...
-
Методы анализа - Свойства флавоноидов
Качественное определение. Для обнаружения флавоноидов в ЛРС используют химические реакции и хроматографию. Химические реакции подразделяются на цветные и...
-
Оценка качества лекарственных средств, Определение подлинности - Аскорбиновая кислота
Определение подлинности Химический аскорбиновый кислота При определении подлинности используют восстановительные и кислотные свойства аскорбиновой...
-
Наиболее представительные ионы и соответствующие им структуры помещены в таблицы, их используют при интерпретации масс-спектров. Кроме того сравнивают...
-
Азотный кислота утилизация оксид Методы получения азотной кислоты Первый завод по производству HNO3 из аммиака коксохимического производства был пущен в...
-
На хроматографической пластинке, покрытой закрепленным тонким слоем силикагеля, отмечают линию старта, на которую наносят каплю хлороформной вытяжки из...
-
Выполнение реакции: Реактив - хлорид железа (III) (раствор, содержащий иодид калия). Для его приготовления к 3 мл 10%-го раствора хлорида железа (III)...
-
Это метод который нашел мировое применение для анализа лекарствнных средств. Он основан на свойстве галогенидов количественно осаждаться нитратом серебра...
-
Задачи и методы количественного анализа - Основы аналитической химии
Количественный анализ - это совокупность химических, физико-химических и физических методов определения количественного соотношения компонентов, входящих...
-
Общая методика. В круглодонной трехгорлой колбе емкостью 100 мл растворяли 11,9 г бензотриазола (2-аминопиридина) в 20 мл толуола. Колбу соединяли с...
-
Особенности анализа органических соединений
Особенности анализа органических соединений: - Реакции с органическими веществами протекают медленно с образованием промежуточных продуктов. -...
-
Выбор метода производства (или выделение) готового продукта Современные методы производства азотной кислоты основаны на применении синтетического аммиака...
-
Реакция с реактивом Марки. К сухому остатку на фарфоровой чашке добавляют 1 каплю реактива Марки, наблюдают лимонно-желтое окрашивание, переходящее при...
-
Фотоэлектроколориметрические методы относятся к объективным методам, так как интенсивность окраски растворов оценивают с помощью специальных устройств -...
-
Проба Бейльштейна. [6] Медную проволоку с загнутым в виде петельки концом прокаливают в пламени горелки для образования на поверхности слоя оксида меди...
-
Применение статистических методов анализа для адекватной интерпретации результатов контроля остаточных знаний соискателей высшего образования на примере...
-
АНАЛИТИКА Компиляция выдержек из различных источников - удельная б-активность U235 и U238 составляет соответственно 0,08 и 0,012 Бк/мкг (или 80 и 12...
-
Синтез гетероциклических соединений Синтез 4-амино-1,2-бензотиазола К раствору 5-8 г (31 ммоль) 2,6-диметилтолуола в 15 мл мезителена (температура...
-
Источники и способы получения - Аскорбиновая кислота
Аскорбиновая кислота содержится в значительных количествах в овощах (салат, капуста), плодах, ягодах, хвое, шиповнике, в листьях черной смородины....
-
Введение - Аскорбиновая кислота
Аскорбиновая кислота впервые выделена в чистом виде Сцент-Гиорги в 1928 г. под названием гексуроновая кислота. В 1933 г. рядом исследователей установлена...
-
Обработка смесью серной и азотной кислот - метод Дениже. Данный метод часто используют в агрохимических и почвенных лабораториях. В настоящее время...
-
В сухую колбу Кьельдаля вносят 0,1 г исследуемого продукта, наливают 5 см3 концентрированной серной кислоты. Добавляют небольшое количество катализатора....
-
Метод Кьельдаля - обработка серной кислотой так же называют - "мокрое сжигание". Определение количества азота с помощью метода Кьельдаля основано на...
-
Определение галоида по методу Кариуса. Навеску вещества при нагревании окисляют дымящей азотной кислотой в присутствии нитрата серебра. При этом галоид...
-
Запасы этих растворов, несоответствующих показателям качества, исчисляются сотнями тысяч тонн и дальнейшее их хранение становится очень опасным для...
-
ОПРЕДЕЛЕНИЕ МЕТОДА ФАКТОРНОГО АНАЛИЗА И ЧИСЛА ФАКТОРОВ - Многомерный статистический анализ
Определение метода факторного анализа. Различные методы факторного анализа различаются в зависимости от подходов, которые используются для выделения...
-
Количественная характеристика трудовых ресурсов в первую очередь измеряется такими показателями, как общая, списочная, явочная и среднесписочная...
-
Моделирование. Детерминизм. Требования к моделированию В процессе исследования объекта часто бывает нецелесообразно или даже невозможно иметь дело...
-
В последнее время органические вещества признаны определяющими весь ход гидрогеохимических процессов и техногенеза окружающей среды в целом. Основную...
-
Анализ удобрений - Агрохимический анализ почв, растений, удобрений
Определение видов и форм некоторых минеральных удобрений по качественным реакциям 1. Простые минеральные удобрения могут быть Кристаллическими (к ним...
-
Этаминал-натрий дает фиолетовую окраску с солями кобальта и изопропиламином. Выполнение реакции. К 2 мл хлороформного раствора исследуемого вещества...
-
Идея электроспрея, хоть и не нова, была возрождена в связи с ее настоящим применением к биомолекулам. Первые эксперименты с электроспреем были проведены...
-
Задачи и методы качественного анализа - Основы аналитической химии
Обнаружение или, как иногда говорят, "открытие" отдельных элементов или ионов, входящих в состав веществ - это задачи качественного анализа. Качественный...
-
Хранилище серной кислоты На территории участка серной кислоты сернокислотного цеха (далее УСК СКЦ) установлено четыре емкости - хранилища, изготовленные...
-
Схема 1. Технологическая схема производства серной кислоты по методу ДК. 1-серная печь; 2- котел-утилизатор; 3- экономайзер; 4- пусковая топка;...
-
Для примера рассмотрим вытекающую из общей постановки (3),(4) двухкритериальную () многоэтапную динамическую задачу, с целевыми функциями дохода и потерь...
-
Сущность группировки, их виды и значение Группировка -- это распределение единиц по группам в соответствии со следующим принципом: различия между...
-
В результате первой стадии статистического исследования (статистического наблюдения) получают статистическую информацию, представляющую собой большое...
Рассмотрим методы идентификации и количественного анализа на примере рецептуры аптеки №9/249 - Аскорбиновая кислота