Метод вакуум-термического восстановления - Металлургия лития, рубидия и цезия
Первые систематические исследования процессов металлотермического восстановления редких щелочных металлов были про-ведены русским химиком Н. Н. Бекетовым, получившим металлические рубидий и цезий действием алюминия на RbOH и CsOH. В дальнейшем в качестве исходных веществ для получения лития, рубидия и цезия была опробована большая группа соединений (галогениды, гидроокиси, карбонаты, сульфаты, хроматы, цианиды, алюминаты, силикаты и бихроматы) и значительное ко-личество восстановителей (магний, кальций, барии, натрий, алю-миний, железо, цирконий, кремний, углерод, титан).
Выбор восстановителя и восстанавливаемого соединения произ-водится прежде всего сопоставлением изобарно-изотермических потенциалов реакций восстановления:
МеА + Ме' = Ме'А + Ме
Ввиду заметного давления пара лития, рубидия и цезия при температурах их восстановления изменение давления в системе существенно влияет на скорость реакции и ее направление. В связи с этим большинство металлотермических реакций получения ли-тия, рубидия и цезия проводят в специальных вакуум термических установках.
Помимо величины и давления пара эффективность вакуум-термического восстановления лития, рубидия и цезия определяется и другими физико-химическими факторами, а именно: способ-ностью к образованию между восстановителем и восстанавливае-мым металлом интерметаллических соединений, сплавов и твер-дых растворов; гигроскопичностью исходного соединения восста-навливаемого щелочного металла и т. д.
Указанные выше факторы отчасти объясняют неудачи многих попыток металлотермического восстановления некоторых соедине-ний лития, рубидия я цезия.
Так, восстановление гидроокисей магнием и алюминием по реакциям
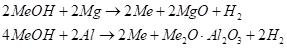
Оказалось очень сложным и бесперспективным из-за бурного про-текания реакции, гигроскопичности исходных соединений, летуче-сти магния при температуре процесса (800 - 900°С) и частичного образования гидридов щелочных металлов. Выход металла при этом небольшой, в частности при использовании алю-миния - не выше 30%.
Изучение возможности восстановления хлоридов (видимо, и других галогенидов) лития, рубидия и цезия такими реагентами, как натрий, алюминий, кремния, титан, цирконий и железо, вскры-ло целый ряд трудностей в осуществлении технологического про-цесса. Натрий обладает высокой летучестью при рабочих темпера-турах и поэтому очень загрязняет получаемый металл. Алюминий, кремний, титан, цирконий и железо дают легко возгоняющиеся продукты реакции, взаимодей-ствующие в конденсаторе с щелочным металлом и образующие исходные хлориды.
Проведенные исследования показали также, что вос-становление LіCI и LiCN щелочноземельными металлами и кар-бидом кальция приводит к неполному извлечению лития либо вследствие высокой летучести его хлорида при температуре про-цесса, либо из-за образования очень устойчивого карбида лития (при использовании LiCN). Небольшой выход металла (50 - 56%) был получен и при восстановлении RbCl и CsCl карбидом каль-ция.
Неудачными оказались н попытки применить в качестве исход-ных соединений карбонаты и их смесь с гидротартратами, хотя и было опробовано несколько восстановителей (С, Fe, Ni, Mg, Si). Процесс при этом протекает при высокой температуре 1000 - 1300°С), очень бурно, часто с воспламенением и взрывом. Выде-ляющаяся при реакции двуокись углерода превращает литий, рубидий и цезий в окиси, а углерод взаимодействует с литием с об-разованием карбида Li2C2. В результате выход металла с большим содержанием различных примесей составляет всего 18 - 50%.
Из всех многочисленных соединений лития лишь его окись и моноалюминат позволили получить при вакуум-термическом восстановлении, что касается рубидия и цезия, то высокий выход при хорошем качестве металла был достигнут при восстановлении алюминатов магнием и бихроматов и хроматов цирконием и хлоридов кальцием
Похожие статьи
-
Вакуум-термическое восстановление окиси и моноалюмината лития - Металлургия лития, рубидия и цезия
Вакуум-термическое восстановление окиси литии проводят кремнием или алюминием в присутствии окисн кальция, которая связывает SiO2 и AI 2 O 3 ,...
-
Метод термического разложения солей в крайне ограничен-ных масштабах применяется только для получения небольших количеств особо чистых рубидия и цезия,...
-
Получение литиевых сплавов электролизом представляет боль-шой практический интерес: легко осуществляется легирование алюминия, меди, свинца и других...
-
Вакуум-термическое получение металлических рубидия и цезия - Металлургия лития, рубидия и цезия
Вакуумтермический метод является основным методом полу-чения металлических рубидия и цезия. Для восстановления рубидия и цезия используются следующие...
-
Введение., Электрохимический метод получения металлов - Металлургия лития, рубидия и цезия
Получение лития, рубидия и цезия в виде металлов связано с рядом особенностей, обусловленных прежде всего высокой химиче-ской активностью этих металлов....
-
Упаковка и хранение лития, рубидия и цезия - Металлургия лития, рубидия и цезия
Высокая химическая активность лития, рубидия и цезия тре-бует особых условий хранения, упаковки и обращения с этими ме-таллами. Особенно опасны в...
-
Получение металлического лития - Металлургия лития, рубидия и цезия
Как известно, при электролизе водных раство-ров солей лития, рубидия и цезия на катоде вместо металла выде-ляется водород. Поэтому получение...
-
Вакуум-термическое получение лития из сподумена - Металлургия лития, рубидия и цезия
Большой практический интерес представляют методы непосред-ственного получения лития из его минерального сырья. В полу-промышленном масштабе пока...
-
NаСl + NН4НСО3 NаНСО3 + NН4Сl Равновесие которой почти нацело смещено вправо (вследствии очень малой растворимости NаНСО3 в растворе NН4Сl)....
-
Методы, применяющиеся для синтеза мультиферроиков - Мультиферроики
Для синтеза мультиферроиков используются различные методы синтеза. К ним относятся: спекание, гидротермальный синтез, соосаждение, золь-гель метод,...
-
Получение металлического бария, Восстановление окиси или хлорида бария - Барий
Металлический барий получают металлотермическим восстановлением окиси или хлорида бария, термическим разложением гидрида и нитрида бария или Ba(NH 3)e,...
-
Мы обнаружили интересный факт в опытах с соляной кислотой (опыты 6,7, таблица 4). Оказалось, что в солянокислой восстановительной среде йод, выделившийся...
-
Сравнение методов получения хлорида калия - Производство хлорида калия галургическим способом
Флотационный метод обогащения по сравнению с галургическим (растворение и кристаллизация) имеет следующие преимущества: - флотация проходит при...
-
Для получения монокристаллов арсенида индия с высокими и стабильными электрофизическими параметрами необходимо использовать высокочистые исходные...
-
Формула изобретения - Каталитический риформинг
1. Адсорбент для очистки газов и жидкостей от галогенсодержащих соединений, включающий оксиды цинка и алюминия, соединение щелочного металла,...
-
Углерод (лат. Carboneum), С - химический элемент IV группы периодической системы Менделеева. Известны два стабильных изотопа 12С (98,892 %) и 13С (1,108...
-
А) Углерод (С), кремний (Si), германий (Ge), олово (Sn), свинец (РЬ) - элементы 4 группы главной подгруппы ПСЭ. На внешнем электронном слое атомы этих...
-
APCI также стала важным способом ионизации, потому что она генерирует ионы непосредственно из раствора, и способна к анализу относительно неполярных...
-
Один из способов повысить селективность - это правильно подобрать катализатор. Рассмотрим этот метод, на примере получения анизола и крезола. Анизол и...
-
Методы расчета квантовых выходов - Свойства нейтральной формы гибридного соединения
В изучении фотоизомеризации часто случается так, что продукт реакции нельзя выделить в чистом состоянии, так как невозможно разделить реакционную смесь...
-
Полимерами называют вещества, молекулы которых (макромолекулы) состоят из одного или большего числа составных звеньев. Молекулярная масса (число атомов)...
-
Легирование стали повышает ее антикоррозионные свойства. Например, совершенную стойкость к атмосферной коррозии показывают нержавеющие легированные...
-
Процессы окисления. - Методы очистки и получения коллоидных растворов
Наряду с серой в реакциях окисления обычно образуются политио-новые кислоты, главным образом пентатионовая кислота H2S5O6 Реакции двойного обмена....
-
Определение температуры плавления Температуру плавления определяем с помощью малогабаритного нагревательного стола типа "Boetinus" с наблюдательным...
-
Общая методика. В трехгорловую колбу емкостью 50 мл, снабженную мешалкой, обратным холодильником и термометром, помещаем 20.0 мл моногидрата и нагреваем...
-
Химия фталоцианина (Рс) и его металлокомлексов (МРс) началась с его случайных открытий фталоцианина. Линстед с сотрудниками были первыми исследователями...
-
Конденсационные методы получения коллоидных систем - Методы очистки и получения коллоидных растворов
Из классификации дисперсных систем по размеру частиц следует, что коллоидные растворы (золи) занимают промежуточное положе-ние между молекулярными и...
-
Кривые титрования - Методы осаждения
Кривые титрования в аргентометрии обычно строят в координатах pAg -- V, Где pAg -- взятый с обратным знаком лога-рифм концентрации ионов Ag+, V -- Объем...
-
Методы анализа - Свойства флавоноидов
Качественное определение. Для обнаружения флавоноидов в ЛРС используют химические реакции и хроматографию. Химические реакции подразделяются на цветные и...
-
Методы выделения - Свойства флавоноидов
Для флавоноидов, как и для других веществ, не существует способа выделения, универсального для всех растительных материалов. В каждом конкретном случае...
-
Методы устранения жесткости - Жесткость воды и способы устранения
Чтобы избавиться от временной жесткости необходимо просто вскипятить воду. При кипячении воды, гидрокарбонатные анионы вступают в реакцию с катионами и...
-
Методы неорганического синтеза - Синтез ацетата натрия ("Горячий лед")
НЕОРГАНИЧЕСКИЙ СИНТЕЗ, получение неорганических соединений. Как правило, состоит из нескольких последовательных или параллельных процессов -...
-
Количественный анализ - это совокупность, химических, физико-химических и физических методов определения количественного соотношения компонентов,...
-
Положение металлов в ПС. Физические свойства металлов. Методы получения металлов - Основы химии
Металлы располагаются в основном в левой и нижней части ПС К физическим свойствам относятся плотность, плавление (температура плавления),...
-
Физические свойства Таллия - Третья группа периодической системы
. Таллий мягкий металл, на воздухе легко окисляется и быстро тускнеет. Таллий при давлении 0,1 Мн/м2 (1 кгс/см2) и температуре ниже 233 °С имеет...
-
Бериллий с точки зрения металлурга - Бериллий
Свойства бериллия чаще всего именуются "удивительными", "чудесными" и т. п. Отчасти это справедливо, причем главная "удивительность" заключается в...
-
Физические свойства., Химические свойства. - Третья группа периодической системы
Алюминий в свободном виде -- серебристо-белый металл, обладающий высокой тепло - и электропроводностью. Алюминий имеет невысокую плотность -- примерно...
-
Алюминий - самый распространенный в земной коре металл. На его долю приходится 5,5-6,6 мол. доли % или 8 масс. %. Главная масса его сосредоточена в...
-
Особенности обработки цветных металлов - Цветные металлы
Цветные металлы прочны и долговечны, способны переносить высокие температуры. Недостаток только один -- способность корродировать и разрушаться под...
-
Физико-химические свойства ртути - Ртуть: свойства и токсичность
Ртуть (Hg) - химический элемент II группы периодической системы элементов Д. И. Менделеева; атомный номер 80, относительная атомная масса 200,59; в...
Метод вакуум-термического восстановления - Металлургия лития, рубидия и цезия