Физико-химические закономерности получения продукта - Производство ацетона
Ацетон, применение которого можно отметить почти во всех сферах человеческой деятельности, имеет характерные физические свойства. Например, он оказывает наркотическое воздействие на организм человека, хотя считается малоопасным. Особенно это проявляется у людей, которые часто работают с ацетоном, используя его в качестве растворителя.
Стоит отметить, что он имеет свойство накапливаться в организме. Легковоспламеняемость этого вещества - основная опасность при работе с ним.
В связи с тем, что это вещество обладает высокой летучестью, оно имеет свойство быстро испаряться в атмосферу. Воздушные смеси с большой концентрацией ацетона - взрывоопасны. Ацетон, химические свойства которого нашли применение в лакокрасочной промышленности, обладает устойчивостью к действию подавляющего большинства окислителей. Это полезное свойство позволяет использовать его для производства авиационных, кабельных, автомобильных и многих других лаков и эмалей.
Безопасность в работе с ацетоном. При использовании ацетон, ГОСТ 2603-79, требует аккуратности и внимательности, поскольку является активным растворителем. Его можно применить для разбавления нитролаков и нитроэмалей, а также придать загустевшей эмали нужную консистенцию. Лакокрасочное покрытие после высыхания приобретет дополнительный блеск благодаря ацетону. [1]
Это вещество активно применяется для очистки поверхностей и инструмента от полиуретановой монтажной пены или лакокрасочных материалов. Ацетилен, использующийся для сварки металлов, очень хорошо растворяется в нем. При давлении в 15 атмосфер, создаваемом стальным баллоном, в котором хранится ацетилен, один объем ацетона способен растворить примерно 250 объемов ацетилена.
При использовании данного химического соединения следует помнить о правилах безопасности, использовать респиратор и резиновые перчатки, поскольку продолжительное вдыхание этого растворителя может привести к отеку глаз, а также вызвать головокружение и потерю ориентации в пространстве.
Физико-химические показатели ацетона
|
Наименование показателей |
Норма по ГОСТ |
|
Внешний вид |
Бесцветная прозрачная жидкость |
|
Массовая доля ацетона, %, не менее |
99,75 |
|
Плотность при 200С, г/см 3 |
0,789-0,791 |
|
Массовая доля воды, %, не более |
0,2 |
|
Массовая доля метилового спирта, %, не более |
0,05 |
|
Массовая доля кислот в пересчете на уксусную кислоту, %, не более |
0,001 |
|
Устойчивость к окислению марганцовокислым калием, ч, не менее |
4 |
Способ заключаются в том, что дистилляцию ацетона-сырца последовательно проводят в трех ректификационных колоннах. При этом в первой ректификационной колонне производят выделение низкокипящих примесей с добавлением в колонну реагента щелочного характера с последующим отбором оставшейся смеси компонентов в виде кубового продукта и подачи его в качестве питания во вторую ректификационную колонну для отделения высококипящих примесей и выделения большей части ацетона в виде товарного ацетона, причем содержание ацетона в кубе второй ректификационной колонны поддерживают до уровня не менее чем 0,5 массовых % от питания отбором оставшихся компонентов смеси в виде кубового продукта второй ректификационной колонны и последующей подачи его в качестве питания в третью ректификационную колонну для выделения оставшегося ацетона совместно с оставшимися низкокипящими примесями, в том числе с оставшимися альдегидами, и подачу этой смеси в первую ректификационную колонну, во вторую ректификационную колонну подают дополнительно реагент щелочного характера, позволяющий производить ацетон, имеющий время окисления перманганатом не менее десяти часов, при этом в первую ректификационную колонну реагент щелочного характера добавляют в виде 0,1-30 %-ого водного раствора в количестве 0,05-0,8 массовых % от питания колонны, и дополнительно в нее подают реагент окислительного характера в виде 0,1-30 %-го водного раствора в количестве 0,02-0,5 массовых % от питания при весовом отношении реагента щелочного характера к реагенту окислительного характера от 1:0,1 до 1:100, предпочтительно от 1:0,5 до 1:10; кроме того, во вторую ректификационную колонну подают реагент щелочного характера в количестве 0,03-0,5 массовых % от питания, при этом весовое отношение реагента щелочного характера, поданного в первую колонну, к реагенту щелочного характера, поданного во вторую колонну, составляет 1:0,2, причем вторую и третью колонны эксплуатируют при атмосферном давлении. Предлагаемый способ позволяет производить высококачественный ацетон с минимальными эксплуатационными затратами, достигая максимально возможной производительности. 1 ил. [2]
Известен способ очистки ацетона-сырца, заключающийся в том, что последний подвергают очистке последовательно в двух ректификационных колоннах, при этом очищенный в первой ректификационной колонне ацетон в виде кубового остатка подают во вторую колонну, с верха которой отводят очищенный ацетон в качестве товарного продукта (см. патент US 3215745, кл. С 07С 37/08, 02.11.1965).
Однако известно, что использование только простых методов дистилляции для того, чтобы очистить ацетон не эффективно, так как примеси, в частности алифатические альдегиды, олефины и целый ряд других примесей, остаются в очищенном продукте, снижая его чистоту и качество.
Наиболее близким к изобретению по технической сущности и достигаемому результату является способ очистки ацетона, заключающийся в том, что дистилляцию ацетона-сырца последовательно проводят в трех ректификационных колоннах (см. патент СА 1016100, кл. С 07С 49/08, 23.08.1977). [3]
По патенту СА 1016100 процесс очистки ацетона, содержащего альдегиды, осуществляют путем последовательной дистилляции в трех колоннах. В первой ректификационной колонне из ацетона-сырца отбирают головную фракцию, содержащую ацетальдегид. Дополнительно в колонну подается щелочь, чтобы перевести оставшуюся часть ацетальдегида в альдоли. Альдоли и оставшийся ацетальдегид, вместе с кубом колонны, подают в качестве питания во вторую ректификационную колонну. Во второй ректификационной колонне в виде дистиллята отгоняется большая часть ацетона. Кубовый продукт, содержащий тяжелокипящие примеси и оставшуюся часть ацетона, подается в третью ректификационную колонну, причем кубовый продукт содержит, по крайней мере, 0,5 мас. % ацетона. В третьей ректификационной колонне выделяется в виде дистиллята весь оставшийся ацетон, а также весь оставшийся ацетальдегид, выделившийся при разложении альдолей. Дистиллят этой третьей колонны предпочтительно рецикловать в первую колонну, где ацетальдегид выделяется в головной фракции, или на стадию расщепления гидроперекиси кумола. Первая колонна работает при атмосферном давлении и температуре верха колонны около 50°С. Для того, чтобы провести реакцию альдольной конденсации с оставшимися альдегидами, в колонну подается реагент основного характера, например, каустик (водный раствор NaOH). Большая часть каустика подается на тарелку ниже тарелки питания, в то время как оставшаяся часть подается над тарелкой питания. Вторая колонна работает при пониженном давлении, например, с температурой верха около 40°С. Кубовый продукт этой колонны должен содержать, по крайней мере, 0,5 мас. % ацетона, предпочтительно 1 мас. %. Обычные рабочие условия третьей колонны - работа при повышенном давлении (давление верха колонны 950 мм рт. ст. и температура 85°С).
Использование этого метода позволяет получить ацетон с устойчивостью к окислению "РТ-тестом", равным около 24 часов, согласно определению теста на устойчивость к окислению ацетона по BS 509: part 1:1971.
При этом, согласно британскому стандарту BS 509: part 1:1971, по которому при его определении к 100 мл образца приливают 1,0 мл 0,1 % раствора KMnO4 и определяют время изменения окраски по сравнению с эталоном. Однако теперь РТ определяют по новым американским стандартам - ASTM метод D-1369-94, согласно которому к 50 мл образца приливают 2,0 мл 0,02 % раствора KMnO4. Таким образом, условия определения РТ по BS 509: part 1:1971 значительно отличаются от условий определения РТ по американскому стандарту ASTM метод D-1369-94, по которому и проводили определение РТ в настоящем патенте. При прочих равных условиях при определении РТ по британскому стандарту используют в 2,5 раза большее количество KMnO4 (при пересчете количества KMnO4 в граммах на 100 мл образца) по сравнению с количеством KMnO4, которое используется при определении РТ по американскому стандарту. Таким образом, использование американского стандарта при определении РТ вместо британского стандарта снижает определяемое РТ более чем в 2,5 раза, т. е. указанное в СА 1016100 РТ время снижается с 24 часов до менее 10 часов. Ниже в прототипах 12 и 13 измеряемое по американскому стандарту РТ не превышает 6,5 часов.
Кроме того, реализация способа по патенту СА 1016100 предполагает эксплуатацию второй ректификационной колонны при пониженном давлении, а третьей - при повышенном давлении. При заданном режиме в значительной мере возрастают эксплуатационные расходы как за счет создания вакуума, так и за счет использования холодильных установок при конденсации паров второй колонны. При этом работа второй колонны при пониженном давлении приводит к существенному снижению ее производительности по сравнению с ее работой при атмосферном давлении. При прочих равных условиях (флегмовое число, температура питания и флегмы) перевод второй колонны с работы при 500 мм рт. ст., как указано в СА 1016100, на работу при атмосферном давлении (760 мм рт. ст.) повышает производительность колонны на 50 %. Дополнительный недостаток предложенной схемы заключается в том, что работа третьей колонны при повышенном давлении приводит к образованию большего числа примесей (как за счет большего разложения альдолей, так и за счет дополнительных примесей, вновь образующихся при более высоких температурах по сравнению с работой колонны при атмосферном давлении), которые, циркулируя в системе выделения и очистки ацетона, в конечном итоге в большей степени аккумулируются в ней и приводят к снижению качества товарного ацетона.
Обнаружение ацетона. В химико-токсикологическом анализе для обнаружения ацетона применяют реакции с растворами иода, нитропруссида натрия, фурфурола, о - нитробензальдегида и метод микродиффузии.
Реакция образования йодоформа. При взаимодействии ацетона с раствором иода в щелочной среде образуется йодоформ:
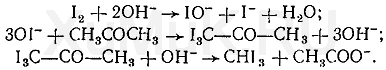
Выполнение реакции. К 1 мл исследуемого раствора прибавляют 1 мл 10 %-го раствора аммиака и несколько капельраствора иода в иодиде калия. В присутствии ацетона образуется желтый осадок йодоформа с характерным запахом, а его кристаллы имеют характерную форму.
Предел обнаружения: 0,1 мг ацетона в пробе.
Эту реакцию дает и этиловый спирт.
Реакция с нитропруссидом натрия. Ацетон с нитропруссидом натрия в щелочной среде дает интенсивно-красную окраску. При подкислении уксусной кислотой окраска переходит в красно-фиолетовую:
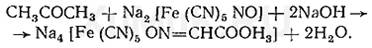
С нитропруссидом натрия окрашенные соединения образуют вещества, содержащие енолизируемые СО-группы:
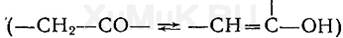
Кетоны, в молекулах которых отсутствуют метильные или метиленовые группы, связанные с СО-группами, не дают этой реакции.
Выполнение реакции. К 1 мл исследуемого раствора прибавляют 1 мл 10 %-го раствора гидроксида натрия и 5 капель 1 %-го свежеприготовленного раствора нитропруссида натрия. При наличии ацетона в пробе появляется красная или оранжево-красная окраска. При добавлении 10 %-го раствора уксусной кислоты до кислой реакции через несколько минут окраска переходит в красно-фиолетовую или вишнево-красную. [4]
Таким образом, главным недостатком этого изобретения является не только недостаточно высокое качество производимого ацетона по сравнению со значительными эксплуатационными и капитальными расходами, но и заметное снижение производительности установки.
Похожие статьи
-
Технологическая схема - Производство ацетона
Технический результат заключается в том, что представляется возможным производить высококачественный ацетон с минимальными эксплуатационными затратами,...
-
Получение синтезированного газа - Анализ и технологическая оценка химического производства
Химические методы переработки нефти проводят при высоких температурах без катализатора (термический крекинг), при высоких температурах в присутствии...
-
Таблица 2 - Структура сырья в производстве метанола, %. Сырье В мире Беларусь и Россия Природный газ 73,8 70,7 Нефть и нефтепродукты 24,4 4,0 Отходы...
-
В настоящее время химическая промышленность производит много различных видов синтетических каучуков, превосходящих по некоторым свойствам натуральный...
-
Впервые в мире синтез изопрена из изобутилена и формальдегида в промышленном масштабе был осуществлен в СССР В 1964-1965 гг. В 1917 г. голландский химик...
-
Азотный кислота утилизация оксид Методы получения азотной кислоты Первый завод по производству HNO3 из аммиака коксохимического производства был пущен в...
-
Получение продукта конденсации карбамида и формальдегида холодным способом - Поликонденсация
Реактивы: Карбамид - 60 г (1 моль); формальдегид 40%-ный - 130 г (1,75 моля); уротропин - 3-4 г, щавелевая кислота - 0,3 г. Оборудование: Трехгорлая...
-
Технология получения стекла Технология получения стекла состоит из двух производственных циклов. Цикл технологии стекломассы включает операции: А)...
-
Процессы, основанные на микробиологической ферментации, разработаны и для получения ряда других органических кислот. Среди них -- глюконовая кислота и ее...
-
Заключение - Производство ацетона
Исследованием степеней превращения ацетона на полученных образцах контактных масс установлено см-3 температура прокалки не влияет на степень превращения...
-
Экология - Производство ацетона
Отходы защелачивания ацетона-сырца при производстве ацетона Код по ФККО 3 13 621 01 33 3 Наименование вида отходов Отходы защелачивания ацетона-сырца при...
-
Введение - Производство ацетона
Актуальность темы . Ацетон (или диметилкетон) является простейшим представителем кетонов. Является бесцветной легкоподвижной летучей жидкостью с...
-
Введение., Способы получения перхлоратов - Производство перхлоратов в промышленности
Получение перхлората калия или перхлоратов вообще имеет большое значение для промышленности. Ведь перхлораты широко используются как в проведении...
-
Процесс получения винилхлорида сбалансированным методом из этилена состоит из шести стадий: 1. синтез 1,2-дихлорэтана прямым жидкофазным хлорированием...
-
Описание процесса получения серной кислоты - Работа сернокислотного производства
Первая ступень мокрой очистки газа производится в cкруббере Вентури, где слабая 25 %-ная серная кислота для орошения газа подается насосами на два...
-
Полимеризация двуокиси азота. Переработка нитрозных газов в азотную кислоту обычно происходит при температурах от О до 50 °С. В этих условиях двуокись...
-
Действие на организм, Получение аммиака - Аммиак
Аммиак сильно раздражает слизистые оболочки уже при 0,5%-ном содержании его в воздухе. Острое отравление аммиаком вызывает поражения глаз и дыхательных...
-
ТЕХНОЛОГИЧЕСКИЕ СХЕМЫ ПОЛУЧЕНИЯ МАЗЕЙ., ПРИГОТОВЛЕНИЕ МАЗЕЙ В АПТЕКАХ - Производство мазей
ПРИГОТОВЛЕНИЕ МАЗЕЙ В АПТЕКАХ Приготовление мазей в аптеках. В аптеках мази готовят по экстемпоральным прописям, которые в среднем в нашей стране...
-
Выбор метода производства (или выделение) готового продукта Современные методы производства азотной кислоты основаны на применении синтетического аммиака...
-
В конце XIX в. началось промышленное производство молочной кислоты при участии молочнокислых бактерий Lactobacillus delbrueckii, L. leichmannii и L....
-
При строгом соблюдении порядка подготовки, пуска в работу или остановки объекта (как и отдельных видов оборудования) пропусков продуктов, как правило, не...
-
Общее описание метода В настоящее время самым современным и наиболее эффективным с экономической точки зрения является сбалансированный процесс...
-
Основы технологии получения хлорида калия - Производство хлорида калия галургическим способом
В основе получения хлорида калия галургическим методом лежат закономерности растворения в системе KCl-NaCl-. Обе соли относятся к числу хорошо...
-
Получение карбамидо формальдегидного продукта конденсации по горячему способу - Поликонденсация
Реактивы: Карбамид - 60 г; формалин 40%-ный - 200 г (мольное соотношение, 1:2,7); аммиак 25%-ный - 5,4 г; метиловый или этиловый спирт - 30 мл....
-
Производство высококонцентрированных кормовых препаратов - Этапы получения лизина
При получении высококонцентрированных кормовых препаратов лизина готовую культуральную жидкость предварительно подкисляют серной кислотой до pH 1,6-2,0....
-
Производство кормового препарата ЖКЛ (жидкого концентрата лизина) - Этапы получения лизина
Технология производства ЖКЛ основана на упаривании готовой культуральной жидкости до содержания 40% АСВ. Для этого предварительно нагретую до температуры...
-
Обогащение калийной руды производится двумя методами: флотационным и химическим (галургическим). Флотационный метод Флотационный метод стал...
-
Из перечисленного обзора типов ММ, составляющих предмет ИСО, можно выделить следующие особенности ММ ИСО [3]. - Системный подход, заставляющий...
-
Технологическое оформление процесса получения винилхлорида сбалансированным по хлору методом Первой стадией этого комбинированного процесса является...
-
Схема реакции: Реактивы: Фенолфталеин - 3,18 г; дихлорангидрид изофталевой кислоты - 2,03 г (мольное соотношение 1:1); едкий натр - 0,8 г;...
-
Введение - Оптимизация управлением производства на примере ОАО "Днепропетровский стрелочный завод"
Современный этап развития экономики характеризуется переходом предприятий на новые условия хозяйствования, необходимостью развития перспективных...
-
ПРОМЫШЛЕННОЕ ПРОИЗВОДСТВО: ТЕХНОЛОГИЧЕСКИЕ АСПЕКТЫ - Технология получения винилхлорида
На 2010 год существуют четыре основных способа получения винилхлорида, реализованные в промышленных масштабах. Винилхлорид можно получить различными...
-
Значение контролируемого Параметра Количество единиц продукции 60-70 70-80 80-90 90-100 100-110 20 80 110 150 50 Итого 410 Построить гистограмму и...
-
Сравнение методов получения хлорида калия - Производство хлорида калия галургическим способом
Флотационный метод обогащения по сравнению с галургическим (растворение и кристаллизация) имеет следующие преимущества: - флотация проходит при...
-
При пропускании смеси окиси углерода (СО) и водорода (Н2) над нагретым до 2000С катализатором, содержащим восстановленное железо, образуются смеси...
-
МИРОВОЕ ПРОИЗВОДСТВО ВИНИЛХЛОРИДА - Технология получения винилхлорида
Винилхлорид является одним из крупнейших по объему органических полупродуктов мирового химического производства, уступая лишь этилену (113 млн. тонн в...
-
Еще в начале 20 века было установлено, что при взаимодействии СО и Н2 в присутствии соответствующих катализаторов можно получить углеводороды. Так, в...
-
Схема 1. Технологическая схема производства серной кислоты по методу ДК. 1-серная печь; 2- котел-утилизатор; 3- экономайзер; 4- пусковая топка;...
-
Методы очистки коллоидных растворов - Методы очистки и получения коллоидных растворов
При получении коллоидных растворов тем или иным методом, особенно с помощью химических реакций, практически невозможно точно предусмотреть необходимое...
-
Диспергированием называют тонкое измельчение твердых мате-риалов или жидкостей и распределение их частиц в жидкой или газообразной среде, в результате...
Физико-химические закономерности получения продукта - Производство ацетона